Introdução
A vacinação contribuiu para o alcance de resultados positivos na Saúde Pública do Brasil, a exemplo da eliminação da poliomielite, interrupção da transmissão do sarampo e da rubéola, redução intensa da incidência de difteria, coqueluche, meningite causada por H. influenzae tipo B,1 tétano, tuberculose em menores de 15 anos de idade, além da redução significativa na mortalidade infantil.2 Destaca-se, ademais, a eliminação da febre amarela urbana e a erradicação da varíola.3 Houve declínio nas taxas de hospitalizações e de mortalidade por doenças imunopreveníveis,4 no Brasil e em outros países.5 O Programa Nacional de Imunizações (PNI) é considerado a intervenção de Saúde Pública de maior sucesso no Brasil.6
O Sistema de Informações do Programa Nacional de Imunizações (SI-PNI) permite estimar as coberturas vacinais e sua homogeneidade entre as vacinas e entre os municípios das Unidades da Federação do país, com boa aceitabilidade e representatividade.7 Apesar das adequadas coberturas vacinais nos âmbitos nacional e estadual, nos municípios as coberturas são heterogêneas, menores nos grupos socioeconômicos mais altos e nos mais baixos.8 A vacinação ainda não alcança toda a população-alvo9,10 e a baixa cobertura pode estar relacionada ao nível de conhecimento, atitudes e práticas sobre ações de vacinação.11 Essa situação demanda atenção especial no nível local, desde que a poliomielite e o sarampo, por exemplo, continuam a ser problemas sanitários em países da Ásia, África Central e Oriente Médio,12 com os quais o Brasil mantém intercâmbio comercial e turístico.
A Organização Mundial da Saúde (OMS) recomenda pelo menos 95% de cobertura vacinal para manutenção da erradicação, eliminação ou controle de doenças imunopreveníveis, além de indicadores como a proporção de municípios com coberturas vacinais adequadas e a proporção de crianças vivendo em municípios com coberturas vacinais adequadas.13 No Brasil, também se adota a homogeneidade de cobertura entre vacinas, medida pela proporção desses imunobiológicos cujas metas de coberturas foram alcançadas em cada município.14 Esses indicadores devem ser acompanhados por um sistema de vigilância do risco de transmissão de doenças imunopreveníveis no município e em áreas com a presença de suscetíveis, característica de situações que merecem intervenções oportunas.15 O sistema de vigilância deve garantir (i) coberturas adequadas, evitando doenças e mortes desnecessárias,16 (ii) alertas para incentivar a adesão às vacinações agendadas e (iii) chamadas para atualização de vacinas atrasadas.17
Têm-se empreendido esforços pela obtenção de informações confiáveis para monitoramento dos programas de imunizações.18 O método administrativo disponibiliza dados da rotina de forma mais barata e oportuna, enquanto os inquéritos domiciliares constituem a única fonte de estimativas reais de coberturas vacinas,19 embora estes sejam morosos e de alto custo. Os dois métodos são utilizados no país; contudo, o monitoramento sistemático da situação de risco não foi totalmente implantado, apesar de os indicadores de cobertura e homogeneidade terem sido pactuados no Sistema Único de Saúde brasileiro, o SUS.20,21
Este estudo teve por objetivo descrever a classificação de risco de transmissão de doenças imunopreveníveis nos municípios brasileiros.
Métodos
Trata-se de um estudo epidemiológico descritivo com dados secundários referentes às coberturas de dez vacinas administradas em 2014, na população menor de dois anos de idade residente nos 5.570 municípios brasileiros. Trata-se das seguintes vacinas: (i) bacilo de Calmette e Guérin (BCG); (ii) febre amarela (FA); (iii) hepatite A (HA); (iv) meningocócica C conjugada (meningo C); (v) difteria, tétano, pertussis, hepatite B e Haemophilus influenzae b (pentavalente); (vi) pneumocócica 10 valente (pneumo 10); (vii) poliomielite inativada (VIP)/poliomielite atenuada oral (VOP) (poliomielite); (viii) sarampo, caxumba e rubéola (tríplice viral); (ix) sarampo, caxumba, rubéola e varicela atenuada (tetraviral); e (x) rotavírus humano (VORH).
A situação vacinal foi verificada utilizando-se os indicadores de cobertura vacinal (CV) e homogeneidade de coberturas vacinais entre vacinas no município (HCV), ambos pactuados no SUS por meio do Contrato Organizativo de Ação Pública da Saúde (COAP)20 e do Programa de Qualificação das Ações de Vigilância em Saúde (PQAVS).21 Também foram avaliados os indicadores de proporção de abandono (PA), proporção de crianças menores de dois anos vivendo em municípios com cobertura vacinal adequada (PCVA) e risco de transmissão de doenças imunopreveníveis no município (RTDI).
Em relação às CV, o PNI estabeleceu a meta de 90% para as vacinas BCG e VORH, 95% para pentavalente, poliomielite, penumo 10, meningo C, tríplice viral, tetraviral e HA, e 100% para FA. A CV teve como numerador o total de doses que completam o esquema de cada vacina, e como denominador, o número de nascidos vivos no município registrados no Sistema de Informações sobre Nascidos Vivos (Sinasc) para o ano de 2012, utilizados para estimativas de crianças menores de um ano e de dois anos de idade. As CV foram obtidas no SI-PNI: http://pni.datasus.gov.br
Foram estabelecidas duas etapas de análise: (I) categorização dos indicadores CV, PA e HCV e (II) classificação do risco de transmissão de doenças imunopreveníveis nos municípios. A CV recebeu três classificações: baixa (<meta); adequada (≥meta a ≤120%); e elevada (>120%). Quanto à homogeneidade, o COAP definiu que o município deve alcançar a meta para 75% ou mais das vacinas, enquanto no PQAVS, essa proporção foi estabelecida em 100%. A HCV foi arbitrada em três classes: baixa (<75%); adequada para o COAP (≥75%); e adequada para o PQAVS (=100%). Para HCV nos 3.527 municípios com recomendação de vacinação contra FA (ACRV), foram consideradas as dez vacinas; nos demais, nove. A proporção de abandono - obtida em http://tabnet.datasus.gov.br - foi calculada somente para vacinas com esquema multidoses (meningo C, pentavalente, pneumo 10, poliomielite, VORH), considerando-se a diferença entre o número de primeiras doses e o número de últimas doses do esquema vacinal, dividido pelo número das primeiras doses, multiplicando-se o resultado por 100, estratificando-se em três categorias: baixa (<5%); média (≥5% a ≤10%); e alta (>10%). Para a proporção de crianças menores de dois anos em municípios com cobertura vacinal adequada, o numerador constituiu-se da população de crianças menores de dois anos dos municípios com HCV prevista no COAP e no PQAVS, e o denominador, o total de crianças dessa faixa etária existente em cada município. Os municípios foram classificados pelo porte populacional, adaptado do referencial do PQAVS: pequeno porte (≤20.000 habitantes); médio porte (≥20.001 a ≤100.000 habitantes); e grande porte (≥100.001 habitantes).
O risco de transmissão de doenças imunopreveníveis no município foi composto pelos indicadores de cobertura vacinal, homogeneidade de coberturas vacinais entre vacinas, proporção de abandono e porte populacional do município, definindo-se cinco categorias:
risco muito baixo - município com HCV=100%;
risco baixo - município com HCV≥75% a <100%, com CV adequada para as vacinas poliomielite, tríplice viral e tetraviral, as quais previnem doenças eliminadas ou em fase de eliminação (poliomielite, sarampo e rubéola), e ainda, a vacina pentavalente, devido ao componente contra difteria-tétano-pertussis (DTP), considerado como "marcador" de qualidade de serviço de vacinação devido ao esquema de três doses injetáveis até os seis meses de idade;
risco médio - município com HCV ≥75% a <100%, porém com cobertura vacinal abaixo da meta para uma ou mais das vacinas poliomielite, tríplice viral, tetraviral ou pentavalente;
risco alto - município com HCV <75%; e
risco muito alto - município de grande porte populacional, com HCV <75% e alta PA (≥10%), incluídos neste grupo os municípios sem registro de vacinação, independentemente do porte populacional.
No tratamento automatizado e análise dos dados, utilizou-se o programa Epi Info 2000 versão 3.5.1. (Centers for Disease Control and Prevention, Atlanta, USA, 2008).
Por envolver apenas o uso de dados secundários, sem identificação de indivíduos, o estudo atendeu às considerações éticas previstas na Resolução do Conselho Nacional de Saúde (CNS) nº 466, de 12 de dezembro de 2012, e foi dispensado de aprovação prévia por Comitê de Ética em Pesquisa.
Resultados
Em 2014, verificou-se que 54,2% dos municípios brasileiros alcançaram a meta de CV para vacina BCG, 39,6% para FA, 66,8% para hepatite A, 62,2% para meningo C, 60,9% para pentavalente, 58,2% para pneumo 10, 60,9% para poliomielite, 32,4% para tetraviral, 77,3% para tríplice viral e 67,7% para VORH. As vacinas BCG, FA e tetraviral tiveram maior percentual de municípios com cobertura muito baixa e baixa (Figura 1). Observou-se 409 municípios com coberturas vacinais iguais a zero. Não houve dados de cobertura vacinal para cinco municípios: Mojuí dos Campos (Pará), Paraíso das Águas (Mato Grosso do Sul), Pinto Bandeira (Rio Grande do Sul), Balneário Rincão e Pescaria Brava (Santa Catarina). Excluindo-se as coberturas vacinais iguais a zero, as demais coberturas variaram de 0,1% para FA a 3.240,0% para hepatite A. Nas Unidades da Federação, as coberturas variaram de 19,6% para FA em São Paulo a 166,0% para hepatite A no Espírito Santo. No âmbito nacional, a menor cobertura foi de 46,7% para FA, e a maior, de 120,3% para hepatite A, sendo que das dez vacinas avaliadas, alcançou-se cobertura adequada para seis delas.
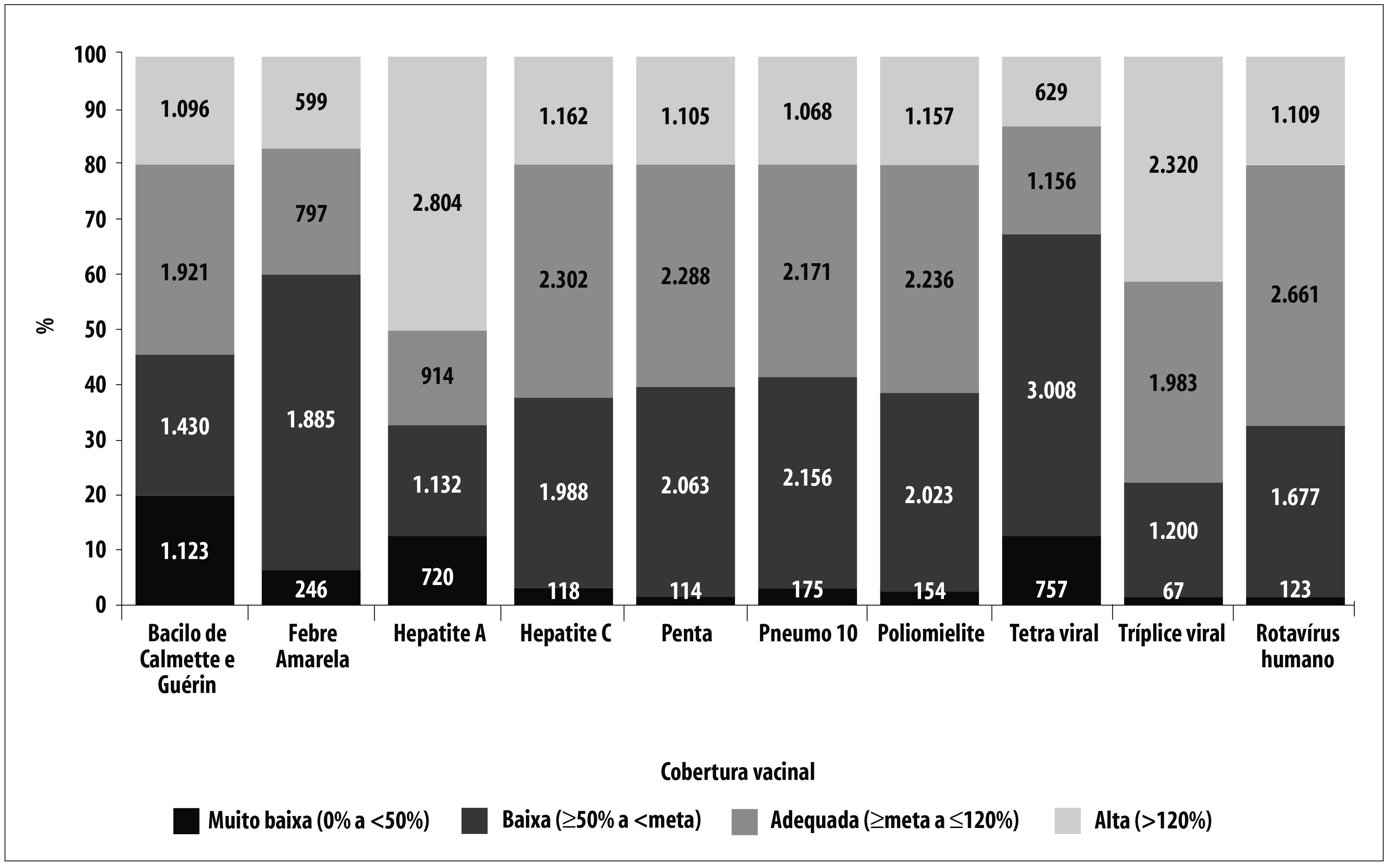
Figura 1 - Distribuição dos municípios (N e %) conforme a classificação da cobertura de dez vacinas, Brasil, 2014
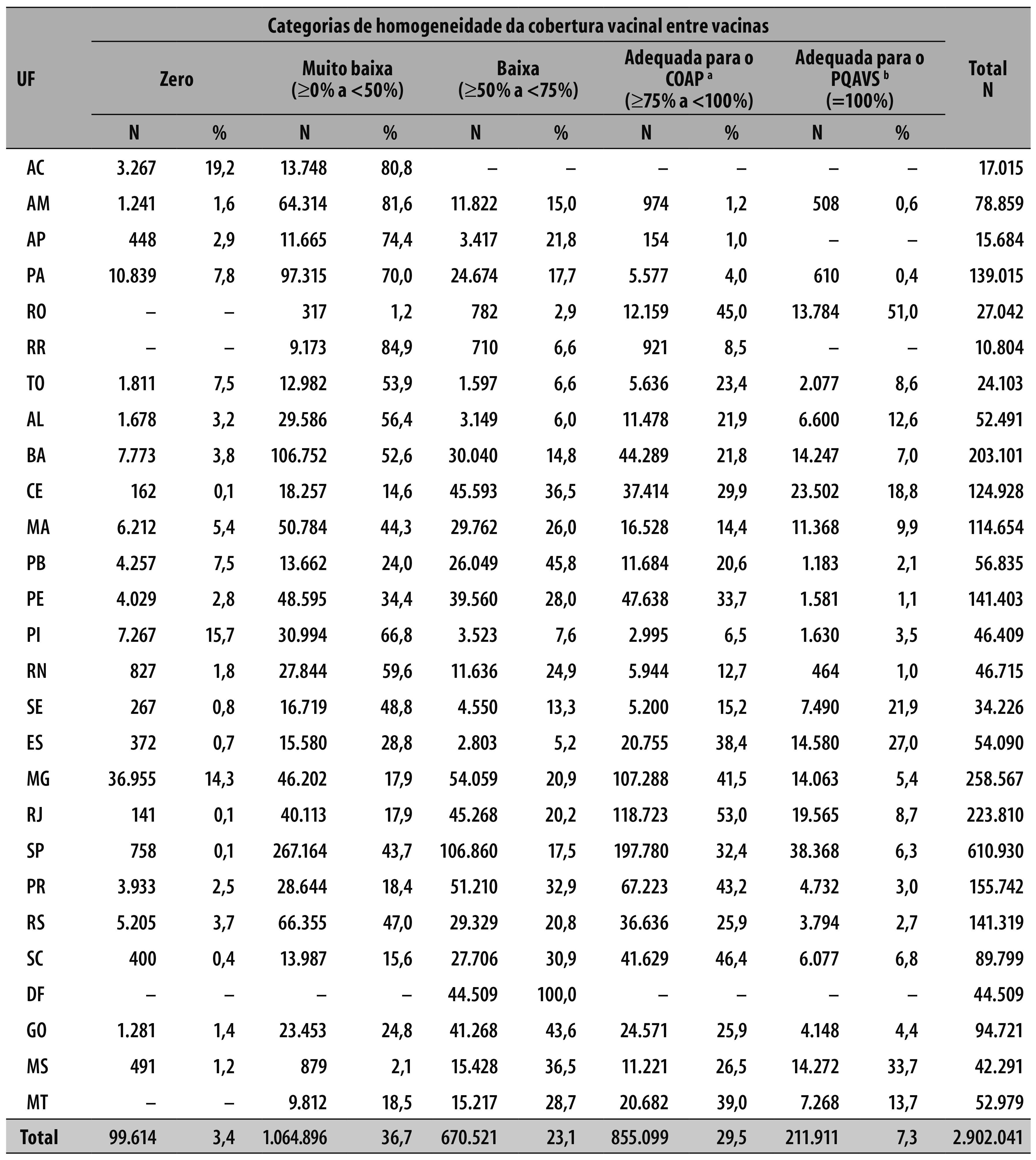
A homogeneidade foi adequada para o PQAVS em 667 (12,0%) municípios. Em outros 1.775 (31,9%) municípios, a homogeneidade atendeu aos requisitos do COAP, em 2.801 (50,3%) foi baixa ou muito baixa e em 327 (5,9%) foi igual a zero. O estado do Mato Grosso do Sul alcançou 54,4% dos municípios com homogeneidade de cobertura, pelo critério do PQAVS, enquanto Rondônia teve 61,5% de municípios com homogeneidade de cobertura segundo o COAP (Tabela 1).
Tabela 1 - Distribuição dos municípios (N e %) por unidade da federação (UF) conforme a categoria da homogeneidade de cobertura vacinal, Brasil, 2014

a) COAP: Contrato Organizativo da Ação Pública da Saúde
b) PQAVS: Programa de Qualificação das Ações de Vigilância em Saúde
Do total de 2.902.041 menores de dois anos de idade, 14,9% residiam em municípios de pequeno porte (70,2% do total de municípios), 28,3% em municípios de médio porte (24,6% dos municípios) e 56,8% dessas crianças residiam em municípios de grande porte (5,2% dos municípios). Observou-se que 29,5% da população-alvo residia em municípios com homogeneidade de cobertura adequada para o COAP e 7,3% com homogeneidade de cobertura adequada para o PQAVS (Tabela 2).
Tabela 2 - Distribuição da população de crianças menores de dois anos de idade (N e %) vivendo em municípios conforme categorias de homogeneidade de cobertura vacinal, nas Unidades da Federação (UF). Brasil, 2014
a) COAP: Contrato Organizativo da Ação Pública da Saúde
b) PQAVS: Programa de Qualificação das Ações de Vigilância em Saúde
O percentual de municípios com baixa proporção de abandono variou de 41,7% para vacina poliomielite a 62,9% para meningo C. A vacina poliomielite também teve o maior percentual de municípios com alta proporção de abandono (39,6%); o menor percentual de abandono (18,9%) foi para meningo C (Figura 2). A proporção de abandono oscilou de -543,4% (negativa) para meningo C a 100,0% (positiva) para pneumo 10.
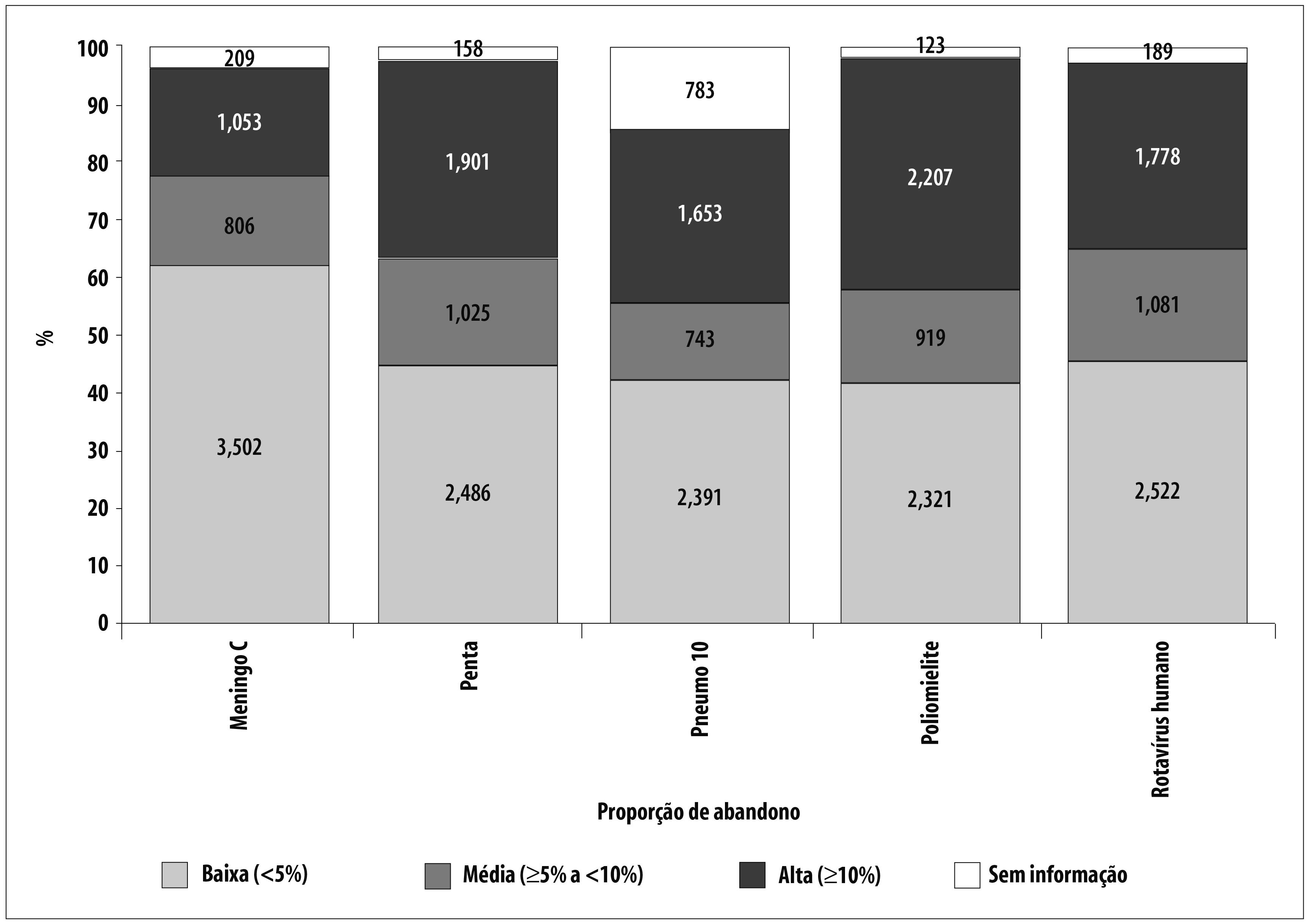
Figura 2 - Distribuição dos municípios (N e %) conforme a classificação da proporção de abandono de cinco vacinas. Brasil, 2014
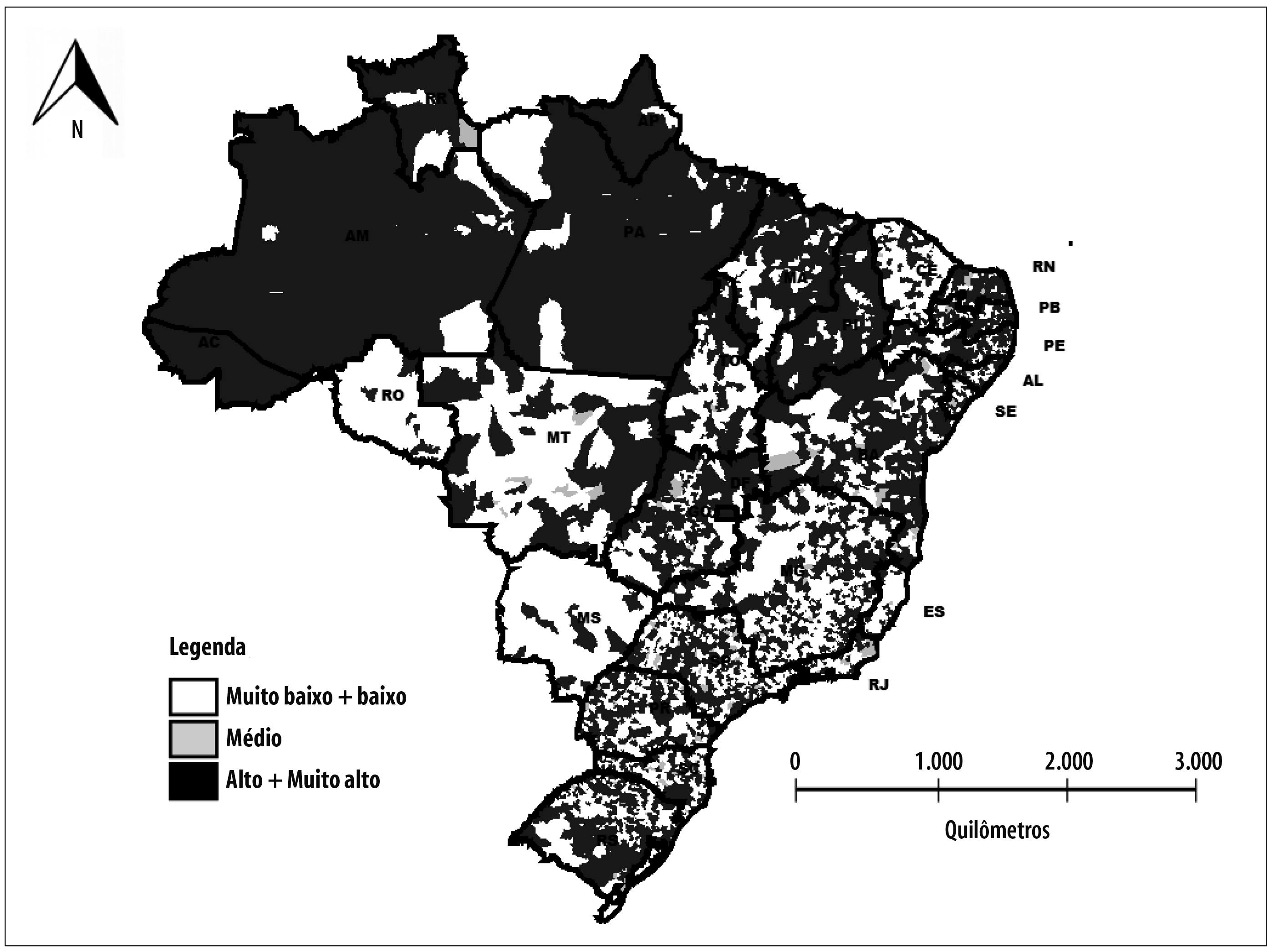
O indicador de risco de transmissão de doenças imunopreveníveis detectou dois grupos principais: o primeiro grupo, de baixo risco, correspondeu a 1.650 (29,6%) municípios; o segundo grupo, de alto risco, 3.027 (54,3%) municípios. No grupo de risco muito baixo, foram registrados 667 (12,0%) municípios. No grupo de médio risco, foram 125 (2,2%) municípios, enquanto no grupo de risco muito alto, encontrou-se 101 (1,8%) municípios. Predominaram municípios de pequeno porte populacional nos grupos de menor risco, variando de 68,2% no grupo de risco baixo a 73,6% no grupo de risco médio. No grupo de risco muito alto, predominaram os municípios de grande porte populacional (95,0%), conforme esperado. A análise espacial do risco de transmissão de doenças imunopreveníveis identificou que os municípios com risco muito baixo e risco muito alto se distribuíram por todos os estados brasileiros. Porém, houve maior concentração de municípios com risco alto e risco muito alto nos estados do Acre, Amazonas, Amapá, Pará, Piauí e Roraima (Figura 3).
Discussão
O alcance das metas de coberturas vacinais pelos municípios, possivelmente, é o maior desafio para o PNI no momento. Este estudo mostrou que vários municípios não atingiram coberturas adequadas, principalmente para as vacinas tetraviral, FA e BCG. Em alguns municípios, a BCG é administrada nas maternidades logo após o nascimento da criança, promovendo altas coberturas, ao contrário daqueles municípios que não ofertam essa vacina nos estabelecimentos hospitalares destinados ao parto. Observou-se grande proporção de municípios com altas proporções de abandono para algumas vacinas, resultado acorde com outro estudo.22 A classificação da cobertura vacinal e da proporção de abandono foram semelhantes àquelas observadas em pesquisa sobre vacinação no Brasil.4 A homogeneidade seguiu padrões pactuados no SUS;20,21 entretanto, esses padrões podem ser alterados conforme a necessidade dos gestores, exigindo adaptação da vigilância a novos indicadores introduzidos.
A análise conjunta da cobertura vacinal, da homogeneidade e da proporção de abandono possibilitou melhor entendimento do risco de transmissão de doenças imunopreveníveis nos municípios brasileiros, constituindo uma nova ferramenta para o gestor direcionar ações oportunas em locais com maior fragilidade da situação vacinal, conforme outros autores têm defendido,23 em resposta às ameaças de epidemias e da emergência de doenças imunopreveníveis. As cinco categorias de risco possibilitarão mais opções de priorização de ações, devido ao grande número de municípios de alto risco. Posteriormente, essa categorização poderá ser reduzida para três níveis - baixo, médio e alto risco -, conforme estudo anterior, no qual cada prioridade recebeu diversos níveis de hierarquia:16 em relação à pesquisa referida, o diferencial deste estudo reside na ausência de hierarquias de prioridades e no processamento automatizado dos indicadores, possibilitando a elaboração rápida de um boletim para vigilância da situação vacinal nos municípios.
O presente trabalho permitiu identificar: maioria dos municípios com alto risco de doenças imunopreveníveis; coberturas vacinais atípicas (muito baixas; ou muito elevadas) em alguns municípios, possivelmente devidas a duplicidade de registro de doses aplicadas, subestimação da população ou falta de registro individual do vacinado por local de residência; oscilação nas proporções de abandono de valores negativos, decorrente do maior número de vacinados com a última dose do esquema vacinal quando comparados àqueles vacinados com a primeira dose, até abandono completo do esquema de algumas vacinas; municípios com homogeneidade igual a zero e vários com homogeneidade muito baixa; minoria das crianças vivendo em municípios com homogeneidade de cobertura adequada; e inexistência de informação sobre vacinação em alguns municípios. Essa situação evidenciou duas questões fundamentais.
A primeira questão remete a possíveis inconsistências nos dados do SI-PNI devidas ao registro - em alguns municípios - de dados agregados por local de ocorrência (ao invés do registro de dados individuais por residência do vacinado), capazes de distorcer as coberturas vacinais e proporções de abandono, interferindo no indicador de risco. A consistência dos dados do sistema de informações pode contribuir para a melhoria das coberturas, principalmente no seguimento individual das crianças, melhorando a oportunidade dos esquemas vacinais.24 Vacinação inválida também interfere nas coberturas mas pode ser minimizada com um bom sistema de informações. O desvio do prazo para vacinação pode levar a baixa proteção contra doenças imunopreveníveis ou requerer a repetição da dose, causando perda evitável de tempo, recursos materiais e financeiros.25 Abordagens sobre uso da informações para o direcionamento das ações no nível local têm ajudado a melhorar as coberturas vacinais em vários países,26 sendo imprescindível que os municípios mantenham os registros de vacinação no SI-PNI com qualidade e atualizados.
A segunda questão diz respeito ao monitoramento da qualidade dos serviços de vacinação. Deve-se averiguar a confiança da comunidade nas vacinas e no serviço de imunização oferecido.27 Se a vacinação buscar tão somente o cumprimento do calendário ou responder a situações impositivas, ela ficará desassociada do cuidado das famílias com frágil sustentabilidade.28 A integração das ações do programa de vacinação com a Estratégia Saúde da Família pode ampliar seu alcance na comunidade, impactando positivamente as ações de imunoprevenção.29 Com o aumento da credibilidade, as coberturas vacinais melhoram enquanto as proporções de abandono tendem a declinar.30 O acesso aos serviços também pode afetar as coberturas vacinais, seja em função de áreas caracterizadas pela violência, seja pela dificuldade de acesso geográfico como acontece com áreas indígenas ou assentamentos agrícolas.16 Outros aspectos a considerar são a falta de disponibilidade de tempo dos pais para conduzir suas crianças e o posto de saúde encontrar-se fechado,2 sendo recomendável a oferta de horários alternativos para vacinação.
A vigilância das coberturas requer avaliações sistemáticas e recomendações aos gestores de ações corretivas, priorizando os municípios conforme a classificação da situação de risco. Deve-se atentar para a atualização dos dados no SI-PNI, local e nacional, com correção das coberturas vacinais e proporções de abandono atípicas e realização de monitoramento rápido de coberturas, uma vez que a classificação de risco baseada exclusivamente em dados administrativos pode não refletir a cobertura real de cada vacina. É preciso incluir ações e metas de imunizações na Programação Anual de Saúde (PAS) e no Plano Plurianual (PPA) dos estados e municípios, para ampliar a governabilidade sobre a melhoria das coberturas. A distribuição, o armazenamento e a administração qualificada das vacinas também podem contribuir com a manutenção de coberturas vacinais adequadas, mesmo em situações de escassez desses produtos. Finalmente, faz-se necessário conhecer os locais e os problemas a demandar ações oportunas.
A classificação de risco de transmissão de doenças imunopreviníveis oferece uma ferramenta adicional para identificação de áreas prioritárias, onde as ações poderão ser direcionadas pelos gestores, melhorando a qualidade e contribuindo para o sucesso do Programa Nacional de Imunizações nos municípios, Unidades da Federação e, por conseguinte, no plano da nação.










 texto en
texto en