Apresentação
As hepatites virais constituem um dos temas que compõem o Protocolo Clínico e Diretrizes Terapêuticas (PCDT) para Atenção Integral às Pessoas com Infecções Sexualmente Transmissíveis (IST), sendo mais especificamente abordado no PCDT para Hepatite B e Coinfecções e PCDT para Hepatite C e Coinfecções, publicados pela Secretaria de Vigilância em Saúde do Ministério da Saúde do Brasil. Os referidos documentos foram aprovados pela Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec).1-3Para a elaboração do presente artigo, foram realizadas seleção e análise de evidências disponíveis na literatura e discussão por especialistas em IST em 2020.
Aspectos epidemiológicos
As hepatites virais A, B e C são causadas por vírus que apresentam tropismo primário pelo tecido hepático, constituindo grande desafio à saúde pública em todo o mundo. Globalmente, essas infecções são responsáveis por mais de 1,34 milhão de óbitos anualmente, dos quais 66% são causadas pela hepatite B, 30% pela hepatite C e 4% pela hepatite A.4 Essas mortes decorrem principalmente das complicações das formas crônicas das hepatites, como insuficiência hepática, cirrose e hepatocarcinoma.5 Dados tão significativos levaram a Organização Mundial da Saúde (OMS) a assumir, como um dos seus objetivos, eliminar as hepatites virais até 2030.6
No período de 1999 a 2019, o Sistema de Informação de Agravos de Notificação (Sinan) registrou a ocorrência de 673.389 casos de hepatites virais no Brasil. Destes, 168.036 (25%) foram referentes à hepatite A, 247.890 (36,8%) à hepatite B, 253.307 (37,6%) à hepatite C e 4.156 (0,6%) à hepatite D.7
O vírus da hepatite A (hepatitis A virus, HAV) pertence à família Picornaviridae e seu genoma é composto por ácido ribonucleico (ribonucleic acid, RNA), comumente transmitido por meio de contato orofecal e ingestão de água ou alimentos contaminados. Sua transmissão sexual tem sido relatada especialmente entre homens que fazem sexo com homens, o que reforça a necessidade de incluir as medidas de prevenção entre adultos.8-12
O vírus da hepatite B (hepatitis B virus, HBV) pertence à família Hepadnaviridae, cujas variações genéticas permitem reconhecer dez diferentes genótipos, aspecto de importância epidemiológica, clínica e terapêutica.13, 14Dentre os vírus considerados hepatotróficos, é o único com material genômico composto por ácido desoxirribonucleico (deoxyribonucleic acid, DNA). Os meios mais frequentes de transmissão do HBV são a exposição parenteral ou percutânea, vertical e sexual.7 O sangue é o veículo de transmissão mais importante, mas outros fluidos também podem transmitir o HBV, como sêmen e conteúdo vaginal.15 As rotas de transmissão predominantes variam de acordo com a prevalência da infecção pelo HBV. Em áreas com alta prevalência, a via perinatal e a horizontal por contato próximo na infância são as principais formas de transmissão do vírus.16, 17Em áreas de baixa prevalência, a via percutânea e o contato sexual são as formas de maior risco de contaminação.18
O vírus da hepatite C (hepatitis C virus, HCV) pertence à família Flaviviridae, cujo material genético é formado por fita única de RNA de sentido positivo; sua variação genética permite reconhecer sete genótipos diferentes.19 Sua transmissão ocorre por meio da exposição percutânea, sexual e vertical. As frequências de ocorrência para cada uma dessas categorias variam conforme a população estudada e a concomitância de fatores associados. No entanto, ressalta-se que a via parenteral é muito mais eficiente e prevalente na transmissão do HCV do que a transmissão sexual e vertical. O maior número de novas infecções vem sendo observado entre usuários de drogas injetáveis e pelo compartilhamento de seringas.20, 21
Sobre a transmissão sexual do HCV, sabe-se que é mais frequente entre homens que fazem sexo com homens.22 Como em outras infecções de transmissão sexual, a presença de outras IST, a exemplo da infecção pelo vírus da imunodeficiência humana (human immunodeficiency virus, HIV) e práticas sexuais desprotegidas, especialmente aquelas com maior risco de sangramento mucoso (sexo anal sem uso de lubrificantes, introdução de partes do membro superior na vagina ou no ânus, sexo grupal, compartilhamento de objetos sexuais e prática de sexo sob influência de drogas psicoativas), constituem importante grupo de situações e fatores facilitadores de transmissão do HCV.23, 24Apesar de a transmissão do HCV ser mais baixa em pessoas com hábitos heterossexuais, ela se eleva entre aquelas com grande número de parcerias sexuais ou que praticam sexo anal.21
Aspectos clínicos
A hepatite A é autolimitada, não evolui para doença crônica e tem na vacina a sua principal forma de controle.25 Seu período de incubação varia de 15 a 50 dias e é sintomática em 70% dos adultos.26, 27 Caracteriza-se por início súbito de náusea, vômitos, anorexia, febre, mal-estar e dor abdominal, seguida por icterícia, colúria, acolia e prurido.28 Pessoas infectadas pelo HAV transmitem o vírus durante o período de incubação, que dura entre um e seis meses, persistindo até uma semana depois do início da icterícia.29
A hepatite pelo HBV pode mostrar-se como doença aguda ou crônica. Na forma aguda, cerca de 70% dos casos apresentam a forma subclínica e 30% a forma ictérica, eventualmente um curso mais grave da doença.30, 31Na fase aguda, as manifestações clínicas como anorexia, astenia, mal-estar, náusea, icterícia, colúria e dor no quadrante superior direito do abdome são indistinguíveis de outras hepatites virais.32
Na hepatite pelo HBV, a proporção de progressão de infecção aguda para crônica em indivíduos imunocompetentes é determinada principalmente pela idade em que a infecção ocorre, sendo de 90% na transmissão vertical,33 de 20% a 50% entre 1 e 5 anos de idade34, 35e de 0 a 10% após a adolescência.12, 36Na sua forma crônica, a hepatite B é frequentemente assintomática, mas pode evoluir para insuficiência hepática crônica, cirrose e hepatocarcinoma.37
Sobre a infecção causada pelo HCV, observa-se que cerca de 50% a 85% das pessoas evoluem para a forma crônica da infecção, apresentando manifestações clínicas inespecíficas como cansaço, alterações do sono, náusea, diarreia, dor abdominal, anorexia, mialgia, artralgia, fraqueza, alterações comportamentais e perda de peso.38, 39Manifestações extra-hepáticas incluem crioglobulinemia, glomerulonefrite membrano-proliferativa, tireoidite autoimune, porfiria cutânea tarda, entre outras.40 Na ausência de eliminação viral espontânea e de tratamento, 20% dos casos de infecção pelo HCV evoluem para cirrose ao longo do tempo.41
Diagnóstico
O diagnóstico das hepatites virais A, B e C baseia-se na detecção de marcadores sorológicos (antígenos virais e anticorpos específicos) e molecular (ácido nucleico viral) no sangue, soro, plasma ou fluido oral da pessoa infectada, por meio de imunoensaios ou de técnicas de biologia molecular.12, 42, 43 A incorporação dos testes rápidos ao Sistema Único de Saúde (SUS) do Brasil ampliou as oportunidades de testagem e de diagnóstico precoce dessas infecções, os quais podem ser realizados em locais sem infraestrutura laboratorial ou de difícil acesso.44
Para o diagnóstico da hepatite A aguda, utilizam-se testes de imunoensaio que detectam anticorpos IgM anti-HAV no soro (até seis meses após o início dos sintomas). A pesquisa por anticorpos IgG anti-HAV, seja por testes anti-HAV IgG ou anti-HAV total (IgM e IgG), auxilia na identificação de indivíduos não imunizados ou previamente infectados. Esses exames devem ser sempre solicitados para pessoas expostas a situações de risco para essa infecção.44, 45 A presença de anticorpos IgG anti-HAV indica imunidade duradoura.46
A maioria das pessoas infectadas pelo HBV é assintomática e diagnosticada na fase crônica da doença. A Figura 1 ilustra a dinâmica temporal da variação dos marcadores da infecção.47 A definição sucinta desses marcadores consta na Figura 2.48 Para a triagem da infecção, é utilizado teste laboratorial de imunoensaio ou teste rápido visando à detecção do antígeno de superfície do HBV (HBsAg). Nos casos positivos, a complementação diagnóstica é feita com o anti-HBc total e, se disponível, com teste molecular (HBV-DNA). O HBeAg, anti-HBe e anti-HBs, juntos aos demais marcadores, auxiliam na avaliação da fase clínica e monitoramento evolutivo da infecção.16, 37, 42-44, 49
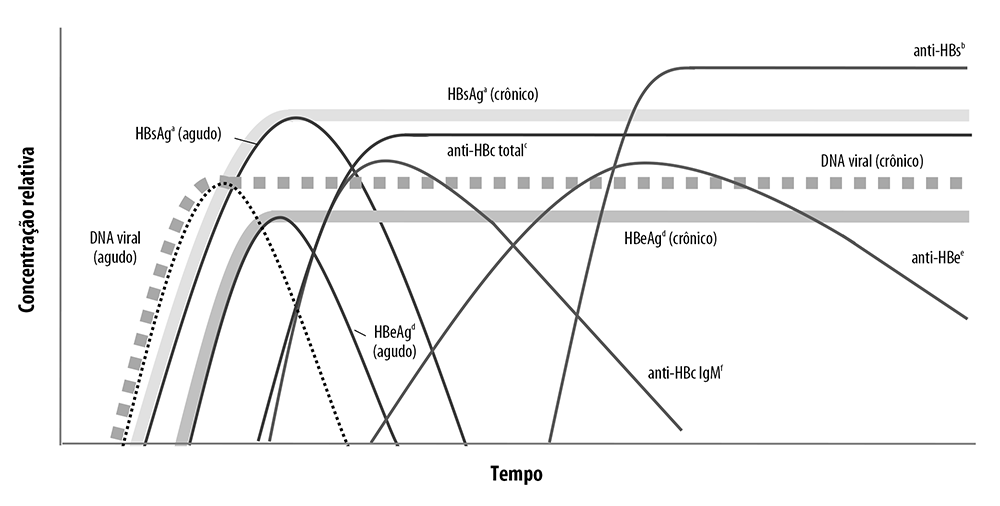
Fonte: modificado e adaptado de Sablon & Shapiro, 2005.47
Notas: a) HBsAg - antígeno de superfície do vírus da hepatite B (HBV);b) Anti-HBs - anticorpo contra o antígeno de superfície do HBV; c) Anti-HBc Total - anticorpo das classes IgM e IgG contra o antígeno do núcleo do HBV; d) HBeAg - antígeno “e” do HBV; e) Anti-HBe - anticorpo contra o antígeno “e” do HBV; f) Anti-HBc IgM - anticorpo da classe IgM contra o antígeno do núcleo do HBV.
Figura 1 Marcadores séricos da infecção causada pelo vírus da hepatite B de acordo com o tempo de evolução da infecção
Figura 2 Interpretação dos marcadores da infecção pelo vírus da hepatite B
| Marcador | Interpretação |
|---|---|
| HBsAga | Marcador de infecção atual pelo vírus da hepatite B (HBV), seja aguda ou crônica. Detectado na fase inicial da infecção aguda. Sua persistência por mais de 6 meses sinaliza para a infecção crônica. |
| HBV-DNAb | Marcador de intensidade da replicação viral. Presente na fase inicial da infecção aguda, podendo ser detectado antes do HBsAg. Na infecção crônica, sua presença é detectável na maioria dos casos. Sua quantificação é útil na classificação da forma clínica da infecção crônica. |
| HBeAgc | Marcador da replicação viral. Sua detecção indica elevada replicação e infecciosidade do HBV. Está presente na fase aguda e em algumas formas crônicas. |
| Anti-HBed | O início da detecção coincide com o declínio da concentração de HBeAg. Sua presença indica redução da replicação viral. Algumas formas replicativas da doença crônica apresentam esse anticorpo na ausência do HBeAg. |
| Anti-HBc IgMe | Marcador de infecção recente pelo HBV. Presente durante a fase aguda da infecção. Eventualmente, pode ser detectado na reagudização de casos crônicos. |
| Anti-HBc IgGf | O início da detecção acontece durante a fase aguda da infecção e persiste por tempo indeterminado. Sua presença indica infecção vigente (quando o HBsAg está positivo) ou contato prévio com o HBV. |
| Anti-HBsg | Indica imunidade contra o HBV. Presente após o desaparecimento do HBsAg (cura funcional) ou em resposta à vacina. |
Fonte: adaptado de Liang, 2009.48
Notas: a) HBsAg - antígeno de superfície do HBV; b) HBV-DNA - ácido nucleico viral; c) HBeAg - antígeno “e” do HBV; d) Anti-HBe - anticorpo contra o antígeno “e” do HBV; e) Anti-HBc IgM - anticorpo da classe IgM contra o antígeno do núcleo do HBV; f) Anti-HBc IgG - anticorpo IgG contra o antígeno do núcleo do HBV; g) Anti-HBs - anticorpo contra o antígeno de superfície do HBV.
Na hepatite B aguda, o HBsAg, HBeAg, anti-HBc IgM e o HBV-DNA são os primeiros marcadores a serem detectados. A presença do HBsAg é confirmação da infecção, podendo ser detectada de duas a 12 semanas após a exposição ao vírus. Sua negativação, quando a infecção é debelada, acontece semanas após a detecção, podendo se prolongar por até seis meses. O anti-HBc IgM evolui para negatividade após controle da infecção aguda, mas, em casos de reagudização da hepatite B, pode ser detectado.48
O HBeAg é marcador da intensa replicação viral e sua detecção relaciona-se à alta infecciosidade do HBV.48 Os anticorpos anti-HBc IgG também aparecem precocemente e normalmente persistem pelo resto da vida. Não servem para classificar forma clínica, pois todos os indivíduos que foram infectados, curados ou não, apresentam esse marcador. Tem uso epidemiológico, pois indica contato prévio com o vírus ou infecção vigente. A presença de anticorpos anti-HBe indica o início da recuperação, mas muitos indivíduos com forma crônica replicativa da doença podem apresentar esse marcador na ausência do HBeAg.50 O marcador anti-HBs surge durante a fase de convalescença, após o desaparecimento do HBsAg. Sua presença indica imunidade contra o HBV. Na ausência do anti-HBs, o anti-HBc total passa a ser o único marcador isolado da infecção prévia. Em indivíduos não expostos ao HBV (anti-HBc IgG negativos), a presença de anticorpos anti-HBs indica imunidade pela resposta vacinal contra a hepatite B.51
Na incapacidade de resolução da infecção aguda, alguns indivíduos tornam-se portadores crônicos do HBV. Nesses casos, a persistência do HBsAg por mais de seis meses sinaliza para a infecção crônica. Na hepatite B crônica, os marcadores HBsAg e HBV-DNA permanecem presentes e detectáveis. A avaliação do HBeAg e anti-HBe, junto aos demais marcadores, auxilia no monitoramento e avaliação da fase clínica da infecção.48, 50
A testagem para hepatite B deve ser ofertada ou solicitada para todas as pessoas de maior vulnerabilidade ao agravo. Aquelas cujos resultados forem negativos devem ser encaminhadas para vacinação.16, 44
Na infecção pelo HCV a maioria das pessoas infectadas é assintomática e o rastreamento é feito pela detecção de anticorpos anti-HCV utilizando teste de imunoensaio ou teste rápido. Nas pessoas com resultados reagentes, a complementação do diagnóstico é feita por teste molecular, no caso, a reação em cadeia da polimerase mediada por transcrição reversa (reverse transcriptase-polymerase chain reaction, RT-PCR) para detectar o RNA do HCV, confirmando a infecção ativa, aguda ou crônica. A testagem para hepatite C deve ser solicitada para todos os indivíduos em situações de risco para a infecção.12, 52
Tratamento
Não está disponível tratamento antiviral específico para a hepatite A, apenas medicamentos para alívio dos sintomas, os quais geralmente desaparecem dentro de dois meses.53
Durante a infecção aguda pelo HBV, apenas medidas de suporte são suficientes, visto que mais de 90% apresentam resolução espontânea. Se houver necessidade de tratamento, utilizam-se os inibidores de transcriptase reversa.54 No Brasil, a escolha é o fumarato de tenofovir desoproxila ou o entecavir.37 Medidas preventivas devem ser tomadas para todos os contatos expostos, indicando-se imunoglobulina e vacinação para aqueles soronegativos ou com sorologia desconhecida, segundo critérios estabelecidos.55
Após seis meses de persistência do HBsAg no sangue, a infecção pelo HBV é considerada crônica e deve ser avaliada clínica e virologicamente para decisão sobre necessidade de terapia medicamentosa. O tratamento da forma crônica da hepatite B tem como principal objetivo a supressão viral, evitando, com isso, a progressão da hepatopatia e o óbito. A negativação do HBsAg e soroconversão para o antiHBs (cura funcional) seria o resultado ideal, mas raramente alcançado. Não cumprindo esse objetivo, o aparecimento do anti-HBe, a redução da carga viral e a normalização das enzimas hepáticas passam a ser os desfechos alternativos.37, 56
Devido à sua complexidade, esse tratamento deve ser instituído com orientação do especialista, visto que depende de múltiplas variáveis clínicas e laboratoriais, como a presença de acometimento hepático significativo, resposta imunológica à infecção, carga viral e fatores de risco para a progressão da doença (idade e histórico familiar de hepatocarcinoma).37, 55 A biopsia hepática pode ser útil para avaliar o grau de agressão tecidual e para os casos em que seja necessário descartar doença hepática de base.57 A definição de terapia antiviral na infecção crônica pelo HBV depende, a princípio, do grau da hepatopatia, da concentração de aminotransferases e da carga viral (HBV-DNA).58
Objetivamente, a infecção pelo HCV pode ser curada utilizando-se tratamento antiviral de ação direta. Entretanto, por ser uma infecção assintomática na maioria dos casos, grande número de pessoas infectadas não são diagnosticadas e ainda existe limitação de acesso à terapia em alguns locais.52 Esse tratamento deve ser acompanhado por especialistas, visto sua complexidade.
As alternativas terapêuticas para o tratamento da infecção pelo HCV incorporadas ao SUS apresentam elevada efetividade terapêutica, confirmada por resposta virológica sustentada (Figura 3). Comparando-se situações clínicas semelhantes, todos os esquemas propostos apresentam efetividades também similares. Características que os diferenciam são as indicações para determinadas populações, a comodidade posológica, o controle mais acessível e o custo. A terapia tem como objetivo a resposta virológica sustentada, que significa negativação persistente do RNA viral após 12 a 24 semanas do término do tratamento.41
Figura 3 Principais fármacos e associações mais frequentes para o tratamento da hepatite C
| Principais fármacos e associações mais frequentes para o tratamento da hepatite C |
|---|
| Sofosbuvir + daclatasvir |
| Sofosbuvir/ledipasvir |
| Sofosbuvir/velpatasvir |
| Elbasvir/grazoprevir |
| Glecaprevir/pibrentasvir |
| Ribavirina |
Fonte: adaptado do Protocolo Clínico e Diretrizes Terapêuticas para Hepatite C e Coinfecções.41
Vigilância, prevenção e controle
A notificação dos casos de hepatites virais é compulsória para todos os estados do país desde 2016. Todos os casos suspeitos também devem ser comunicados semanalmente às autoridades de saúde.59
A prevenção da infecção pelo HAV depende da melhoria das condições sanitárias da população e da realização da vacinação (crianças até os 5 anos de idade e pessoas expostas a maior risco da infecção), segundo os critérios do Centro de Referência para Imunobiológicos Especiais.56 No entanto, em adultos, deve ser considerada também a transmissão sexual, indicando e incentivando práticas sexuais seguras.12 No caso de exposição de risco para a hepatite A, há indicação de testagem e as pessoas negativas podem ser vacinadas até 14 dias após a exposição.29
Para o controle da infecção pelo HBV, a melhor estratégia é a vacinação, que apresenta elevados percentuais de efetividade, os quais variam de acordo com a idade (crianças pré-termo e pessoas acima de 60 anos apresentam menores percentuais de viragem sorológica) e a presença de comorbidades, a exemplo de pessoas em hemodiálise, pessoas com hepatopatias, neoplasias e aquelas portadoras do HIV.33, 56, 60-62
O fato de que 90% das infecções pelo HBV adquiridas no período perinatal evoluem para a cronicidade fundamentam as estratégias de vacinação universal de todos os recém-nascidos, independentemente de a mãe ser portadora crônica do vírus.56, 60Essa estratégia é fundamental para cumprir o objetivo de controlar a hepatite B até o ano 2030.6, 63
As orientações e cuidados com as pessoas usuárias de drogas ilícitas e aquelas que praticam atividade sexual sem proteção adequada são as estratégias que potencialmente podem trazer melhores resultados na redução das infecções pelo HCV.6, 21-24Outra forma de controle da infecção pelo HCV é a terapia antiviral de ação direta contra o vírus, cujo sucesso ampliou a discussão sobre o tratamento como estratégia para prevenção da doença.64
Populações e situações especiais
A abordagem das hepatites causadas pelos vírus HAV, HBV e HCV durante a gravidez exige atenção sobre os aspectos profiláticos envolvidos tanto na transmissão horizontal quanto na transmissão vertical desses vírus. Para a redução e controle de exposições de risco, são necessários os fundamentos comportamentais e sanitários da profilaxia primária, acrescidos dos recursos da imunoprofilaxia ativa e passiva, quando existentes.65, 66Sabe-se que o controle da transmissão vertical do HBV e do HCV depende da triagem universal dessas infecções durante o pré-natal. De forma geral, durante o pré-natal é importante identificar se os parceiros das gestantes não infectadas são portadores dessas infecções, o que permite a adoção de estratégias que reduzem as infecções agudas durante a gravidez, a exemplo da inclusão do parceiro na assistência pré-natal.67
Hepatite A na gestação
O período curto de viremia e os cuidados durante o parto (evitando o contato do feto com fezes maternas) justificam a raridade da transmissão vertical do HAV.68 O parto vaginal é o mais indicado para essas mulheres e a amamentação natural é liberada.69
Tanto a imunoglobulina quanto a vacina contra o HAV são seguras para uso durante a gravidez. Em caso de exposição a fatores de risco clínicos, ocupacionais e de estilo de vida, além de viagens para áreas de elevada prevalência, a imunoprofilaxia pode ser utilizada.12, 70
Hepatite B na gestação
As proporções de cronicidade da infecção pelo HBV são mais elevadas quanto mais precocemente ocorrer a infecção.71 Por isso, o controle da transmissão vertical potencialmente reduz a ocorrência de hepatite crônica, cirrose e hepatocarcinoma.72, 73
Orienta-se a pesquisa do HBsAg na primeira oportunidade no pré-natal e sua repetição no momento do parto.74 Para gestantes soronegativas, deve-se iniciar o esquema vacinal de três doses. A informação vacinal não exclui a necessidade de verificar se a gestante é portadora do HBV em todos esses momentos, pois não há certeza de viragem sorológica vacinal mesmo após as três doses da vacina.75
Com função hepática normal o prognóstico da infecção pelo HBV não é modificado pela gravidez e a infecção não altera o prognóstico gestacional.76, 77Em caso de comprometimento hepático, os prognósticos materno e perinatal poderão ser negativamente afetados.65
A ocorrência de transmissão vertical do HBV é influenciada pela carga viral, pela positividade do HBeAg e do anti-HBe da portadora e pela idade gestacional (infecção adquirida no fim da gestação aumenta o risco de alta carga viral na hora do parto). Sem nenhuma intervenção profilática, o risco de transmissão vertical em portadoras crônicas varia de 5% a 30% (média de 8%). No entanto, se a gestante for portadora do HBeAg, a proporção de transmissão vertical é elevada, mas extremamente variável, ocorrendo em 80% a 90% das vezes.4, 33, 65
Durante o pré-natal de gestantes portadoras crônicas do HBV, estão contraindicadas todas as condutas invasivas sobre o feto e câmara amniótica (amniocentese e cordocentese). Havendo exposição de risco, está indicada a imunoprofilaxia, utilizando, em grupos musculares diferentes, a primeira dose da vacina e imunoglobulina hiperimune anti-hepatite B (0,06mL/kg de peso corporal, máximo de 5mL, intramuscular).56, 74, 78
Além da rotina laboratorial usual, devem ser solicitados os seguintes exames para gestantes portadoras do HBV: provas de função hepática, marcadores da infecção ainda não solicitados (entre eles HBeAg, anti-HBc, anti-HBe, anti-HBs) e carga viral. Todas as gestantes que apresentam carga viral do HBV superior a 200.000UI/mL (correspondentes a 1 milhão de cópias/mL) ou positividade para HBeAg devem fazer profilaxia da transmissão vertical. Alterações da função hepática indicam necessidade de tratamento de longo prazo e não apenas profilaxia (Figura 4).63
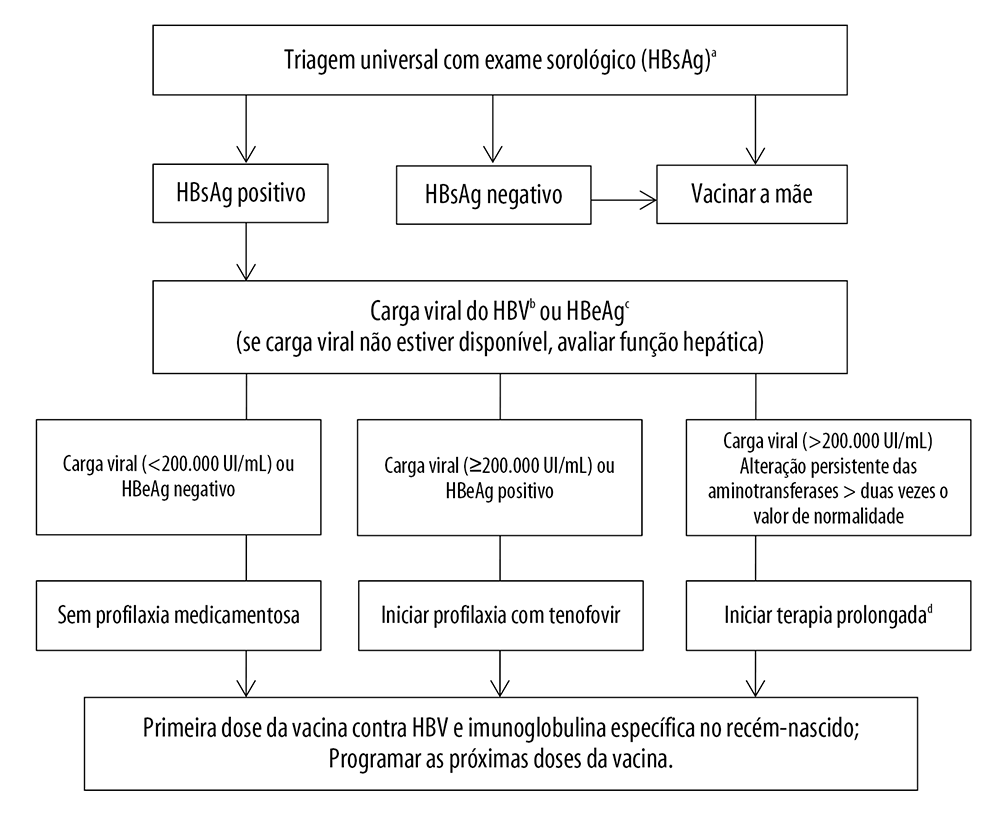
Fonte: modificado e adaptado de World Health Organization, 2020.71
Notas: a) HBsAg - antígeno de superfície do HBV; b) HBV - vírus da hepatite B; c) HBeAg - antígeno “e” do HBV; d) Iniciar terapia prolongada com fumarato de tenofovir desoproxila, pois entecavir não é seguro para lactante.80, 81
Figura 4 Algoritmo das intervenções preventivas para prevenção da transmissão vertical do vírus da hepatite B
Para a profilaxia da transmissão vertical do HBV, está indicado o uso de antivirais inibidores nucleosídicos da transcriptase reversa (lamivudina, tenofovir e telbivudina).63, 79No Brasil, a opção é o fumarato de tenofovir desoproxila (300mg, via oral, dose única diária), iniciado a partir da 28ª semana de gravidez, prolongando-se no puerpério para evitar eventual aumento da carga viral.74 Considerando a necessidade de tratamento prolongado em gestantes portadoras do HBV, também se utiliza o fumarato de tenofovir desproxila. Até o momento, considera-se que o uso do entecavir durante a gravidez não é seguro, devendo ser evitado nesse período.80 Da mesma forma, também não está indicado para ser usado durante o período de amamentação.81
O parto vaginal é liberado para mulheres portadoras do HBV, evitando-se episiotomia e partos instrumentalizados (fórceps ou vácuo) e clampeando rapidamente o cordão umbilical. A amamentação natural também está liberada.82
Todos os recém-nascidos de mulheres portadoras do HBV deverão receber a primeira dose da vacina e a imunoglobulina específica contra o HBV (0,5mL intra-muscular), de preferência nas primeiras 12 horas de vida, conforme apresentado no algoritmo da Figura 4. Existem vários esquemas para a administração das doses adicionais da vacina, alguns com duas, outros com três doses adicionais.63 Países como China, Malásia e Hong Kong, entre outros, utilizam o calendário de duas doses adicionais administradas no segundo e sexto meses de vida do recém-nascido.83-85 Nos Estados Unidos da América e no Canadá, utiliza-se também o esquema de duas doses adicionais administradas no segundo e sexto meses de vida. No entanto, se o recém-nascido for pré-termo ou com peso abaixo de 2,0kg, o esquema vacinal considera três doses adicionais da vacina, administradas no segundo, quarto e sexto meses de vida.75, 86No Brasil, o Programa Nacional de Imunizações indica esquema vacinal de três doses adicionais à dose administrada no momento do parto, utilizando vacinas combinadas (vacina pentavalente) administradas no segundo, quarto e sexto meses de vida, independentemente de prematuridade ou peso do neonato.74, 87
Seja qual for o esquema vacinal utilizado, a situação do recém-nascido deve ser acompanhada até se definir se a infecção foi confirmada ou descartada e a soroconversão aferida.71 No Brasil, indica-se essa avaliação entre 30 e 60 dias após a última dose da vacina anti-HBV.74
Hepatite C na gestação
Em 2020, o Ministério da Saúde incorporou a triagem universal da infecção pelo HCV durante a gravidez.88 A grande resistência à triagem pré-natal do HCV é que não existe profilaxia farmacológica ou imune para reduzir sua transmissão vertical.4 No entanto, existem estratégias comportamentais e assistenciais que reduzem esse risco, como realizar o controle profilático e terapêutico de outras infecções, proibir propedêutica invasiva sobre a câmara amniótica ou fetal e evitar tempo prolongado de corioamniorrexe. Durante o parto deve-se evitar o uso da episiotomia, indicando-se o clampeamento rápido do cordão umbilical.65, 89, 90Além disso, é mais uma oportunidade de identificar portadores do HCV, que podem se beneficiar do tratamento posteriormente.
A transmissão vertical do HCV ocorre entre 3,8% e 7,8% das gestantes com infecção crônica, mostrando associação positiva com a carga viral.91-93Essas proporções de transmissão vertical variam também a depender da idade gestacional em que ocorreu a infecção aguda e da presença de comorbidades, a exemplo da infecção pelo HIV.94, 95Não existe confirmação de que o HCV possa causar malformação fetal.96
Tem sido observado que a infecção pelo HCV em gestantes associa-se com prognósticos perinatais adversos, como restrição de crescimento fetal e prematuridade.97, 98Não parece que esses resultados sejam decorrentes apenas do efeito do HCV, mas também dos inúmeros fatores que coexistem nessas gestantes.94 Independentemente de ação isolada ou em associação, o que se confirma é a necessidade de identificar as gestantes portadoras dessa infecção e indicar assistência pré-natal apropriada e seguimento adequado a seus filhos.88, 99Tanto o parto vaginal quanto a amamentação natural estão liberadas para mulheres portadoras do HCV66, 79desde que não haja concomitância com a infecção pelo HIV.100











 texto em
texto em 


