INTRODUÇÃO
A febre maculosa é uma doença febril aguda causada por riquétsias, bactérias intracelulares obrigatórias, transmitidas principalmente por carrapatos1. No Brasil, Rickettsia rickettsii é a espécie mais relevante, apresentando casos graves na Região Sudeste2,3 e, mais recentemente, na Região Sul3. A doença pode evoluir de forma rápida, com um comprometimento clínico importante, apresentando elevado coeficiente de letalidade, sendo, por isso, agravo de notificação compulsória4. Amblyomma sculptum e Amblyomma aureolatum são incriminados em sua transmissão3.
Entretanto, casos mais brandos de febre maculosa foram identificados nas Regiões Sul, Sudeste e Nordeste do País5,6,7, apresentando linfadenopatia e escara de inoculação como manifestações clínicas relevantes. A doença pode estar associada à Rickettsia sp. cepa Mata Atlântica, espécie filogeneticamente próxima a Rickettsia parkeri6,7 e tendo como vetor envolvido no ciclo epidêmico Amblyomma ovale3,5,8,9.
Em uma abordagem de investigação dos ambientes com potencial risco para a presença da febre maculosa, o Ministério da Saúde promoveu capacitações técnicas aos profissionais da rede do Sistema Único de Saúde, priorizando inicialmente as áreas endêmicas da doença10. Paralelamente aos treinamentos, materiais instrucionais no formato de videoaulas foram produzidos e disponibilizados, abordando os aspectos da vigilância epidemiológica e ambiental10,11,12. Essa iniciativa é parte de um processo que tem como objetivo qualificar e habilitar equipes para realizar investigações de ambientes, e essas ações buscam apoiar os programas municipais e estaduais de vigilância das doenças transmitidas por carrapatos10.
Contudo, tem-se observado baixa frequência de suspeição clínica e epidemiológica de casos na Região Norte e parte das Regiões Nordeste e Centro-Oeste, consideradas áreas silenciosas para a doença4,10,13. Nessas áreas o conhecimento sobre a história natural e da distribuição de riquetsioses de interesse médico ainda é incipiente2.
O presente estudo descreveu um conjunto de iniciativas promovidas pelo Ministério da Saúde a fim de intensificar a vigilância ambiental e epidemiológica, bem como aprimorar o conhecimento sobre as áreas consideradas silenciosas para a febre maculosa no Brasil.
MATERIAIS E MÉTODOS
O estudo foi realizado de 2014 a 2015 e iniciado com o convite a todos os Estados do Brasil que, até 2013, não haviam informado casos confirmados de febre maculosa. Os Estados do Mato Grosso do Sul (MS), na Região Centro-Oeste; Alagoas (AL), Pernambuco (PE), Rio Grande do Norte (RN) e Maranhão (MA), na Região Nordeste; e Rondônia (RO) e Roraima (RR), na Região Norte, foram incorporados ao projeto, após manifestação de interesse.
CAPACITAÇÕES EM ÁREAS SILENCIOSAS
Foram realizadas capacitações técnicas em investigações de casos e vigilância de ambientes da febre maculosa em áreas consideradas silenciosas para presença da doença. O programa buscou tratar da epidemiologia das doenças transmitidas por carrapatos, das rotinas de encaminhamento de materiais biológicos para análise laboratorial, das atividades práticas de campo e de laboratório e do uso adequado de equipamentos de proteção individual e coletiva10,11,12.
INVESTIGAÇÃO DA FAUNA DE VETORES E DE HOSPEDEIROS
Foram realizadas coletas de carrapatos no ambiente e em hospedeiros. Os carrapatos foram coletados com auxílio da técnica de arrasto, armadilha de CO2 ou pela busca ativa, diretamente nos hospedeiros e no ambiente12. A prioridade foi dada para investigar as áreas urbanas e periféricas, onde havia o conhecimento prévio da densidade de vetores com consequente parasitismo humano. Essas áreas incluíram áreas públicas ou privadas, como parques, canis, haras, fazendas de universidades, abrigos de animais domésticos e silvestres12.
As amostras coletadas seguiram o fluxo da Rede Nacional de Vigilância de Ambiente para Febre Maculosa e Outras Riquetsioses, implementada pelo Ministério da Saúde durante as capacitações na investigação de casos e vigilância de ambiente para febre maculosa das áreas com casos confirmados10,11,12. Os carrapatos foram analisados e identificados de acordo com as chaves dicotômicas14.
Na investigação molecular dos bioagentes transmitidos por carrapatos, os vetores foram submetidos à extração de DNA e quantificação de DNA extraído, individualmente ou em pool. Foram utilizados primers gênero-específicos (gltA) para identificação de Rickettsia spp. e primers grupo-específico, para identificação de riquétsias do grupo da febre maculosa (RGFM) (ompA)15,16. As análises foram realizadas no Laboratório de Referência Nacional para Vetores de Riquetsioses na Fundação Oswaldo Cruz no Estado do Rio de Janeiro.
ANÁLISE DE DADOS EPIDEMIOLÓGICOS
Dados epidemiológicos dos respectivos Estados foram analisados utilizando, como base, os registros das fichas de notificação e investigação de febre maculosa inseridas no Sistema de Informação de Agravo de Notificação durante o período de 2014 a 2015. Foram considerados como caso suspeito: indivíduo que apresentou febre, cefaleia, mialgia e história de picada de carrapatos e/ou contato com animais domésticos e/ou silvestres e/ou frequentou área sabidamente de transmissão de febre maculosa nos últimos 15 dias e/ou apresente exantema maculopapular ou manifestações hemorrágicas11. E como caso confirmado: indivíduo suspeito com diagnóstico laboratorial, sorológico ou molecular confirmatório11. Registros que não se enquadraram na definição de caso, proposta pelo MS, foram excluídos da análise11. As variáveis foram analisadas de acordo com a classificação do município de notificação (local onde foi notificado o caso suspeito) e do município da infecção (local onde foi comprovada, por meio de investigação epidemiológica, a autoctonia do caso ao município)4,13. Os dados foram apresentados por números brutos e frequências. Foram utilizados os softwares TabWin 32 v3.6b para tabulação de dados; Microsoft Office Excel 2010 para produção de planilhas e gráficos; e TerraView v3.2.0.1 para elaboração de mapas4,13.
ASPECTOS ÉTICOS
Por se tratar de uma estratégia do serviço de vigilância em saúde, o presente estudo não foi submetido previamente a um comitê de ética em pesquisa. No entanto, obedeceu aos preceitos éticos estabelecidos na Resolução n° 466/2012 do Conselho Nacional de Saúde, não abrangendo dados que pudessem identificar os indivíduos registrados no sistema de informação. A coleta de vetores em animais silvestres foi autorizada pela licença do Instituto Brasileiro de Meio Ambiente, processo nº 02001.000812/2013-01 nº 003. A contenção e manuseio de animais domésticos seguiram as normas estabelecidas pelo Conselho Federal de Medicina Veterinária.
RESULTADOS
CAPACITAÇÕES EM ÁREAS SILENCIOSAS
Foram capacitados 161 profissionais: MS = 29; AL = 18; PE = 10; RO = 18; RR = 19; RN = 29; e MA = 38. As sete capacitações realizadas tiveram representantes de 56 municípios (Figura 1). Quanto ao perfil de escolaridade dos treinandos, 64,4% possuíam nível superior, sendo que 7,6% tinham mestrado e 0,8% doutorado; 22,7% possuíam nível médio, 2,3% nível fundamental e 2,3% não informaram seu nível de escolaridade. Quanto à formação profissional, 28,79% eram biólogos, 21,97% veterinários, 21,97% tinham outras formações superiores ou técnicas e 27,27% não informaram sua formação acadêmica.

Figura 1 -Distribuição dos municípios brasileiros e das Unidades Federadas com profissionais capacitados para proposta de estruturação da Rede Nacional de Vigilância de Ambientes para Febre Maculosa e Outras Riquetsioses no Brasil
Quanto à ocupação/função, 52,42% eram responsáveis técnicos, 20,16% eram técnicos em entomologia, 12,90% eram agentes de controle de endemias e de vigilância em saúde, 8,87% eram agentes em saúde pública, 2,42% eram técnicos em enfermagem e 3,23% eram estagiários, estudantes, sanitaristas ou técnicos em saneamento.
INVESTIGAÇÕES DA FAUNA DE VETORES E DE HOSPEDEIROS
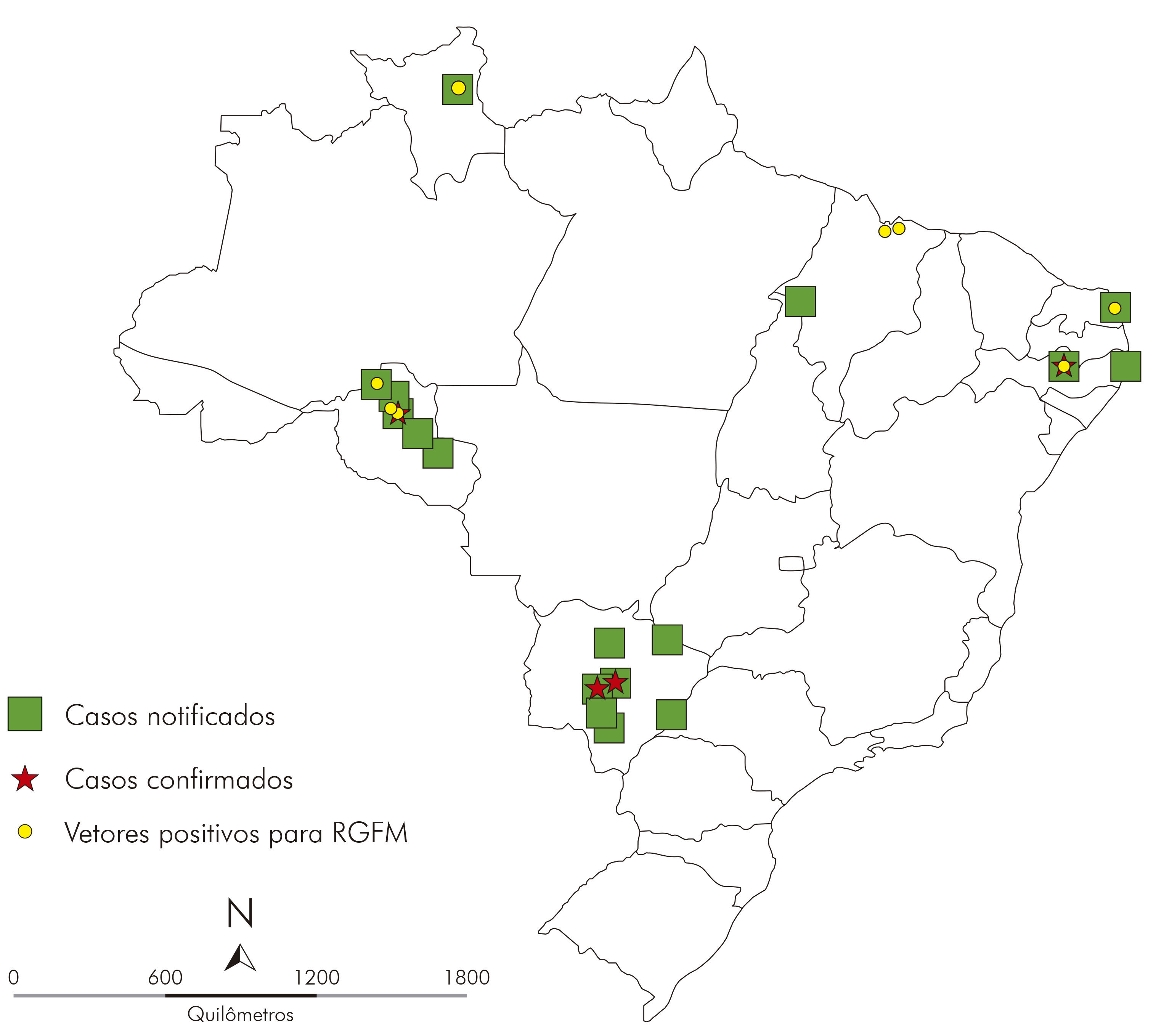
Foram coletados 1.528 potenciais vetores nas áreas investigadas em múltiplos hospedeiros e ambientes (Tabela 1). A positividade para RGFM foi observada em PE, RO, RR, RN e MA (Figura 2). O Estado de Alagoas foi capacitado, mas não enviou amostras dentro do fluxo da Rede Nacional de Vigilância de Ambiente para Febre Maculosa e Outras Riquetsioses e, desta forma, não foi possível analisar a fauna de vetores desse Estado.
Tabela 1 - Espécies de potenciais vetores coletados em áreas silenciosas do Brasil (2014/2015), durante o período de treinamento para vigilância de ambiente e investigação de casos para febre maculosa, segundo cada Unidade Federada capacitada
| Espécie de potencial vetor | Unidades Federadas | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MS | PE | RO | RR | RN | MA | |||||||||||||
| N | Hosp | % | N | Hosp | % | N | Hosp | % | N | Hosp | % | N | Hosp | % | N | Hosp | % | |
| Carrapatos | ||||||||||||||||||
| Amblyomma cajennense | - | - | - | - | - | - | 22 | A | - | 13 | A | 50,0 | - | - | - | - | - | - |
| Amblyomma naponense | - | - | - | - | - | - | 3 | A | - | - | - | - | - | - | - | - | - | - |
| Amblyomma scalpturatum | - | - | - | - | - | - | 1 | A | - | - | - | - | - | - | - | - | - | - |
| Amblyomma pseudoconcolor | - | - | - | 20 | T | 90,9 | - | - | - | - | - | - | - | - | - | - | - | - |
| Dermacentor nitens | - | - | - | - | - | - | 177 | E | 0,8 | 63 | E | - | 176 | E/B | - | 14 | E | 2,7 |
| Rhipicephalus sanguineus | 108 | A/C | - | 23 | C | - | 117 | A/C | 1,5 | 238 | A/C/E | 1,7 | 208 | A/C/B | - | 183 | A/C | 2,7 |
| Rhipicephalus microplus | 2 | B | - | - | - | - | 41 | B/E | 9,0 | 10 | B | 16,6 | 72 | E/B | 5,8 | - | - | - |
| Pulgas | ||||||||||||||||||
| Ctenocephalides felis | 2 | G | - | - | - | - | 10 | C | 100,0 | 3 | C | - | 17 | C | - | - | - | - |
| Xenopsylla cheopis | - | - | - | - | - | - | 2 | A | - | - | - | - | - | - | - | - | - | - |
| Ácaro | ||||||||||||||||||
| Tur turki | - | - | - | - | - | - | 3 | R | - | - | - | - | - | - | - | - | - | - |
Fonte: Grupo Febre Maculosa (RGFM).
N: número de espécimes coletados; Hosp: local de coleta (A - ambiente, B - boi, C - cão, E - equinos, G - gato, R - rato, T - tatu); %: percentual de positividade para riquétsia. Sinal convencional utilizado: - Dado numérico igual a zero não resultante de arredondamento.
ANÁLISE DE DADOS EPIDEMIOLÓGICOS
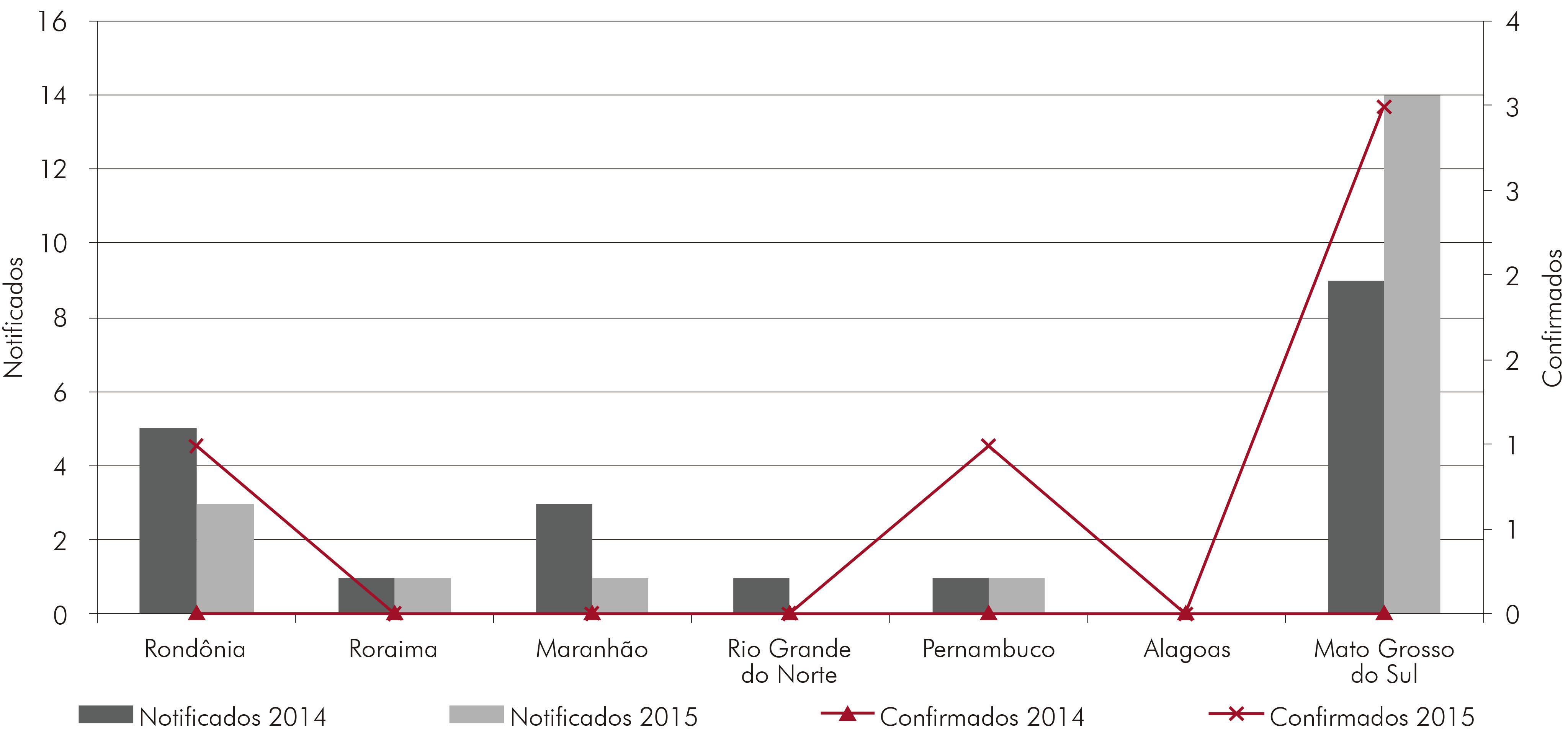
Foram registradas 40 notificações de casos suspeitos de febre maculosa nas áreas silenciosas investigadas no respectivo período. O MS concentrou o maior volume de notificações, 57,5% (23/40). Foram confirmados cinco casos de febre maculosa nos seguintes Estados: MS, 60% (3/5); RO, 20% (1/5); e PE, 20% (1/5) (Figura 3). Nos Municípios de Campo Grande (2) e Dois Irmãos do Buriti em MS (1), Ariquemes em RO (1) e Sertânia em PE (1) houve confirmação de caso (Figura 2).
DISCUSSÃO
Com a iniciativa de intensificar a vigilância e explorar as áreas consideradas silenciosas para a presença da febre maculosa no Brasil, foi possível identificar a frequência de RGFM em 85% das Unidades Federadas que foram treinadas, sejam em vetores ou em humanos. No período em que ocorreram as intervenções, foram registrados os primeiros casos humanos de febre maculosa nos Estados de MS, RO e PE.
Os resultados das intervenções chamam a atenção para subnotificação de casos em áreas das Regiões Centro-Oeste, Norte e Nordeste do Brasil. Os casos de febre maculosa, mesmo em áreas reconhecidamente endêmicas, ocorrem em baixa incidência e com clínica inespecífica4,13, provavelmente esses são os principais fatores que dificultam o diagnóstico clínico em áreas onde a presença da doença ainda não foi assinalada. O exantema, principal sinal clínico da doença, nem sempre está presente11,12 e, em indivíduos de pele escura, quando presente, dificilmente é visualizado17.
Em áreas ermas do Brasil, o parasitismo por carrapatos é evento do cotidiano das populações, o que torna ainda mais difícil fazer o vínculo epidemiológico entre a exposição ao vetor e o desfecho (suspeita clínica da doença)18,19,20. Aliado a esses fatores, existem parasitoses e arboviroses mais incidentes (malária, febre amarela, dengue, Zika e Chikungunya) que acometem as populações dessas áreas e que consomem quase toda a capacidade de resposta dos serviços de saúde dessas regiões21. Nesse sentido, a proposta de instituir a vigilância da febre maculosa em áreas silenciosas buscou otimizar atividades rotineiras de vigilância em saúde de outros programas, incluindo a febre maculosa entre o escopo das doenças sob a vigilância efetiva nessas áreas. Também foram discutidas formas de fazer uso oportuno da riqueza de informações biológicas (amostras) e ecoepidemiológicas, disponíveis de outros programas de vigilância em saúde e de outras instituições públicas, como currais municipais, abrigos de animais, centros de triagem de animais silvestres ou mesmo de instituições parceiras.
Recentemente, novas espécies de riquétsias foram identificadas em vetores no Brasil, como R. parkeri, Rickettsia sp. Mata Atlântica, Rickettsia amblyommii, Rickettsia andeanae e Rickettsia monteiroi3,8, muitas da quais a patogenicidade ainda é desconhecida. Por outro lado, algumas riquétsias transmitidas por carrapatos, como Rickettsia sp. Mata Atlântica, causam quadros clínicos mais brandos, o que poderia estar dificultando a captação destes registros e avaliação da real magnitude da febre maculosa em áreas silenciosas. Dessa forma, investigações que busquem caracterizar os agentes etiológicos que acometem as populações humanas nessas regiões são fundamentais para a compreensão da doença.
A amplitude geográfica e a vasta biodiversidade dessas regiões tornam estas áreas como campo prioritário nas investigações das potenciais doenças transmitidas por carrapatos. Igualmente, a caracterização molecular de RGFM é imprescindível para melhor entendimento do potencial patogênico das riquétsias detectadas em uma área, bem como para avaliar a vulnerabilidade para o potencial estabelecimento do ciclo epidêmico22.
A positividade de RGFM, em vetores associados à investigação de casos humanos, chama atenção para um ciclo silvestre de riquétsias, cujo potencial patogênico ainda precisa ser esclarecido8,23. Também destaca-se a presença de RGFM em Rhipicephalus sanguineus e Ctenocephalides felis, vetores cujo potencial transmissor no Brasil ainda é dúbio, mas com evidências na manutenção de RGFM em ciclos enzoóticos24,25.
O processo da formação da Rede Nacional de Vigilância de Ambientes para Febre Maculosa e Outras Riquetsioses9 tem possibilitado a oportunidade das intervenções, além da uniformização de métodos de investigação e vigilância epidemiológica (predição e prevenção) com frequente resposta na detecção de casos, visando a redução da morbimortalidade, objetivos prioritários do sistema de vigilância da febre maculosa no Brasil.
CONCLUSÃO
Conclui-se que a febre maculosa está presente em áreas consideradas silenciosas para a doença no Brasil. As intervenções, no âmbito da vigilância epidemiológica e ambiental, possibilitaram a detecção de riquétsias em vetores e a confirmação dos primeiros casos humanos da doença nos Estados do MS, RO e PE. Os resultados das intervenções realizadas no âmbito das qualificações técnicas mostraram a importância dessas iniciativas, tendo em vista que muitas doenças não são registradas pelo Sistema Único de Saúde devido ao desconhecimento da epidemiologia por parte dos profissionais de saúde. A febre maculosa causa doença grave na Região Sudeste do Brasil e, por isso, o conhecimento de sua distribuição em áreas consideradas silenciosas é importante para o desencadeamento de estratégias de prevenção e controle.











 texto em
texto em 
 Curriculum ScienTI
Curriculum ScienTI