Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Informe Epidemiológico do Sus
versão impressa ISSN 0104-1673
Inf. Epidemiol. Sus v.9 n.1 Brasília mar. 2000
http://dx.doi.org/10.5123/S0104-16732000000100002
Laboratórios sentinelas - uma proposta para o monitoramento das infecções pelos vírus das hepatites A e B
Sentinel laboratories - a proposal for monitoring viral A and B hepatitis infections
Rosangela GazeI; Diana Maul de CarvalhoI; Ronir Raggio LuizI; Valéria Regina Ramalho ServinoII; Oscar Jorge BerroIII; Yolanda BravimIII
IUniversidade Federal do Rio de Janeiro
IIInstituto de Medicina Nuclear de Macaé
IIISecretaria de Estado de Saúde do Rio de Janeiro/Laboratório Central Noel Nutels
RESUMO
Considerando que as hepatites virais (HV) são representativas da categoria de infecções freqüentemente assintomáticas, propõe-se a utilização de um sistema de laboratórios sentinelas (SLS) como método de monitoramento das infecções pelos vírus das hepatites A (VHA) e B (VHB), através da pesquisa de marcadores virais em material sorológico excedente coletado por outros motivos. Por intermédio de revisão bibliográfica e de avaliação da aplicabilidade da estratégia de laboratórios sentinelas no acompanhamento da tendência destas infecções, desenvolvem-se as bases técnicas para um SLS, discutem-se suas potencialidades e limitações, sua importância na complementação das informações da Vigilância Epidemiológica (VE) das hepatites virais e os instrumentos para criteriosa avaliação do sistema, possibilitando correções e redirecionamentos. Suas principais vantagens sobre o sistema de VE passivo são a simplicidade, melhor qualidade das informações e maior abrangência, gerando aceitabilidade e efetividade. De menor custo que os inquéritos de soroprevalência, um SLS apresenta sensibilidade adequada para o monitoramento do VHA e VHB e possibilita o gerenciamento de programas de prevenção.
Palavras-Chave: Hepatites Virais; Vigilância Epidemiológica; Laboratório Sentinela; Amostras Excedentes de Soro.
SUMMARY
Viral hepatitis (VH) is representative of a category of infections with a significant fraction of asymptomatic cases. In this paper, the use of a system of sentinel laboratories (SSL) in the monitoring of infections for hepatitis A (HAV) and hepatitis B viruses (HBV) is considered, arguing the importance of complementing the information of Epidemiological Surveillance (ES) and the development of the technical bases of this system, its potential, limitations and evaluation criteria. Through bibliographical review and evaluation of the applicability of the laboratory sentinel technique to follow the trend of these infections, we consider the use of exceeding serologic material, collected for other reasons, for the research of viral markers with the aim of supplementing the information of the ES for prevention programs. The main advantages of this system over the passive system of ES, are a better quality of information, increased simplicity, and enhanced effectiveness and acceptability. It is less costly than serumprevalence surveys,and provides good sensitivity for the monitoring of HAV and HBV.
Key Words: Viral Hepatitis; Epidemiologic Surveillance; Sentinel Laboratory; Exceeding Serum Samples.
Introdução
Os indicadores de saúde de uso corrente, baseados em dados de mortalidade, mostram-se menos sensíveis para evidenciar situações onde a morbidade se mantém elevada, mas os óbitos são evitados por ações sobre os efeitos das doenças. Por exemplo, no caso das diarréias, a mortalidade foi reduzida graças aos esforços dos programas de reidratação oral, mas o mesmo impacto não foi obtido sobre a incidência, visto que mudanças estruturais, como as relativas ao saneamento, foram insuficientes.1 Um novo desafio se apresenta à medida que os avanços científico-tecnológicos e o aumento da cobertura dos serviços de saúde vêm permitindo alcançar a redução nos coeficientes de mortalidade. Apesar das dificuldades e limitações, a importante carga da morbidade, em especial nos países em desenvolvimento, deve suscitar estratégias que permitam acompanhar e avaliar sua dinâmica ao longo do tempo.2
Atualmente, o monitoramento das condições de saúde torna necessária a busca de indicadores capazes de dar respostas à pergunta acerca do que adoecem as pessoas tão bem quanto sobre de que elas morrem. E, em alguns casos, outra questão se coloca: Qual a importância e magnitude de doenças que apresentam significativa proporção de casos sem exteriorização clínica, ou nas quais esta só ocorre na fase crônica?
Considerando que as hepatites virais (HV) são representativas dessa categoria, discute-se a proposta de um sistema de laboratórios sentinelas (SLS) para as infecções pelos vírus das hepatites A (VHA) e B (VHB), demonstrando sua importância na complementação das informações da Vigilância Epidemiológica (VE) e sua aplicabilidade no monitoramento destas infecções. Desenvolvem-se as bases técnicas deste sistema, suas potencialidades e limitações, apresentando-se critérios para avaliação.
Metodologia
Através de revisão bibliográfica, identificaram-se alternativas efetivas, simples e de baixo custo para complementar e aperfeiçoar a VE das HV. Um estudo de soroprevalência do VHA e do VHB, em que a estratégia de laboratório sentinela foi empregada, foi avaliado tendo em vista sua aplicabilidade no acompanhamento da tendência destas infecções. E, por último, desenvolveram-se critérios para avaliação do sistema.
A escassez de estudos de soroprevalência do VHA e VHB que utilizassem amostras de soros de laboratórios de análises clínicas orientou a inclusão de outras infecções, como a do HIV, nesta revisão.
Foram utilizados textos que discutissem conceitos, princípios, organização, aplicabilidade, críticas/refutações e limitações de um sistema de vigilância sentinela (SVS) e os referentes à avaliação de redes sentinelas existentes no Brasil e em outros países. As publicações foram avaliadas na íntegra e procedeu-se à seleção sistemática de obras de interesse, a partir das suas referências bibliográficas.
A aplicação de um SLS no monitoramento da tendência das infecções por VHA e VHB e sua potencialidade na detecção de gradientes de variação de parâmetros obtidos ilustrada através da discussão de resultados de pesquisa de soroprevalência dessas infecções em amostras excedentes de soro de laboratório de análises clínicas, em Macaé/RJ, e de outros estudos de soroprevalência.3
Os critérios de avaliação do Centers for Disease Control and Prevention foram utilizados para desenvolver um roteiro de avaliação do sistema proposto.4
Informações da VE acerca das Hepatites Virais A e B
Aspectos relevantes das hepatites virais para a Vigilância Epidemiológica
Embora sua denominação sugira tratar-se de doenças que acometem apenas o fígado, as hepatites virais são viroses sistêmicas que envolvem diversos órgãos e sistemas.5
Clinicamente, as HV podem se apresentar de forma assintomática ou sintomática e estar em qualquer das suas fases evolutivas: aguda, crônica, cirrose ou neoplasia. A hepatite A não evolui a cronicidade, enquanto a B pode ser encontrada em diversos destes momentos evolutivos. Durante a fase aguda, a hepatite A pode cursar de modo fulminante, com êxito letal, em 0,05% dos casos e a B em 0,2%.6
As HV se caracterizam por apresentar um elevado percentual de infecções inaparentes, podendo atingir 90% nos casos de hepatite A e 95% nos de B, na dependência da idade em que ocorram, sendo mais freqüentemente assintomáticas nas crianças menores de cinco anos.7,8
Quanto à hepatite A, sua alta endemicidade em países em desenvolvimento com exposição precoce a seu agente (atingindo crianças menores de dez anos), de forma freqüentemente assintomática e não diagnosticada, faz com que permaneça desconhecida pelo Sistema de Vigilância Epidemiológica (SVE). Contudo, estas crianças desempenham um importante papel na transmissão a suscetíveis, oriundos, muitas vezes, de outras regiões ou países e podem influenciar negativamente a indústria de turismo das áreas endêmicas.9 Desta forma, viajantes para áreas pouco desenvolvidas, com saneamento básico inadequado, são considerados alvos de vacinação contra a hepatite A.10
Por outro lado, a hepatite A, ao ocorrer em adultos, tende a apresentar maior gravidade e gerar demanda por internação.11 Este aspecto, aliado ao aumento da proporção de adultos suscetíveis em conseqüência da transição demográfico-epidemiológica enfrentada atualmente por estas regiões, leva ao incremento da carga desta doença em idades produtivas, acrescentando mais gasto com a saúde e influenciando o custo indireto do tempo de afastamento do trabalho.10
De modo similar, a HVB é uma hipótese diagnóstica pouco suspeitada, apesar das infecções subclínicas poderem evoluir a cronicidade, principalmente em idades precoces.8, 12 Acrescente-se a este, outro fator de peso no planejamento de atividades de VE: a letalidade relativamente baixa dos casos agudos, menos preocupante que a de outros agravos.8 Entretanto, a Organização Mundial da Saúde estima que 2 bilhões de pessoas tenham evidência de infecção passada ou atual pelo VHB e 350 milhões sejam portadoras crônicas, além de 1 milhão de indivíduos morrerem a cada ano em conseqüência de cirrose e câncer de fígado13. Entretanto, o método de codificação das causas de mortalidade pode levar a entendimentos diversos sobre a letalidade desta doença. Murray & Lopez referem: Por exemplo, mortes por câncer de fígado mesmo em um indivíduo sabidamente portador de hepatite B são ainda codificadas como câncer de fígado. Em contraste, na CID- 10, mortes por linfoma entre pessoas com HIV são codificadas como HIV e não como linfoma.14
Aliados a estes fatos, estão ainda o alto custo e a baixa eficácia da terapêutica atual de pacientes crônicos. Como puderam avaliar Moraes & Castillo, entre 1989 e 1992, o Brasil despendeu 16,5 milhões de dólares com internações de casos de hepatite aguda, cirrose e neoplasia hepáticas, 7.500,00 a 8.500,00 com cada tratamento de seis meses com Interferon® e 80 a 120 mil dólares com cada transplante hepático.15
A excepcional estabilidade e alta transmissibilidade do VHA contribuem para a difusão de epidemias de proporções alarmantes10 e o VHB oferece um risco de infecção por acidente com agulha de paciente positivo de 7 a 30%.16 Investir hoje na interrupção da cadeia de transmissão da hepatite B é contribuir para evitar o aumento projetado da carga da doença para o ano 2020, quando a cirrose e câncer de fígado poderão ascender, respectivamente, das 13a e 21a para as 12a e 13a posições na ordenação de causas de morte.17
Notificação das hepatites virais
Embora, em 1961, o Brasil já possuísse uma relação oficial de 45 doenças de notificação compulsória, revista e ampliada em diversas oportunidades, somente em 1996 as HV foram incluídas.18,19 Entretanto, em dezembro de 1998,20 foram excluídas desta relação, sob a alegação de pouco contribuírem para a VE, considerando os distintos significados dos tipos de HV quanto à epidemiologia e às ações de controle. Somente a hepatite B foi mantida devido à gravidade da doença e existência de medidas de controle eficazes em uso no país.20 Um ano depois, hepatite C retornou à lista nacional de notificação compulsória.21 Embora isto possa acarretar a desmobilização de um sistema ainda parcialmente implantado, se pode desconsiderar a validade dos argumentos apresentados.
No Brasil, os dados de notificação das HV, de 1996, mostram coeficientes de incidência de 1,0 caso por 100.000 habitantes de hepatite A, 0,81 de B, 9,6 de não especificadas e 11,62 no conjunto.22,23 Nos EUA, país com sub-registro também relevante, as taxas por 100.000 habitantes, em 1993, para as hepatites A, B, não especificadas e total, foram, respectivamente, de 9,39, 5,18, 0,24 e 16,68 casos.11,24 Embora a comparação entre estes coeficientes não possa ser diretamente efetuada, é útil observar a significativa diferença de ordem de grandeza: o coeficiente de incidência por 100.000 habitantes das HV (11,62) no Brasil é 1,4 vezes inferior ao americano (16,68). Na distribuição proporcional dos tipos de HV, no Brasil, 82,1% dos casos correspondiam às hepatites não especificadas, enquanto nos EUA totalizavam 1,5% do total notificado. Ou seja, em nosso meio, a subnotificação é mais elevada e o SVE apresenta, entre outros, um importante problema a ser contornado: o alto custo do diagnóstico etiológico.
Aplicabilidade de um SLS no monitoramento das infecções pelo VHA e VHB
Mesmo reconhecendo a gravidade e magnitude destas endemias, estudá-las é um desafio, dada a elevada freqüência de infecções inaparentes que demandam estudos sorológicos de alto custo. A identificação do marcador sorológico para as hepatites A e B, custa entre 2,00 e 24,00 dólares por exame.25,26
Embora o número de notificações possa dobrar com a vigilância ativa de casos, nem mesmo esta poderia obter a totalidade dos casos de HV27. Levy et al. verificaram um aumento de três vezes no número de casos diagnosticados com um sistema baseado em notificações de portadores assintomáticos de HBsAg de um grande banco de sangue.28
A obtenção de informações centrada em casos suspeitos e confirmados pressupõe a procura por atenção médica, o que não costuma ocorrer com os assintomáticos, acrescentando mais uma limitação ao SVE baseado em casos notificados. Ou seja, a detecção do agravo freqüentemente ocorre em screenings ou em casos crônicos, quando a infecção já seguiu seu curso natural com seqüelas. Portanto, as informações obtidas pelo SVE vigente tornam-se de baixa sensibilidade para a identificação e monitoramento destas infecções.
Tradicionalmente, nessa situação, os inquéritos populacionais de soroprevalência têm boa aceitação, apesar de seu alto custo operacional. Entretanto, estes estudos refletem situações particulares de grupamentos populacionais em relação ao tempo, dificultando a comparação com outros estudos e a análise da tendência secular dos eventos enfocados.29 Por outro lado, as barreiras operacionais a serem vencidas tornam-se por vezes tão difíceis que levam a perdas consideráveis da amostra e possíveis vieses. Diante dessas dificuldades, acompanhar a tendência histórica de infecções assintomáticas através de inquéritos torna-se um árduo empreendimento, não sendo efetuado com a regularidade necessária para que haja confiabilidade nas séries temporais obtidas.
Reconhecendo a necessidade de um SVE que possa adequar-se ao controle de infecções de caráter predominantemente subclínico e, no caso da hepatite B, de evolução crônica, surge a alternativa de utilizar a vigilância sentinela destes eventos. Cabe, portanto, discutir uma metodologia de vigilância sentinela através de laboratório de análises clínicas, de menor custo operacional que os inquéritos, que poderá complementar as informações da VE, proporcionando subsídios à compreensão da dinâmica da distribuição das hepatites A e B, promovendo a sensibilização política, a mobilização de financiamentos e subsidiando o gerenciamento de programas de prevenção para otimizar a aplicação de recursos.
Considerando o investimento que o MS vem aplicando no controle das hepatites A e B, através da Coordenação de Laboratórios, do Centro Nacional de Epidemiologia, do Instituto Evandro Chagas (Belém/PA) e do Centro de Referência Nacional para Hepatites Virais da FIOCRUZ, com a implementação do diagnóstico etiológico, a proposta de laboratórios sentinelas resgata o papel dos Laboratórios de Saúde Pública no apoio aos serviços de saúde, à VE e à pesquisa.30,31
A vigilância através de postos sentinelas, preconizada para regiões onde o SVE é deficiente ou ausente, ou para complementar o sistema existente, aplica-se, de modo singular, às infecções em estudo.32,33,34 Alvo de críticas pela limitação de não lidar com a totalidade dos serviços de saúde, prejudicando a representatividade dos dados, torna-se útil por possibilitar a obtenção de informações de modo regular e oportuno.
Na busca de alternativas efetivas, de maior simplicidade e de baixo custo operacional, que pudessem complementar e aperfeiçoar os dados da VE das HV, foram identificadas, na revisão bibliográfica, proposições semelhantes à apresentada, em outros países ou para outras doenças. Ferreira e cols. 7 realizaram um estudo de soroprevalência do VHA com amostra proveniente de laboratório de análises clínicas, sem que esta fosse a ênfase dos autores. Apesar das limitações relativas à composição etária e por sexo destas amostras, estudos similares com resultados de triagens sorológicas de doadores de sangue são efetuados há algum tempo e estas soroprevalências vêm tendo grande utilidade na comparação dos níveis de endemicidade das HV.35,36,37,38,39
Em relação a outras doenças, verifica-se que, nos EUA, desde 1989, existe um sistema nacional de vigilância sentinela do HIV que realiza estimativas prevalência a partir de amostras de sangue coletadas na rotina laboratorial com outros propósitos, após serem removidas as identificações do paciente.40 À semelhança deste, o Brasil vem desenvolvendo um SVS do HIV, desde 1992, em que os excedentes de soros coletados em clínicas de DST, maternidades e serviços de emergência públicos são aproveitados para a pesquisa soroprevalência do HIV nesses grupos populacionais.41 Estes sistemas têm como objetivo prover dados para ações de saúde pública e são alternativas de interesse no estudo da prevalência do HIV.42,43
Weinstein e cols., avaliando o uso de sentinelas no monitoramento de arboviroses no sul da Austrália, a partir da pesquisa da soroprevalência em sangue doado, concluíram ser possível obter informações sobre as taxas de infecções subclínicas e, através dos dados de soroprevalência por idade, classificar áreas geográficas segundo o risco. Referem ainda que, como a infra-estrutura para a coleta do material já existe, o custo adicional para o sistema de vigilância é virtualmente inexistente.44
Conceitua-se vigilância sentinela como aquela que através da seleção de um ou mais serviços de saúde - onde se concentram esforços na obtenção de informações epidemiológicas - permite o monitoramento de agravos.45 O atributo de sentinela pode ser aplicado a diversas unidades de observação, como postos, serviços, eventos, populações e médicos. Serviços de saúde sentinelas podem abranger uma grande variedade como hospitais, ambulatórios, maternidades e laboratórios, dentre outros. O traço comum a todos eles é a alusão implícita a um microcampo de informação de sensibilidade suficiente para monitorar um certo universo de fenômenos.46
A falta de representatividade está entre uma de suas principais críticas, pelo de não se trabalhar com o universo amostral e em virtude de a seleção dos locais sentinelas não ser efetuada com em critérios aleatórios. St Louis e cols.47 contra-argumentando, lembram os principais objetivos da vigilância hospitais sentinelas do HIV não requerem inferência para a população geral ou para entidades geográficas. Acrescentam que, para análises de tendência em que os critérios de elegibilidade e os métodos de seleção permanecem inalterados ao longo do tempo, a tendência amostral observada deve refletir a da infecção nas comunidades de onde procedem os participantes dos estudos.
Os agravos à saúde aqui estudados apresentam particularidades que os tornam de difícil acompanhamento pelos sistemas tradicionais de VE, traduzindo-se pela persistente subnotificação e reduzida especificação etiológica que resultam em subestimação de sua magnitude e retardo das ações de controle. Supostamente mais abrangente, VE de casos notificados tende a não ser representativa, necessitando, freqüentemente, de estudos especiais de soroprevalência para suprir estas limitações.48 Como alternativa, as amostras de sangue doado têm sido aproveitadas e constituem fontes de informações adicionais, onde os serviços de hemoterapia podem funcionar também como postos sentinelas.38,39
Por outro lado, experiências bem sucedidas de vigilância sentinela em outros países podem servir de reforço à implantação desta estratégia em nosso meio. Na França, uma rede de médicos sentinelas é responsável pela notificação influenza, HV, uretrite aguda, sarampo caxumba e pela divulgação de boletins epidemiológicos eletrônicos.49 O CDC possui o Programa de Vigilância das HV, 12 estados notificadores, objetivando monitorar os casos agudos e identificar fatores de risco mais freqüentes.11,50 Comunidade Econômica Européia existe uma rede de postos sentinelas de influenza para aumentar a sensibilidade sistema de notificação, fortalecer a comunicação entre os países e agilizar a disseminação de informações.51
Bases técnicas de um SLS para as infecções por VHA e VHB
Excedentes de soros como fonte de informação para a VE
Estudos de prevalência que utilizaram soros excedentes, a partir de sangue doado, são encontrados na literatura, como o de Yoshida e cols. em que um estudo soroepidemiológico das hepatites A e B, citomegalovírus e herpes simples tipo 2 foi efetuado em primodoadores de sangue no RJ.52 Alguns destes estudos, como os de Ferreira e cols. e de Miranda e cols. utilizaram amostras de sangue de laboratórios, ambulatórios ou unidades básicas de saúde.7,53 Hadler e cols., todavia, comentam a possibilidade de ...organizar estudos mais metódicos sobre a epidemiologia do VHB em bancos de sangue.37
A opção de trabalhar com excedentes de soro coletados na rotina laboratorial preserva um princípio ético de relevância. Inquéritos populacionais de soroprevalência do VHA e VHB, ao necessitarem colher sangue de pessoas saudáveis expondo-as aos riscos, mesmo que insignificantes, deste procedimento, sem lhes trazer nenhum benefício direto, podem ser questionáveis.
Considerando-se a crise econômica dos países em desenvolvimento, verifica-se que, como a infra-estrutura necessária à implantação e manutenção de um SLS já existe, seu custo tende a ser inferior ao do sistema vigente. Adicionalmente, uma parcela desta estrutura está localizada em serviços privados de saúde, não onerando o SUS e permitindo, inclusive, o controle da qualidade destes serviços.
Não se pode desprezar o efeito benéfico que poderá advir da atuação de setores da saúde que, tradicionalmente, não costumam atuar cooperativamente. Um SVE que possa ampliar suas fontes de informação para além das unidades notificadoras do SUS, abrangendo o setor privado, os serviços de hemoterapia e os laboratórios de análises clínicas, poderá crescer em representatividade e efetividade. Ao estarem organizados em rede, estes sistemas podem ser complementares e fornecer valiosas informações de caráter comparável.
Uso da prevalência na identificação de áreas e populações de risco
O sucesso do controle da varíola - infecção de transmissão predominantemente direta, aguda, sintomática e grave - imprimiu este modelo de VE para as demais doenças. Centrado na investigação caso a caso, com ações de controle predominantemente sobre o indivíduo, com indicação de isolamento e quarentena de casos e contatos, contava com seu caráter de peste para mobilizar esforços dos profissionais e comunidade no seu combate.
Entretanto, um sistema de vigilância para as HV, modelado pelo da varíola, não supre as condições necessárias ao conhecimento dos grupos mais atingidos, dos fatores de risco predominantes e à oportunidade das ações de controle.
Infecções de transmissão tanto direta quanto indireta, com uma proporção de casos inaparentes maior do que a de sintomáticos, de evolução por vezes insuspeita à cronicidade (B e C), freqüentemente benignas e de baixa transcendência, não se amoldam a sistemas que iniciam a ação a partir de casos notificados. Como a maioria dos casos é desconhecida do próprio indivíduo infectado, não chega a ser conhecida pelo sistema de notificação, permanecendo submersa.
A opção pelo monitoramento de marcadores de prevalência destas infecções, embora não permita o conhecimento dos casos incidentes diretamente, possibilitará mapear os grupos mais vulneráveis e as áreas de risco. Estas informações poderão ser úteis na indicação de prioridades na prevenção da ocorrência de novos casos, quer assintomáticos ou não. Quanto à incidência, é possível também estimá-la a partir do conhecimento da prevalência.54
Aspectos relativos à implantação e manutenção do sistema
Respeitando as diretrizes do SUS, o primeiro passo necessário à implantação é a ampla discussão com os Conselhos Municipais de Saúde (CMS) e a comunidade. Estes CMS, participando das fases de delineamento da estrutura, contribuirão para amoldá-la às diversas realidades locais e para mobilizar a comunidade no sentido de colaborar na sua implantação e avaliação. Para que estes CMS possam conhecer os objetivos, produtos, vantagens, abrangência e limitações de um sistema desta natureza, a elaboração de discussões de ordem técnica é importante.
Como o interesse concentra-se em monitorar as infecções prevalentes através de amostras excedentes de soro de laboratórios de análises clínicas, a principal limitação, visto que os casos agudos não serão detectados, é a impossibilidade de realizar ações de bloqueio no caso de surtos. Entretanto, para períodos epidêmicos, os casos agudos e sintomáticos são reconhecidos pelo SVE existente, não necessitando de suplementação.
O acompanhamento de uma doença na comunidade pode ser enriquecido pelo conhecimento da dinâmica de circulação de seus agentes, como já existe para o sarampo, rubéola, difteria, poliomielite e outras, através da tipagem molecular, para complementar a informação coletada pela vigilância.55
Além das infecções pelos VHA e VHB, na dependência dos aspectos específicos de cada uma, outras hepatites e doenças poderão ser estudadas concomitantemente. A possibilidade de manter uma soroteca permite pesquisas futuras de outros agentes de doenças. Sir Richard Doll, ao ser questionado sobre o que faria se fosse iniciar um estudo caso-controle atualmente, respondeu que, além de ser necessário conhecer o país sede do estudo e os recursos disponíveis, coletaria e congelaria amostras de sangue de todos os indivíduos para que fosse possível posteriormente identificar diversos outros agentes.56
Este monitoramento terá como produto de maior relevância a identificação de áreas e populações mais vulneráveis ao risco de adquirir estas infecções, indicando prioridades de ações voltadas à sua prevenção e controle. Um produto adicional – o desencadeamento de ações direcionadas aos soronegativos (suscetíveis) - só seria possível no caso de o estudo identificar os sujeitos selecionados. Para tal, requer-se amplo debate com a sociedade sobre a preservação do direito individual de recusa na participação e da opção de ser informado (ou não) sobre os resultados dos testes efetuados. Operacionalmente, a garantia destes direitos poderia ser obtida pela inclusão, nos formulários de rotina dos laboratórios, de item objetivo, onde cada paciente pudesse expressar sua vontade quanto a participar e a ser informado.
No caso do HIV, o CDC Family Surveys acompanha a tendência desta infecção nos EUA mantendo coleta anônima não vinculada.33,57 As infecções por VHA e VHB, dispondo de vacinas seguras e eficazes, impõem reflexões de maior complexidade. Embora o desencadeamento da Aids possa ser retardado pelo uso de anti-retrovirais nos portadores do HIV, no caso das hepatites A e B, a imunização pode evitar sua ocorrência nos suscetíveis.
A abrangência deste sistema, voltando-se também para as pessoas que demandam serviços privados de saúde, permite obter dados mais representativos do universo e ainda estimar o diferencial de risco entre os subgrupos, de acordo com a procedência.
Buscando otimizar a operacionalização, sem desprezar a importância de reduzir a presença de vieses de seleção, é mais sensata a escolha de laboratórios sentinelas que apresentem a maior demanda na localidade, sejam de fácil acesso, e ofereçam um amplo leque de exames.34
No sentido de garantir ao máximo a validade interna deste monitoramento, obtendo-se estimativas de soroprevalências mais representativas, a amostra deverá ser obtida de forma estratificada por sexo, idade e localidade de residência, de acordo com a pirâmide demográfica e com o comportamento epidemiológico da infecção na comunidade estudada.34
A periodicidade da obtenção de amostras estará na dependência direta dos resultados obtidos a cada etapa e da possível presença de ciclos regulares nas curvas de incidência das hepatites A e B. Por outro lado, como estratégia de implantação do sistema, a proposição de intervalos deverá ser ponderada sob critérios técnicos e também político-culturais, facilitando a criação de rotina.
Potencialidades e limitações do sistema: o caso de Macaé
Os resultados de uma pesquisa de soroprevalência do VHA e VHB em amostras excedentes de soro de laboratório de análises clínicas situado no Município de Macaé foram avaliados para verificar-se a consistência dos valores encontrados, diante da realidade local e de dados da literatura, da possibilidade de se monitorar a tendência destas infecções e da potencialidade de detecção de gradientes de variação dos valores obtidos.3,58,59 Embora esta pesquisa de soroprevalência apresentasse a limitação de uma amostra não estratificada por idade e sexo, a curva de tendência da soroprevalência do anti-HAV total nos menores de 20 anos mostra a elevação com a idade (Figura 1) observada em inquéritos domiciliares.60 Diferentes patamares de soroprevalência observados devem-se a uma combinação de fatores ligados aos diversos objetivos e metodologias de cada estudo.
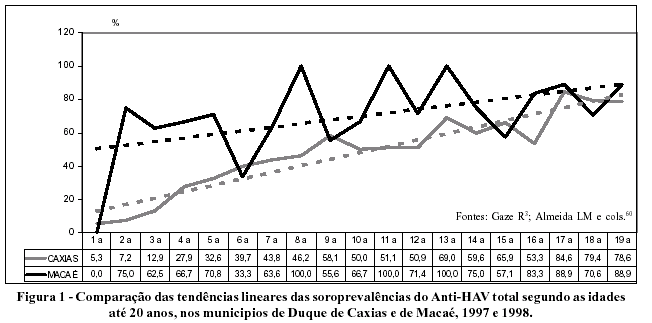
Por exemplo, o método de coleta de sangue em papel de filtro, utilizado em alguns estudos, leva a uma subestimação do parâmetro. Gil e cols., em estudo de validação desta estratégia para estudos epidemiológicos, encontraram uma sensibilidade de 91,3 e uma especificidade de 99,3%, utilizando o ELISA.61 Zoulek e cols., através do radioimunoensaio, verificaram que 20,7% dos soros positivos não teriam sido detectados no eluato do papel de filtro. Observando que, quanto mais baixos os títulos, maior pode ser a subestimação da soroprevalência, concluem que, em regiões endêmicas para o VHA, a soroprevalência nas idades mais velhas através do método de coleta de sangue em papel de filtro pode ser muito inferior à real.62
Na pesquisa referida, com todos os procedimentos de coleta efetuados em ambiente laboratorial e utilizando-se amostras de soro por punção venosa, pôde-se dispor da validade de um método (ELISA) de uso difundido em inquéritos de soroprevalência e considerado como padrão para avaliar a sensibilidade e especificidade de outros63. Por outro lado, uma amostra com intervalos de confiança de menor precisão pode ter levado à superestimação das soroprevalências.
Neste mesmo estudo, a amostra foi dividida em dois subgrupos utilizando o tipo de assistência médica prestada como traçador do nível socioeconômico dos sujeitos. Isto é, as pessoas cujas solicitações de exames provinham de unidades do SUS foram consideradas como de grupos menos favorecidos e as originárias de serviços de saúde privados (NSUS) como pertencentes à fração restante. Enquanto a soroprevalência amostral do anti-HAV total foi de 88,8%, nos subgrupos SUS e NSUS foram, respectivamente, de 94,1% e 83,5% (c2=31,15 e p<0,0001), para o anti-HBc total, a soroprevalência amostral foi de 15,3%, a do SUS de 19,5% e a do NSUS de 11,0% (c2=15,41 e p<0,0001).3 Em ambos, foi possível afirmar que a diferença observada não ocorreu ao acaso. Sendo assim, adaptando-se a amostra às regiões que se pretenda estudar, é possível acompanhar a prevalência destas infecções em áreas geográficas diversas. Mais importante ainda é que, com a padronização dos procedimentos, os dados obtidos poderão ser comparados no tempo.
Observou-se ainda que para o VHA, 65,6% (55,2-74,8) dos menores de dez anos, 79,7% (71,5-86,1) dos adolescentes e 88,5% (84,8-91,4) dos adultos jovens já haviam sido infectados. Abuzwaida e cols.64 detectaram que 47 e 82% entre os menores de dez anos e 85 e 90% entre os adultos jovens, respectivamente em Niterói e Nova Iguaçu, já haviam sido infectados por este vírus.
Para o VHB, a soroprevalência foi de 5,1% (1,2-12,1) nos menores de dez anos, elevando-se para 9,4% (5,2-16,1) entre os adolescentes e 10,6 (7,8-14,2) nos adultos jovens, passando a 17,3% (13,4-21,9) nos mais idosos e chegando a 33,8% (26,5-41,8) nos acima de 60 anos. Vasconcelos e cols. encontraram valores de 14% em doadores de sangue em Florianópolis/SC e Passos e cols. 7,5% entre os menores de dez anos e 10,4% na faixa de dez a 25 anos, em uma comunidade rural paulista.65,66
Critérios para avaliação do sistema
Como qualquer SVE, este SLS requer avaliação criteriosa de suas vantagens/limitações e atualizações continuadas, possibilitando a correção e redirecionamento de métodos e objetivos.
A Figura 2 apresenta, de forma esquemática, uma avaliação das potencialidades e limitações deste sistema.
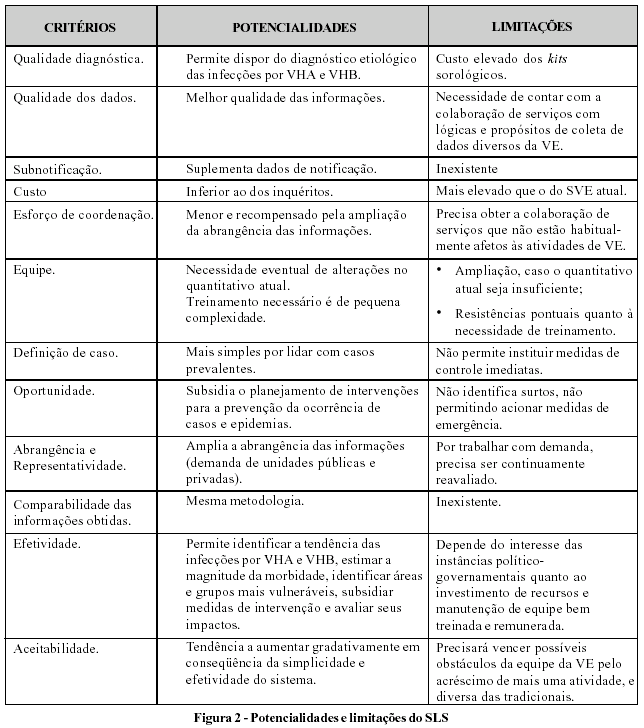
Os critérios de avaliação do CDC podem ser aplicados na sua avaliação com a vantagem de estarem internacionalmente reconhecidos e permitirem a comparação com avaliações efetuadas em outros sistemas.4 Este processo deverá considerar a realidade local, os objetivos e métodos, e a disponibilidade de recursos. Na Figura 3 encontra-se um roteiro com alguns instrumentos que poderão ser utilizados nesta atividade.67
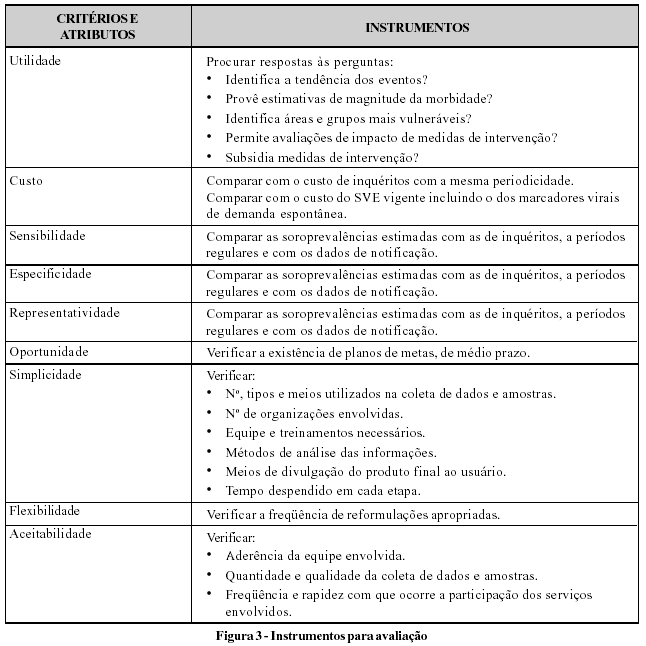
Conclusões
As especificidades das HV podem ser apreciadas sob a ótica dos critérios de avaliação do Centers for Disease Control and Prevention.4 Um SVE passivo, ainda que de baixo custo como o existente, torna-se de pouca utilidade no monitoramento de infecções freqüentemente assintomáticas e, cumulativamente, afetam sua sensibilidade, representatividade e oportunidade, não se podendo estimar a magnitude destes eventos nem se tomar medidas de intervenção em tempo hábil. De complexidade considerável e voltado para doenças de letalidade aparentemente reduzida torna-se de difícil aceitabilidade.68
Controlar a propagação das infecções pelo VHA e VHB eleva as condições de saúde e a qualidade de vida da população, além de reduzir, substancialmente, o custo com assistência médica de casos evitáveis. Transformar o SVE existente em um monitoramento efetivo das HV exige criatividade e apropriação de conhecimentos e metodologias aplicados com sucesso em outros sistemas de vigilância, como os sentinelas. Programas de prevenção, fundamentados em informações atualizadas, poderão ser melhor ajustados para cada região, contribuindo para a redução oportuna e eficaz da ocorrência de casos e da conseqüente demanda hospitalar.
Este artigo teve como objetivo principal discutir a aplicabilidade de um SLS no sentido de obter respostas, com eficácia e eficiência, à questão: Como monitorar doenças de gravidade reconhecida, mas que apresentam significativa proporção de casos sem exteriorização clínica ou nas quais esta só ocorre na fase crônica?
Atualmente, o monitoramento das HV exige a realização de estudos de soroprevalência, para uma adequada avaliação da magnitude destas infecções predominantemente inaparentes. Os inquéritos domiciliares habitualmente utilizados para este fim, embora de sensibilidade inquestionável, terminam por não ser, pelo seu alto custo operacional efetuados com a regularidade necessária.
Embora a metodologia apresentada não elimine o gasto com a pesquisa de marcadores sorológicos, permite sua redução. Por outro lado, o caráter endêmico-epidêmico da hepatite A, as epidemias que freqüentemente provoca, sua alta carga e o custo do tempo de afastamento do trabalho10 tornam plenamente justificáveis estes gastos.
Corroborando estas justificativas, citam-se o alto custo e a baixa eficácia da terapêutica de pacientes crônicos (VHB) e o elevado percentual de portadores.13
Reconhecendo que, como afirmam Teixeira e cols., 18 a exigência de notificação universal das HV pouco contribui para sua VE tendo em vista os diversos mecanismos de transmissão de cada tipo, um SLS centrado no diagnóstico sorológico das infecções pelos vírus das hepatites contorna este problema. Permite a coleta sistemática de dados e o acompanhamento contínuo de longo prazo, com regularidade e freqüência adequadas.
À semelhança do estudo de Macaé, que permitiu a detecção de gradientes nos percentuais de soroprevalência e evidenciou a maior precocidade da infecção nos grupos socioeconômicos menos favorecidos, esta metodologia mostra sensibilidade adequada ao monitoramento das hepatites A e B, com o objetivo de acompanhar a tendência destas infecções em distintas localidades e de traçar prioridades de ações de prevenção e controle3.
O monitoramento da tendência das hepatites A e B possibilitará identificar áreas e grupos de risco, subsidiar estratégias de vacinação de suscetíveis, migrantes e viajantes e avaliar impactos de intervenções relativas ao saneamento básico, à qualidade do sangue e das campanhas de prevenção de doenças sexualmente transmissíveis e do uso de drogas.
Interromper a cadeia de transmissão destas infecções poderá contribuir para evitar o aumento da carga destas doenças: da hepatite A, impedindo sua ocorrência em idade adulta com expressão clínica de maior gravidade; da hepatite B, evitando a evolução silenciosa para casos de cirrose e neoplasia hepáticas.
Estrategicamente, a um só tempo reduzindo custos e preservando princípios éticos, esse SLS pode complementar as informações da VE, compreender a dinâmica da distribuição das infecções por VHA e VHB, promover a sensibilização política e a mobilização de financiamentos e subsidiar o gerenciamento de programas de prevenção.
Agradecimentos
Ao Prof. Francisco Esteves pela contribuição na elaboração deste estudo, à Dra. Maura Selvaggi Soares pela revisão do presente artigo e ao Projeto de Avaliação dos Impactos sobre a Saúde e a Qualidade de Vida do Programa de Despoluição da Baía da Guanabara/ NESC/UFRJ.
Referências bibliográficas
1. World Health Organization. Prevention and control of diarrheal diseases. [online]. Geneva: Oct. 1997. Disponível na Internet: http://www.who.ch/programmes/cdr/pub/cdd/cddpub.htm.
2. Murray CJL, Chen LC. Understanding morbidity change. In: Murray CJL, Michaud C, Mahapatra P, Acharya A, Shibuya K, Lozano R. et al. Designing and implementing a national burden of disease study. Boston: Burden of Disease Unit Harvard Center for Population and Developments Studies; 1992. p.50-72.
3. Gaze R. Hepatites virais: alfabeto submerso [dissertação] Rio de Janeiro (RJ): UFRJ; 1999.
4. Centers for Diseases Control and Prevention. Guidelines for evaluating surveillance systems. MMWR 1988; 37(55) : 1-18.
5. Havens Jr. WP. Viral hepatitis. Medical Clinics of North America 1970; 54(2) : 455-466.
6. Centers for Diseases Control and Prevention. Viral hepatitis. [online]. Atlanta: 2000. [capturado 23 02 2000]. Disponível na Internet: http:// www.cdc.gov/ncidod/diseases/hepatitis.
7. Ferreira CT, Silva GL, Barros FC, Lima JP. Soroepidemiologia da hepatite A em dois grupos populacionais economicamente distintos de Porto Alegre. Gastroenterologia Endoscopia Digestiva 1996; 15(3) : 85-90.
8. Centers for Diseases Control and Prevention. Epidemiology and prevention of viral hepatitis A to E:: an Overview. [online]. Atlanta: 1997.[capturado 12 12 97]. Disponível na internete: http:// www.cdc.gov/ncidod/diseases/ hepatitis/hepatitis htm.
9. Kilpatrick ME, Escamilla J. Hepatitis A in Peru: the role of children. American Journal of Epidemiology 1986; 124(1) : 111-113.
10. Lemon SM. Inactivated hepatitis A virus vaccines. Hepatology 1992; 15(6) : 1194-1197. [Editorial].
11. Centers for Diseases Control and Prevention. Viral hepatitis surveillance program. Report n. 56. [online]. Atlanta: 1996. Disponível na Internet: http://www.cdc.gov/ncidod/diseases/ hepatitis/h96surve.htm.
12. Lyra LGC. Hepatites a Vírus A, B, C, D e E. In: Dani R, Castro LP. Gastroenterologia clínica. 3. ed. Rio de Janeiro: Guanabara Koogan; 1993. p.1251-1287.
13. World Health Organization. Expanded programme on immunization: hepatitis B vaccine - making global progress. Geneva: Oct. 1996.
14. Murray CJL, Lopez AD. Estimating causes of death: new methods and global and regional applications for 1990. In: Murray CJL, Lopez AD. The Global Burden of Disease: A comprehensive assessment of mortality and disability from diseases, injuries, and risk factors in 1990 and project to 2020. Boston: WHO; 1996. p.118-200.
15. Moraes DM, Castillo EAS. Análise epidemiológica das hepatites virais no Brasil, no período de 1993 - 1996. In: Livro de Resumos do IV Congresso Brasileiro de Epidemiologia; 1998. Rio de Janeiro; 1998. p.238.
16. Hu DJ, Kane MA, Heymann DL. Transmission of HIV, hepatitis B virus, and other bloodborne pathogens in health care settings: a review of risk factors and guidelines for prevention. Bulletin of the World Health Organization 1991; 69(5) : 623-630.
17. Murray CJL, Lopez AD. Alternative visions of the future: projecting mortality and disability, 1990-2020. In: Murray CJL, Lopez AD. The global burden of disease: a comprehensive assessment of mortality and disability from diseases, injuries, and risk factors in 1990 and project to 2020. Boston: WHO. Harvard School of Public Health. World Bank., 1996. p.325-395.
18. Teixeira MG, Penna GO, Risi JB, Penna ML, Alvim MF, Moraes JC, Luna E. Seleção das doenças de notificação compulsória: critérios e recomendações para as três esferas de governo. Informe Epidemiológico do SUS 1998; VII(1) : 7-28.
19. Ministério da Saúde. Portaria n. 1100, de 24 de maio de 1996. Estabelece a Lista Nacional de Doenças de Notificação Compulsória. Diário Oficial da União, Brasília, v.84, n.101, p.9133, 27 maio 1996. Seção I, pt.1.
20. Ministério da Saúde. Portaria n. 4052, de 23 de dezembro de 1998. Estabelecea Lista Nacional de Doenças de Notificação Compulsória. Diário Oficial da União, Brasília, v.86, n.247-E, p.19, 24 dez. 1998. Seção I, pt.1.
21. Ministério da Saúde. Portaria n. 1461, de 22 de dezembro de 1999. Estabelece a Lista Nacional de Doenças de Notificação Compulsória. Diário Oficial da União, Brasília, v.87, n.245-E, p.34, 23 dez. 1999. Seção I, pt.3.
22. Fundação Nacional de Saúde. Boletim Epidemiológico 1996 out.; 1(10) : 2. [Editorial].
23. Ministério da Saúde. Informações de saúde: população residente estimada pelo IBGE. [online]. [citado em nov. 1997]. Disponível na Internet: http://www.datasus.gov.br/cgi/deftohtm.exe?ibge/popbr.def.
24. Alter MJ, Mares A, Hadler SC, Maynard J F. The effect of underreporting on the apparent incidence and epidemiology of acute viral hepatitis. American Journal of Epidemiology 1987; 125 : 1339.
25. Yoshida CFT. Centro de referência nacional para hepatites virais da FIOCRUZ. 1999. [Comunicação pessoal]
26. Borges DR. Considerações numéricas sobre os resumos submetidos ao XIII Congresso Brasileiro de Hepatologia. Gastroenterologia Endoscopia Digestiva 1995; 14(4) : XIV. [Editorial]
27. Vogt RD, Larue D, Klaucke DN, Jillson DA. Comparison of an active and passive surveillance system of primary care providers for hepatitis, Measles, Rubella, and Salmonellosis in Vermont. American Journal of Public Health 1983; 73 : 795-797.
28. Levy BS, Mature J & Washburn JW. Intensive hepatitis surveillance in Minnesota: methods and results. American Journal of Epidemiology 1977; 105(2) : 127-134.
29. Andrade ALSS, Martelli CMT, Pinheiro ED, Santana CL, Borges FP & Zicker F. Rastreamento sorológico para doenças infecciosas em banco de sangue como indicador de morbidade populacional. Revista de Saúde Pública 1989; 23(1) : 20-25.
30. Ginuino CF. Sistema de informação para hepatites virais: como se desenha o fluxo da informação sobre hepatites no estado e no município do Rio de Janeiro [Monografia de Curso de Especialização em Saúde Pública]. Rio de Janeiro: Escola Nacional de Saúde Pública/ FIOCRUZ/MS; 1997.
31. Waldman EA. Vigilância epidemiológica como prática de saúde pública [Tese de Doutoramento]. São Paulo: Faculdade de Saúde Pública/USP; 1991.
32. Petersen LR, Calonge NB, Chamberland ME, Engel RH, Herring NC. Methods of surveillance for HIV infection in primary care outpatients in the United States. Public Health Reports 1990; 105(2) : 158-162.
33. St.Louis ME, Raugh KJ, Petersen LR, Anderson JE, Schable CA, Dondero TJ and The Hospital Surveillance Group. Seroprevalence rates of human Immunodeficiency virus infection at sentinel hospitals in the United States. New England Journal of Medicine 1990; 323(4) : 213-218.
34. Alary M, Joly Jr., Parent R, Fauvel M, Dionne M. Sentinel hospital surveillance of HIV infection in Quebec. Canadian Medical Assocation Journal 1994; 151(7) : 975-981.
35. Martelli CMT, Andrade ALSS, Cardoso DDP, Almeida E , Silva S, Zicker F. Considerações metodológicas na interpretação do rastreamento sorológico da hepatite B em doadores de sangue. Revista de Saúde Pública 1991; 25(1) : 11-16.
36. Szmuness W, Dienstag JL, Purcell RH, Harley EJ, Stevens CE, Wong DC, Ikram H, Barshany S, Beasley RP, Desmyter J & Gaon JÁ. The prevalence of antibody to hepatitis A antigen in various parts of the world: a pilot study. American Journal of Epidemiology 1977; 106(5) : 392- 398.
37. Hadler SC, Fay OH, Pinheiro F, Maynard JE. La hepatitis en las Américas: informe del grupo colaborador de la OPS. Boletin de la Oficina Sanitaria Panamericana 1987; 103(3) : 185-209.
38. Murphy EL, Brysman S, Williams AE, Co-Chien H, Schreiber GB, Ownby HE, Gilcher RO, Kleinman SH, Matijas L, Thompson RA, Enmo GJ. Demographic determinants of hepatitis C virus seroprevalence among blood donors. Journal of The American Medical Association 1996; 275(13) : 995-1000.
39. Dubois F, Desenclos JC, Mariotte N, Goudeau A. Hepatitis C in a French population-based survey, 1994: seroprevalence, frequency of viremia, genotype distribution, and risk factors. Hepatology 1997; 25(6) : 1490-1496.
40. Pappaioanou M, Dondero TJJr, Petersen LR, Onorato IM, Sanchez CD, Curran JW. The family of HIV seroprevalence surveys: objectives, methods, and uses of sentinel surveillance for HIV in the United States. Public Health Reports 1990; 105(2) : 113-119.
41. Ministério da Saúde. Coordenação Nacional de DST/AIDS. Estudos de prevalência do HIV. [online] Brasília: 1999. [citado em mar. 1999]. Disponível na Internet: http://www. aids.gov.br/uvad/compila.htm.
42. Onorato IM, Gwinn M, Dondero TJJR. Applications of data from the CDC family of surveys. Public Health Reports 1994; 109(2) : 204-211.
43. Sherlock CH, Strathdee SA, Le T, Sutherland D, O'shaughnessy MV, Schechter MT. Use of pooling and outpatient laboratory specimens in an anonymous seroprevalence survey of HIV infection in British Columbia, Canada. AIDS 1995; 9(8) : 945-950.
44. Weinstein P, Worswick D, Macintyre A, Cameron S. Human sentinels for arbovirus surveillance and regional risk classification in South Australia. Medical Journal of Australian 1994; 160(8) : 494-499.
45. Pereira MG. Vigilância epidemiológica. In: Pereira MG. Epidemiologia: teoria e prática. Rio de Janeiro: Guanabara Koogan; 1995. p.449-482.
46. Samaja J. Muestras y representatividad en vigilancia epidemiologica mediante sitios centinelas. Cadernos de Saúde Pública 1996; 12(3) : 309-319.
47. St. Louis ME, Olivo N, Critchley S, Rauch KJ, White CR, Munn VP, Dondero TJ. Methods of surveillance for HIV infection at US sentinel hospitals. Public Health Reports 1990; 105(2) : 140-146.
48. Villarejos VM, Serra JC, Anderson- Visoná K, Mosley JW. Hepatitis A virus infection in households. American Journal of Epidemiology 1982; 115(4) : 577-586.
49. Valleron AJ, Bouvet E, Garnerin P, Ménarès J, Heard I, Letrait S, Lefaucheux J. A computer network for the surveillance of communicable diseases: the French experiment. American Journal of Public Health 1986; 76(11) : 1289-1292.
50. Centers for Diseases Control and Prevention. Trends based on reporting to the national notifiable diseases surveillance system. [online]. Atlanta: 1993. [citado em Apr. 1996]. Report n. 56. Disponível na Internet: http://www.cdc.gov/ncidod/diseases/hepatitis/h96trend.htm.
51. Velden K. The european influenza surveillance scheme. [online]. Paris: Netherlands Institute of Primary Health Care, 1999. Disponível na Internet: http://www.eiss.org.
52. Yoshida CFT, Nogueira MMR, Mercadante LAC, Pinhão AT, Schatzmayr HG. Seroepidemiological survey of hepatitis A and B, cytomegalovirus and herpes simplex type 2 in prime blood donors from Rio de Janeiro, Brazil. Revista de Microbiologia 1987; 18(1) : 5-11.
53. Miranda LVG, Passos ADC, Figueiredo JFC, Gaspar AMC, Yoshida CF. Prevalência de anticorpos contra hepatite A em população submetida à coleta de sangue em unidades de saúde. In: Livro de Resumos do IV Congresso Brasileiro de Epidemiologia. Rio de Janeiro 1998. p.235.
54. Freeman J, Hutchison GB. Prevalence, incidence and duration. American Journal of Epidemiology 1980; 112(5) : 707-723.
55. Wharton M, Ching PL. Surveillance indicators.[online]. Atlanta: 1998. Disponível na Internet: http://www. cdc.gov/nip/manual/survindi/ survindi/htm.
56. Doll R. Conversando com Richard Doll. In: IV Congresso Brasileiro de Epidemiologia; 1998; Rio de Janeiro. Rio de Janeiro; 1998. directed testing in a Newark, NJ, Hospital. Archives of Internal Medicine 1991; 151 : 965-968.
58. Gaze R, Carvalho DM, Berro O, Bravim Y, Ginuino CF, Servino VRR. Soroprevalência do anti-HAV em Macaé. Gastroenterologia Endoscopia Digestiva 1999; 18(sl.1) : s32.
59. Gaze R, Carvalho DM, Yoshida CFT, Servino VRR. Soroprevalência do anti-HBc total em dois grupos sócioeconômicos distintos. Gastroenterologia Endoscopia Digestiva 1999; 18(sl.1) : s32.
60. Almeida LM, Luiz RR, Coeli CM, Coletty PE, Santos NM, Santos MLF, Guimarães AAM, Neto RSA, Massad E, Struchiner CJ. Soroprevalência da hepatite A: um possível parâmetro para mensuração de efeitos de intervenções ambientais sobre a saúde. In: Heller L, Moraes LRS, Monteiro TCN, Salles MJ, Almeida LM, Câncio J. Saneamento e Saúde nos Países em Desenvolvimento. Rio de Janeiro: CC&P Editores Ltda, 1997. p.324-348.
61. Gil A, González A, Dal-Ré R, Ortega P, Dominguez V, Astasio P, Aguilar L. Detection of antibodies against hepatitis A in blood spots dried on filter paper. Is this a reliable method for epidemiological studies? Epidemiology and Infection 1997; 118(2) : 189-191. [ Abstract]
62. Zoulek G, Bürger P & Deinhardt F. Markers of hepatitis viruses A and B: direct comparison between whole serum and blood spotted on filter-paper. Bulletin of the World Health Organization 1985; 63(5) : 935-939.
63. Souto FJD, Fontes CJF, Oliveira JM, Gaspar AMC, Lyra LGC. Confiabilidade de teste ELISA de produção nacional para a pesquisa do anticorpo contra o antígeno central da Hepatite B (anti-HBc). Gastroenterologia Endoscopia Digestiva 1995; 14(4) : 137.
64. Abuzwaida ARN, Sidoni M, Yoshida CFT, Schatzmayr HG. Seroepidemiology of hepatitis A and B in two urban communities of Rio de Janeiro, Brazil. Revista do Instituto de Medicina Tropical de São Paulo 1987; 29 : 219-223.
65. Vasconcelos HCCF, Yoshida CFT, Vanderborght BOM, Schatzmayr HG. Hepatitis B and C prevalences among blood donors in south region of Brazil. Memórias do Instituto Oswaldo Cruz 1994; 89(4) : 503-507.
66. Passos ADC, Gomes UA, Figueiredo JFC, Nascimento MMP, Oliveira JM , GasparA MC , Yoshida CFT. Prevalência de marcadores sorológicos de hepatite B numa pequena comunidade rural do Estado de São Paulo, Brasil. Revista de Saúde Pública 1992; 26(2):119-124.
67. FischmannA. Vigilância epidemiológica. In: Rouquayrol, MZ. Epidemiologia & Saúde. 4. ed. Rio de Janeiro: MEDSI; 1993. p.421-441.
68. Wakimoto MD, Marzochi KBF, Hartz ZMA. Avaliação do sistema de vigilância epidemiológica no município do Rio de Janeiro. In: Livro de Resumos do IV Congresso Brasileiro de Epidemiologia; 1998; Rio de Janeiro. Rio de Janeiro; 1998. p.257.
 Endereço para correspondência:
Endereço para correspondência:
Rua Teodoro da Silva, 751 - Apto 504 - Bloco 02
Vila Isabel, Rio de Janeiro/RJ
CEP: 20.560-000
E-mail:zanza@rio.com.br













