Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Epidemiologia e Serviços de Saúde
versión impresa ISSN 1679-4974versión On-line ISSN 2237-9622
Epidemiol. Serv. Saúde v.13 n.1 Brasília mar. 2004
http://dx.doi.org/10.5123/S1679-49742004000100006
Eventos adversos associados à vacina tríplice viral com cepa Leningrad-Zagreb nos Estados de Mato Grosso e Mato Grosso do Sul, durante as campanhas de imunização de 1998*
Adverse events following use of MMR vaccine with Leningrad-Zagreb mumps strain during mass campaigns in Mato Grosso and Mato Grosso do Sul States in Brazil, 1998
Inês DouradoI; Sérgio Souza da CunhaI; Maria de Lourdes Sousa MaiaII; Kátia Mongenor Barbosa LimaIII; Beatriz Alves de Castro SoaresIV; Maurício Lima BarretoI
IInstituto de Saúde Coletiva, Universidade Federal da Bahia, Salvador-BA
IIPrograma Nacional de Imunizações, Departamento de Vigilância Epidemiológica, Secretaria de Vigilância em Saúde, Ministério da Saúde, Brasília-DF
IIISecretaria de Estado da Saúde de Mato Grosso do Sul, Campo Grande-MS
IVSecretaria de Estado da Saúde de Mato Grosso, Cuiabá-MT
RESUMO
No Brasil, as campanhas de imunização com a vacina tríplice viral (TPV) contendo a cepa Leningrad-Zagreb (LZ) têm sido associadas a surtos de meningite asséptica e caxumba. O principal objetivo deste estudo é estimar o risco de meningite e caxumba associado com a campanha de vacinação com TPV-LZ nos Estados de Mato Grosso e Mato Grosso do Sul em 1998. A incidência de meningite e caxumba e razão de incidência (incidência no período pós-campanha, comparada à incidência no período anterior às campanhas) foram estimadas utilizando-se os dados disponíveis no Sistema Nacional de Agravos de Notificação (Sinan). Em ambos os Estados, foram observados surtos de meningite asséptica três semanas após as campanhas, cujas incidências apresentam diferenças estatisticamente significantes, quando comparadas às dos períodos anteriores às campanhas. No Estado de Mato Grosso do Sul, onde dados de caxumba estavam disponíveis no Sinan, também se observou surto de caxumba, cuja incidência foi cerca de 70 vezes maior que a do período anterior à campanha. Discute-se a relação causal entre a campanha e os surtos observados.
Palavras-chave: vacinas; efeitos adversos; vacina tríplice viral; TPV.
SUMMARY
In Brazil mass vaccination campaigns (MIC) with Leningrad-Zagreb mumps strain-based measles-mumps-rubella (MMR-LZ) vaccines have been associated with outbreaks of aseptic meningitis and mumps. The main objective of this paper is to estimate the risk of vaccine-related meningitis and mumps in the States of Mato Grosso and Mato Grosso do Sul in 1998. The incidence of meningitis and mumps and relative risks (comparison of incidence before and after MIC with MMR) were estimated using data from routine surveillance of these two states. Increase in meningitis incidence was observed in both states, three weeks after the MIC, and the incidence was statistically significant when compared to the incidence in periods before the campaign. Regarding mumps, in the State of Mato Grosso do Sul – the only state where data were available – the incidence was 70 times higher after the campaign than the period before. The possible causal association between the campaign and the outbreaks is discussed.
Key words: vaccines; adverse events; measles-mumps-rubella; MMR.
Introdução
A vacina tríplice viral (TPV) é constituída de vírus vivos atenuados e visa prevenir três doenças: sarampo, rubéola e caxumba. Existem diversos tipos de vacinas TPV, que se diferenciam nos vírus vacinais empregados. Cada vacina é constituída de vírus vacinais vivos, causadores de reações adversas semelhantes às manifestações clínicas das infecções naturais. Por exemplo, uma pessoa que recebe uma vacina TPV pode ter mancha cutânea semelhante à de pacientes com sarampo e rubéola. Entretanto, essas reações adversas são bem menos freqüentes que as manifestações provocadas pela infecção natural.
Quanto aos vírus da caxumba, a vacina TPV utilizada no país até 1998 apresentava duas diferentes cepas de vírus: a cepa URABE Am9 (URABE) e a cepa Leningrad-Zagreb (LZ). Como essas cepas são vírus vivos atenuados, as pessoas que recebem a TPV também podem apresentar manifestações clínicas semelhantes à caxumba natural. Por exemplo, é fato conhecido que um percentual significativo dos casos de caxumba natural também apresente meningite: em até 50% dos casos de caxumba, pode haver meningite associada.1 Nem sempre os casos de meningite causados pela caxumba são diagnosticados, porque as manifestações de meningite – febre, dor de cabeça, vômitos – são confundidas com as manifestações da caxumba. Ademais, como tais casos de meningite são provocados pelo próprio vírus da caxumba, não se consegue isolar bactérias na investigação laboratorial de rotina desses casos, e, em geral, o liquor apresenta aspecto e características diferentes das encontradas por meningites bacterianas. Na literatura médica, os casos de meningite em que não se conseguem isolar bactérias (geralmente de etiologia viral, de evolução benigna e de curta duração) são denominados de meningite asséptica.2
Em 1998, campanhas de imunização foram realizadas com vacina TPV contendo a cepa LZ, nos Estados de Mato Grosso, Mato Grosso do Sul, Rio Grande do Norte e Paraíba. As campanhas nos três primeiros Estados utilizaram apenas vacinas contendo a cepa LZ. O objetivo do presente estudo é descrever a ocorrência de meningite asséptica e de caxumba nos Estados de Mato Grosso do Sul (MS) e Mato Grosso (MT) e estimar a associação desses eventos com a campanha de vacinação. Outra versão deste trabalho, com dados adicionais e outros procedimentos estatísticos, foi publicada anteriormente.3
Metodologia
No Estado de Mato Grosso do Sul, a campanha iniciou-se no dia 15 de agosto de 1998 (semana epidemiológica 32). Segundo dados oficiais do Programa Nacional de Imunizações (PNI) sobre o primeiro mês de campanha, estima-se que 442.962 crianças tenham sido vacinadas, para uma população-alvo de 473.718, o que corresponde a uma cobertura vacinal de 94%.
No Estado de Mato Grosso, a campanha iniciou-se no dia 26 de setembro de 1998 (semana epidemiológica 38) e a estimativa para o número de vacinados é de 402.927, em uma população-alvo de 580.587 – cobertura vacinal de 69%. A vacina foi administrada em crianças de 1 a 11 anos de idade, independentemente de vacinação prévia.
Fonte de dados
No estudo, foram utilizados dados de casos de meningite notificados junto ao Sistema Nacional de Agravos de Notificação (Sinan), ocorridos no ano de 1998, em MS; e nos anos de 1996, 1997 e 1998, em MT. Em cada banco de dados, foram selecionadas as seguintes variáveis, contempladas no modelo de ficha de notificação do Sinan:
a) dados de identificação – data de internamento, semana epidemiológica de notificação, idade, sexo;
b) dados referentes ao exame liquórico – aspecto, contagem de leucócitos, linfócitos e monócitos;
c) dados referentes à bacteriologia – cultura e bacterioscopia do liquor e sangue; e
d) diagnóstico etiológico.
Classificação dos casos
Os casos de meningite foram classificados em duas categorias. Na primeira categoria, estão os casos assinalados na ficha de notificação como "viral" e de "etiologia desconhecida", que correspondem à denominação de "casos de meningite de etiologia não esclarecida" (MENES) utilizada na rotina dos serviços de vigilância. Na segunda categoria, os casos de meningite com características do liquor compatíveis com etiologia viral: celularidade maior do que 10 e menor do que 1.500 células por ml; e presença de linfócitose/ou monócitos em um percentual maior do que 49%. Foram excluídos da segunda categoria os casos sem dados laboratoriais. Os casos com exame bacteriológico positivo (Gram ou cultura de liquor ou sangue) foram descartados em ambas as classificações. Observe-se que as categorias não são excludentes, significando que um caso pode pertencer às duas ou apenas a uma categoria; por isso, os resultados são apresentados separadamente, para cada uma.
Casos de caxumba
Todos os casos registrados no sistema de notificação compulsória de Mato Grosso do Sul em 1998 foram utilizados, já que não existem dados que permitam classificá-los em categorias ou validar o diagnóstico. Dados para MT não estavam disponíveis no momento da análise, ou seja, no ano de 1998.
Análise
Os coeficientes de incidência de meningite foram estimados para cada classificação e para os períodos antes e após as campanhas de vacinação. Para cada período de tempo, o número de casos foi dividido pela estimativa da população de 1 a 11 anos multiplicada pelo número de semanas epidemiológicas (pessoa-tempo). As razões de incidência foram obtidas dividindo-se a incidência para cada período pós-campanha pela incidência pré-campanha. Também foi estimada a diferença de risco (DR), definida como a diferença entre a incidência para cada período pós-campanha e a incidência pré-campanha.
O total de doses foi estimado pelo número da população-alvo da campanha multiplicado pela cobertura vacinal. O número de doses de vacina aplicadas para cada caso de meningite foi estimado assumindo-se que o excesso de casos foi atribuído à vacina, a saber:

As análises foram realizadas utilizando-se o programa estatístico Stata, versão 7.0.4 Intervalos de confiança de 95% foram estimados para as incidências, diferenças e razões de incidência (ver "methods and formulas" em "EPITAB – tables for epidemiologists").4,5
Resultados
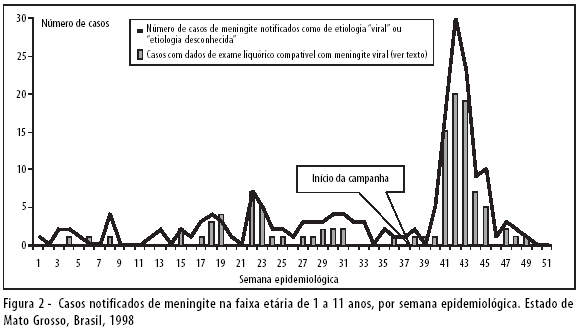
As Figuras 1 e 2 mostram a distribuição de casos de meningite para cada Estado e por semana epidemiológica. Em ambos os Estados, observa-se um aumento da ocorrência de casos de meningite três semanas após a campanha, tanto para casos reportados na ficha de notificação como sendo meningite de etiologia "viral" ou "etiologia desconhecida", como para casos com dados de exame liquórico compatível com meningite viral. No mesmo período, não foi observado qualquer aumento no número de casos com etiologia bacteriana ou no total de casos de meningite em indivíduos com idade acima de 12 anos (dados apresentados na publicação anterior).3
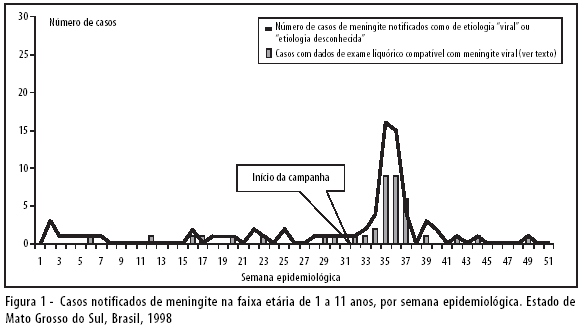
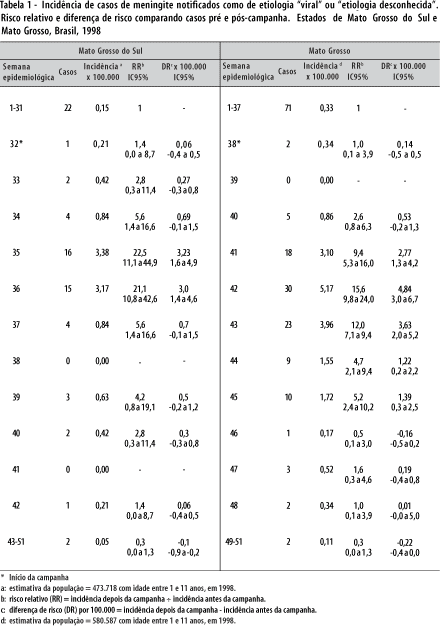
A Tabela 1 mostra as incidências, razões de incidência e diferença de incidência para os casos notificados como meningite de etiologia "viral" ou "etiologia desconhecida" na faixa etária de 1 a 11 anos, por semana epidemiológica, em ambos os Estados. A média de casos por semana, antes da campanha, foi de 0,71 (22 casos divididos por 31 semanas) e 1,9 (71 casos divididos por 37 semanas), respectivamente em Mato Grosso do Sul e Mato Grosso. Foi observado aumento da incidência de meningite a partir da 2a-3a semana após a abertura da campanha de imunização, até a 5a-7a semana. Em Mato Grosso do Sul, a incidência mais elevada ocorre na semana 35 (3a semana pós-campanha), correspondendo a um valor 23 vezes maior, quando comparado ao da incidência média pré-campanha. O aumento persiste até a semana 37, o que significa que o surto perdurou por cerca de quatro semanas (34 a 37). Em Mato Grosso, o aumento de incidência de casos notificados como meningite de etiologia "viral" ou "etiologia desconhecida" torna-se estatisticamente significante a partir da semana 41; e atinge seu pico na semana seguinte (42a), quando a incidência é cerca de 16 vezes maior que a observada anteriormente. O surto perdura até a semana 45 (cerca de cinco semanas).
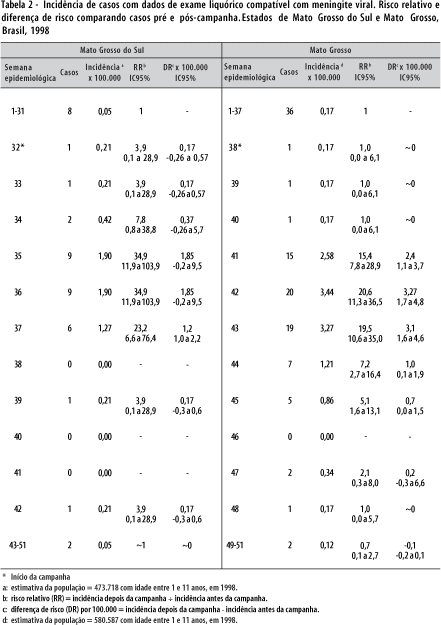
A Tabela 2 mostra as incidências para meningite asséptica pelo critério laboratorial (dados de exame liquórico compatível com meningite viral), por semana epidemiológica, em ambos os Estados. O período de aumento de incidência de meningite e a sua duração são similares aos apresentados na Tabela 1. O pico de incidência foi de 1,9 e 3,4 casos por 100.000 habitantes, respectivamente em Mato Grosso do Sul e Mato Grosso.
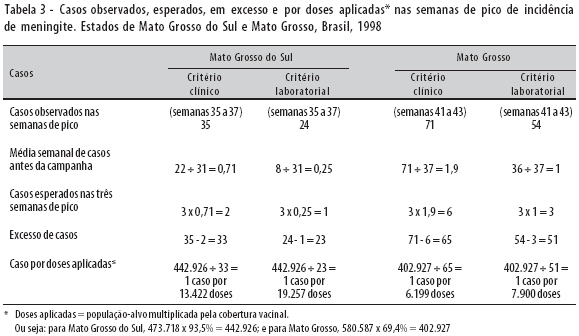
Na Tabela 3, observa-se que a estimativa do número de casos de meningite por doses aplicadas variou de um caso para 6.199 doses a um caso para 7.900 doses em Mato Grosso. Em Mato Grosso do Sul, variou de um caso para 13.422 doses a um caso para 19.257 doses.
A Tabela 4 apresenta a distribuição de casos de caxumba registrados em Mato Grosso do Sul, por semana epidemiológica. Observa-se que o número de casos de caxumba na semana 35 chegou a 884, correspondendo a uma incidência 72 vezes maior que a incidência nas semanas antecedentes à campanha.
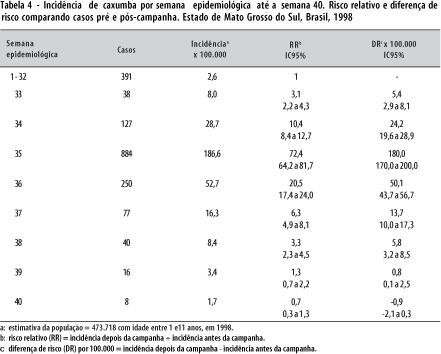
Entre as semanas 1 e 32, antes da campanha, foram registrados 391 casos de caxumba, correspondendo a uma média semanal de 12 casos (391÷32). Entre as semanas 33 e 38, período pós-campanha, foram registrados 1.416 casos, enquanto eram esperados 72 (6 semanas x 12 casos/semana), correspondendo a um excesso de 1.344 casos (1.416 - 72) neste período e a uma estimativa de 1 caso para 313 (442.926 ÷ 1.416) doses aplicadas (IC95%: 297 a 330).
Discussão
Os principais achados do trabalho podem ser sintetizados nos seguintes pontos:
a) existência de surtos de meningite asséptica de provável etiologia viral nos Estados de Mato Grosso e Mato Grosso do Sul, ocorridos cerca de três semanas após o início da campanha de imunização com a vacina tríplice viral;e
b) existência de surto de caxumba no Estado de Mato Grosso do Sul, no mesmo período.
Os dados sugerem que os surtos de meningite e caxumba foram causados pelo uso da vacina TPV durante as campanhas. Uma hipótese alternativa seria que os aumentos de incidência fossem decorrentes da variação sazonal. Entretanto, a incidência nos anos de 1996 e 1997, no Estado de Mato Grosso, não apresentou qualquer padrão sazonal.3 Os dados de meningite em Mato Grosso do Sul anteriores a 1998 não estavam disponíveis no momento da análise. Registros de casos de caxumba anteriores a 1998 estavam disponíveis para esse Estado, e o surto epidêmico, aparentemente, também não correspondeu a qualquer padrão sazonal.3
Outra hipótese alternativa seria a ocorrência de um aumento na incidência de caxumba por vírus selvagem (ou de outra etiologia) concomitante à campanha de vacinação. Entretanto, esse evento significaria dois surtos com características similares em dois Estados diferentes, ademais de restritos à população-alvo das campanhas – um grau de coincidência demasiadamente alto, bastante improvável.
Dois pontos devem ser considerados na interpretação desses resultados. Primeiramente, não se dispõe de dados de anos anteriores para o Estado de Mato Grosso do Sul (antes de 1997) que permitam analisar uma série histórica e estabelecer padrão sazonal ou cíclico de meningite. Tampouco dispõe-se de dados sobre ocorrência de caxumba no Estado de Mato Grosso. Em segundo lugar, não há confirmação laboratorial da etiologia dos casos de meningite. Na prática clínica de rotina, o diagnostico etiológico de meningite viral não é factível pelas dificuldades de isolamento viral. Geralmente, o caso é notificado como "viral" ou "meningite de etiologia indefinida", baseado em informações sobre o quadro do paciente e exame liquórico. No presente estudo, foram utilizados os casos de meningite notificados compatíveis com a definição de síndrome de meningite asséptica adotada na prática médica, ou seja: qualquer caso de meningite usualmente acompanhado de pleiocitose linfocitária e cuja etiologia não é aparente na avaliação clínica e laboratorial inicial.2 Essa definição não é específica, mas julgamos ser um proxi adequado para meningite viral.
A hipótese mais plausível apresentada pelo estudo é de uma relação causal entre o uso da vacina LZ e os surtos de meningite e caxumba observados, fundamentada nos seguintes argumentos:5
a) Magnitude do efeito – razões de incidência elevadas, estatisticamente significantes.
b) Especificidade – não-evidência de evento similar em ano anterior (apenas em Mato Grosso, quanto a meningite; e em Mato Grosso do Sul, quanto a caxumba), e restrita à população-alvo da campanha.3
c) Surtos de curta duração – sugestão de exposição maciça em curto período de tempo, compatível com uma campanha de vacinação.
d) Plausibilidade biológica – ocorrências de caxumba e meningite já descritas como eventos adversos secundários à vacina contra caxumba.6
e) Ocorrência dos surtos 3-4 semanas após o principal dia de vacinação – o que corresponde ao período de incubação descrito para ambos os eventos, posteriormente ao uso da vacina contra caxumba.7,8
Mas, qual é a freqüência de reações adversas provocadas por outras vacinas TPV empregadas no Brasil? Surtos epidêmicos de meningite e caxumba foram observados após as campanhas de vacinação com a vacina TPV no ano de 1997, em diferentes Estados: Bahia, Ceará, Rio Grande do Sul e Piauí. Em Salvador, Bahia,8 um estudo estimou a ocorrência de um caso de meningite asséptica para cada 13.000 doses de vacina aplicadas – todavia, uma freqüência menor que a da meningite decorrente de infecção natural.
As vacinas TPV contendo a cepa LZ foram utilizadas na antiga Iugoslávia, aparentemente com baixa incidência de reações adversas.9 Em uma campanha de vacinação com TPV realizada nas Bahamas em 1997, na qual se utilizou a cepa LZ,10 foi registrado apenas um caso de meningite asséptica para um total de 103.170 pessoas vacinadas com idade entre 4 e 40 anos. Contudo, Tesovic et al publicaram uma carta em 1993, onde estimam o risco para meningite asséptica por essa cepa em cerca de nove casos para 10.000 doses aplicadas.11 No Brasil, uma investigação desenvolvida em 1996 (não publicada) refere que a cepa LZ produz mais casos de caxumba quando comparada a outras cepas (inclusive URABE).7
As estimativas de diferenças de risco sugerem, fortemente, que a incidência de meningite e caxumba atribuída ao uso da vacina é menor que a incidência desses eventos quando causados por infecção natural. Entretanto, mesmo considerando-os como eventos raros, a magnitude das incidências de caxumba e meningite foi suficiente para provocar surtos epidêmicos, potencialmente capazes de abalar a confiança da população nos efeitos das vacinas TPV.
Agradecimentos
O primeiro autor do artigo agradece o apoio da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes) do Ministério da Educação.
Referências bibliográficas
1. Gonzaga MM. Caxumba. In: Tonelli E. Doenças infecciosas na infância. Rio de Janeiro: Editora Médica e Científica; 1987. p.521-528.
2. Tunkell AR, Scheld WM. Acute meningitis. In: Mandell D. Bennett’s principles and practice of infectious diseases - Chapter 71. Philadelphia: Churchill Livingston; 2000. p.959-997.
3. Cunha SC, Rodrigues LC, Barreto LM, Dourado I. Outbreak of aseptic meningitis and mumps after mass vaccination with MMR vaccine using the Leningrad- Zagreb mumps strain. Vaccine 2002;20:1106-1112.
4. StataCorp Stata reference manual: release 7. College Station; 2001.
5. Rothman KJ. Modern epidemiology. Boston: Little, Brown and Company; 1986.
6. Balraj V, Miller E. Complications of mumps vaccine. Reviews in Medical Virology 1995;5:219-227.
7. Boaventura S, Famer S, Ranieri TMS, Bercini MA, Schermann MT, Mohrdieck R, Cardoso EM, Coimbra RMV, Menezes JB, et al. Avaliação de reatogenicidade de três vacinas tríplice viral (sarampo, caxumba, e rubéola). In: IV Congresso Brasileiro de Epidemiologia; 1998 ago 1-5; Rio de Janeiro, Brasil. Rio de Janeiro: Abrasco; 1998.
8. Dourado I, Cunha SC, Teixeira MG, Farrington CP, Melo A, Lucena R, Barreto ML. An Outbreak of aseptic meningitis asociated with MMR mass vaccination campaign: implications for immunization programs. American Journal of Epidemiology 2000;151:1-7.
9. Beck M, Smerdel S, Dedic I, Delimar N, Rajninger Miholic M, Juzbasic M, Manhalter T, Vlatkovic R, Borcic B, et al. Immune response to Edmonston- Zagreb measles virus strain in monovalent and combined MMR vaccine. Developments in Biological Standardization 1986;65:95-100.
10. Panamerican Health Organization. Evaluation of the Bahamas’ MMR campaign. Epi News Letter 1999;21:4-5.
11. Tesovic G, Begovac J, Bace A. Aseptic meningitis after measles, mumps, and rubella vaccine. The Lancet 1993;341(8859):1541.
 Endereço para correspondência:
Endereço para correspondência:
Instituto de Saúde Coletiva/UFBA,
Rua Padre Feijó, 29, 4o andar,
Canela, Salvador-BA.
CEP: 40110-170
E-mail:maines@ufba.br
*Este artigo utiliza a mesma base de dados do estudo previamente publicado em: Cunha SS, Rodrigues LC, Barreto ML, Dourado I. Outbreak of aseptic meningitis and mumps after mass vaccination with MMR vaccine using the Leningrad-Zagreb mumps strain. Vaccine 2002;20:1106-1112. Versão modificada, autorizada pelos editores.
*Estudo apoiado pela Secretaria de Vigilância em Saúde/Ministério da Saúde.











 Curriculum ScienTI
Curriculum ScienTI