Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Epidemiologia e Serviços de Saúde
versión impresa ISSN 1679-4974versión On-line ISSN 2237-9622
Epidemiol. Serv. Saúde v.19 n.2 Brasília jun. 2010
http://dx.doi.org/10.5123/S1679-49742010000200009
Vacinação contra pneumococo em crianças com doença falciforme no Espírito Santo, entre 2004 e 2007
Vaccination against pneumococcus in children with sickle cell anemia in the State of Espirito Santo, Brazil, between 2004 and 2007
Diana de Oliveira FrauchesI; Prisces Amélia dos Santos B. A. MatosII; Juliana Hiromi VatanabeIII; Juliane Falci de OliveiraIII; Ana Paula Neves Burian LimaIV; Sandra Fagundes Moreira-SilvaI
IHospital Infantil Nossa Senhora da Glória, Vitória-ES, Brasil. Escola Superior de Ciências da Santa Casa de Misericórdia de Vitória, Vitória-ES, Brasil
IIHospital Infantil Nossa Senhora da Glória, Vitória-ES, Brasil. Univix Faculdade Brasileira, Vitória-ES, Brasil
IIIHospital Infantil Nossa Senhora da Glória, Vitória-ES, Brasil
IVHospital Infantil Nossa Senhora da Glória, Vitória-ES, Brasil. Centro de Referência para Imunobiológicos Especiais do Espírito Santo, Vitória-ES, Brasil
RESUMO
Doença falciforme cursa com alta vulnerabilidade a infecções, principalmente por bactérias encapsuladas. Este estudo transversal objetivou verificar a vacinação contra Streptococcus pneumoniae em crianças com doença falciforme diagnosticadas entre 2004 e 2007 pelo Serviço de Referência em Triagem Neonatal da Associação de Pais e Amigos dos Excepcionais de Vitória (SRTN-APAE), que pesquisa a hemoglobinopatia em 92% dos nascidos vivos do Espírito Santo. Revisão de prontuários de todas as crianças diagnosticadas e conferência do registro de vacinação do Centro de Referência para Imunobiológicos Especiais (CRIE-ES) mostrou cobertura vacinal de 50%. Vacinação completa predominou entre crianças residentes na Grande Vitória, com mãe de 20 anos ou mais e menor número de irmãos, mas não houve associação entre estas variáveis e cumprimento do esquema. Para aumentar a baixa cobertura vacinal detectada, sugere-se promoção de educação permanente dos profissionais de saúde, descentralização do CRIE-ES, suprimento adequado de imunobiológicos e busca domiciliar de pacientes faltosos.
Palavras-chave: cobertura vacinal; vacinação; Streptococcus pneumoniae; anemia falciforme; doença da hemoglobina S.
SUMMARY
Sickle cell anemia runs with high vulnerability to infections, mainly by encapsuled bacteria. This transversal study had as its objective, the verification of vaccination against Streptococcus pneumoniae in children diagnosed with sickle cell anemia between 2004 and 2005 by the Neonatal Screening Reference Service of the Association of Relatives and Friends of the Handicapped of Vitoria (SRTN-APAE)*, which researches hemaglobin s. disease in 92% of the living newborns in the state of Espirito Santo. Revision of the medical records of all children diagnosed and checking of the vaccination registry of the Reference Centerfor Special Immunobiologics (CRIE-ES) has shown vaccinal coverage of 50%. Complete vaccination was predominant among children residing in the Great Victoria area, whose mothers were twenty years or older and with a lesser number of siblings, but there was no association between these variables and the carrying out of the plan. To increase the low vaccinal coverage detected, the promotion of permanent education of health professionals and the decentralization of the CRIE-ES, and adequate supply of immunobiologicals and home visits to patients who fail to attend is suggested.
Key words: immunization coverage; vaccination; Streptococcus pneumoniae; anemia, sickle cell; hemoglobin S disease.
Introdução
A doença falciforme é decorrente de uma alteração gênica que leva à produção da hemoglobina S. Em condições de hipóxia, as hemácias assumem forma semelhante a uma foice devido à polimerização desta hemoglobina e, por não circularem adequadamente, ocorre vaso-oclusão, seguida de isquemia nos diversos tecidos e órgãos, bem como hemólise crônica e seus mecanismos compensadores.1-4
No Brasil, a distribuição da hemoglobina S é bastante heterogênea.2,5,6 Dados do Programa Nacional de Triagem Neonatal (PNTN), instituído pelo Ministério da Saúde em 2001, indicam proporções de recém-nascidos diagnosticados com doença falciforme variando de um caso para 650 nascidos vivos, na Bahia, até um para 13.000, em Santa Catarina, sendo que, no Espírito Santo, situa-se em um para 1.800.6
As principais causas de vulnerabilidade de pacientes com doença falciforme a infecções são a disfunção esplênica e a hipóxia tecidual.2,4 A disfunção esplênica é causada por trombose e enfarto decorrentes da vaso-oclusão, evoluindo para atrofia e fibrose do órgão, em um processo que começa já na primeira infância e é denominado auto-esplenectomia. Além das alterações estruturais, ocorre diminuição da opsonização pela menor síntese de opsoninas e pela alteração das vias do sistema complemento, levando à fagocitose e à morte intracelular ineficazes, principalmente para bactérias encapsuladas.1-3
Nos EUA, o risco de infecção por Streptococcus pneumoniae em crianças com anemia falciforme é 30 a 100 vezes maior para bacteremia e 400 vezes maior para sepse ou meningite.4 A gravidade das infecções justificou a adoção, como rotina para os pacientes falcêmicos, de quimioprofilaxia com penicilina a partir dos três a quatro meses até os cinco anos de idade, sendo, no Brasil, mais empregada penicilina benzatina, a cada 21 dias, ou, em caso de alergia a este antibiótico, eritromicina.4
As dificuldades de manutenção do esquema profilático e o aumento da resistência à penicilina tornam fundamental investir na prevenção primária contra o pneumococo, por meio de vacinação específica.7,8 Embora em pacientes com anemia falciforme a resposta imune seja prejudicada pela deficiência de células B circulantes devido à asplenia funcional, esta alteração ocorre em um processo que se desenvolve a partir do primeiro ano de vida, consolidando-se por volta dos seis aos oito anos de idade3 e atingindo 94% das crianças aos cinco anos de idade,4 o que reforça a necessidade de vacinação precoce.1-3
Existem atualmente dois tipos de vacina contra pneumococo disponíveis no Brasil:7
1) Vacina 23-valente (Pn23), que contém 23 sorotipos de pneumococo, incluindo cerca de 80% dos sorotipos causadores de doença invasiva no Brasil e induz resposta imunológica T-independente de curta duração, principalmente em imunodeprimidos, variável com os sorotipos de pneumococo. A vacina protege 80% das crianças e dos adultos jovens, mas não é efetiva em menores de dois anos de idade. É indicada para administração a partir desta idade, em dose única, com reforço após cinco anos.
2) Vacina 7-valente conjugada (Pnc7), com sete sorotipos responsáveis por até 70% das doenças invasivas no Brasil. A resposta imunológica é T-dependente, mais duradoura e precoce, protegendo mais de 90% das crianças hígidas contra os sete sorotipos. É recomendada a partir dos dois meses de idade, em esquema básico de três doses, quando iniciada antes dos sete meses, ou de duas doses, após esta idade.
A utilização de Pnc7, assim como de outras vacinas conjugadas, possibilita a vacinação precoce contra pneumococo e, quando o esquema é complementado com Pn23, amplia-se o espectro de proteção contra o agente4 e aumenta-se a resposta imune.8,9
Paralelamente, há evidências de alta efetividade de vacinas conjugadas contra pneumococo em pacientes com doença falciforme9 e sua introdução no esquema vacinal de crianças desta população produziu redução significativa na ocorrência de doença invasiva pelo agente em pacientes menores de dez anos, nos EUA.8
No Brasil, Pn23 e Pnc7 são disponibilizadas gratuitamente nos Centros de Referência para Imunobiológicos Especiais (CRIEs).7 A norma técnica do Ministério da Saúde prevê a administração destas vacinas em esquema definido segundo a idade do paciente (Figura 1),7 sendo que, em 2006, a faixa etária para utilização de Pnc7 foi ampliada de seis a 24 meses de idade para de dois meses a cinco anos.10

Os CRIEs foram criados em 1993 pelo Ministério da Saúde e destinamse ao atendimento de pessoas portadoras de quadros clínicos que aumentam sua susceptibilidade a infecções, bem como àquelas detentoras de condições que condicionam risco de complicação para si ou para outros em virtude de motivo biológico, por convívio com pessoas imunodeprimidas, intolerância aos imunobiológicos comuns, exposição inadvertida a agentes infecciosos, motivos profissionais ou violência contra a pessoa.7
No Espírito Santo, o único CRIE (CRIE-ES) está localizado no Hospital Infantil Nossa Senhora da Glória (HINSG), em Vitória-ES.11 Em decorrência da indicação de vacina contra pneumococo e outros imunobiológicos especiais para pessoas com asplenia anatômica ou funcional, atende grande número de pacientes com doença falciforme, muitos encaminhados pelo Serviço de Referência em Triagem Neonatal da Associação de Pais e Amigos dos Excepcionais de Vitória (SRTN-APAE).
Este serviço é o único cadastrado pelo PNTN do Ministério da Saúde, no estado. Realiza busca ativa da hemoglobinopatia em recém-nascidos de todos os municípios, tendo examinado, entre 2004 e 2007, 188.642 dos 204.664 nascidos vivos de mães residentes no Espírito Santo, registrados no Sistema Nacional de Informações sobre Nascidos Vivos (92,17%). É composto por rede de coleta de exames, laboratório, sistema de busca domiciliar dos pacientes com exames alterados e ambulatório multidisciplinar para atendimento aos pacientes.12
Considerando a abrangência do SRTN-APAE no Espírito Santo, esta pesquisa teve como objetivo verificar a situação vacinal contra pneumococo nas crianças com doença falciforme diagnosticadas no serviço, para estimar, em nível do estado, a cobertura da vacina contra pneumococo neste grupo populacional susceptível.
Metodologia
Foi realizado estudo transversal no qual todas as 106 crianças diagnosticadas com doença falciforme no SRTN-APAE entre 2004 e 2007 foram identificadas no cadastro do serviço, que disponibilizou os prontuários para coleta dos dados objeto da pesquisa. Posteriormente, utilizou-se o nome de cada criança e de sua mãe para busca no arquivo do CRIE-ES, visando a conferência e a complementação de informações sobre vacinação.
Doença falciforme foi definida como a presença da hemoglobina S em homozigose ou em associação com outras hemoglobinas anormais, de acordo com os critérios adotados no SRTN-APAE, excluídos os portadores de traço falciforme.
A situação vacinal das crianças em relação ao pneumococo foi tomada como variável efeito. Considerou-se com esquema completo a criança que, respeitada a idade, completou o protocolo preconizado pelo Ministério da Saúde (Figura 1).7 Com esquema incompleto foi classificada a criança que iniciou o protocolo, porém não recebeu a(s) dose(s) subsequente (s), inclusive reforço, e não vacinada, a criança que não recebeu vacina ou não possuía registro de vacinação na documentação consultada. Com base nisto, definiu-se como situação vacinal adequada, a das crianças com esquema completo, sendo inadequada a das crianças com esquema incompleto ou sem vacinação.
Como variáveis causais foram exploradas:
1) Município de residência: agrupado em Grande Vitória (correspondente à região metropolitana da capital, incluindo Cariacica, Fundão, Guarapari, Serra, Viana, Vila Velha e Vitória) e interior (demais municípios do estado), admitindo-se que a distância do CRIE-ES ao interior pudesse dificultar o cumprimento do esquema vacinal.
2) Idade da mãe: categorizada em até 19 anos e 20 anos ou mais, considerada adolescência como fator de risco para não cumprimento do esquema vacinal;
3) Número de irmãos: 0 a 2 e 3 a 6, esperando-se que o maior número de irmãos acarretasse prejuízo na adesão ao esquema vacinal.
Também foram estudados dados sobre raça/cor, gênero, idade de início do esquema de vacinação e vacina administrada.
Tomou-se como cobertura vacinal a proporção de crianças com vacinação adequada, entre as crianças estudadas, e como proporção de abandono, o número de crianças com esquema incompleto, entre as crianças que iniciaram o esquema.
Utilizou-se distribuição de frequências para análise descritiva das variáveis. Teste qui-quadrado de Pearson bi-caudal, em nível de significância de 0,05, e odds ratio foram empregados para verificar a associação entre as variáveis de interesse.
Considerações éticas
O estudo foi aprovado pelo Comitê de Ética em Pesquisa do Hospital Infantil Nossa Senhora da Glória (HINSG) (registro 31/2008). Os pesquisadores firmaram termo de responsabilidade de utilização de dados, pois não houve contato direto com os pacientes ou responsáveis para obtenção do consentimento livre e esclarecido.
Resultados
Entre 2004 e 2007, o SRTN-APAE realizou exames de triagem neonatal em 92,17%, em média, dos 204.664 nascidos vivos do Espírito Santo (Tabela 1). Com esta cobertura e considerando a proporção de um caso para 1.800 nascidos vivos,6 seria esperada a detecção de 105 crianças com doença falciforme no período.
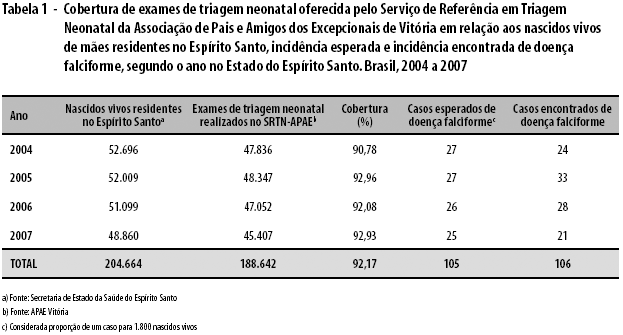
As 106 crianças que foram diagnosticadas e constituem objeto desta pesquisa eram principalmente brancas (81,90%), com ligeiro predomínio do sexo masculino (51,89%), sendo que somente 50% apresentaram esquema vacinal completo contra pneumococo (Tabela 2).

A proporção de abandono (número de crianças com esquema incompleto no total de crianças que iniciaram o esquema), mostrou-se maior nas crianças residentes no interior, com mães de até 19 anos e com maior número de irmãos (Tabela 3).
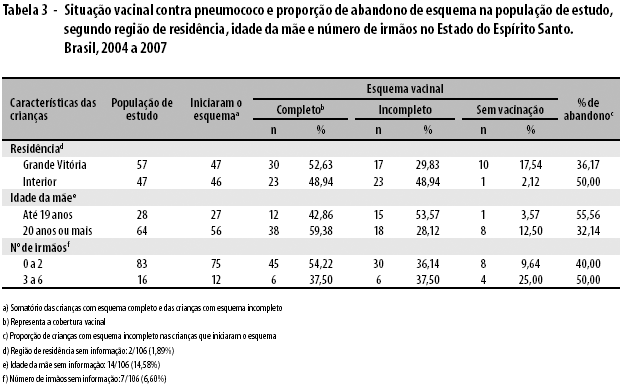
Ao mesmo tempo, a cobertura vacinal (proporção de crianças com esquema vacinal completo no total de crianças estudadas) foi maior entre as crianças residentes na Grande Vitória, com mãe de 20 anos ou mais e com menor número de irmãos (Tabela 3).
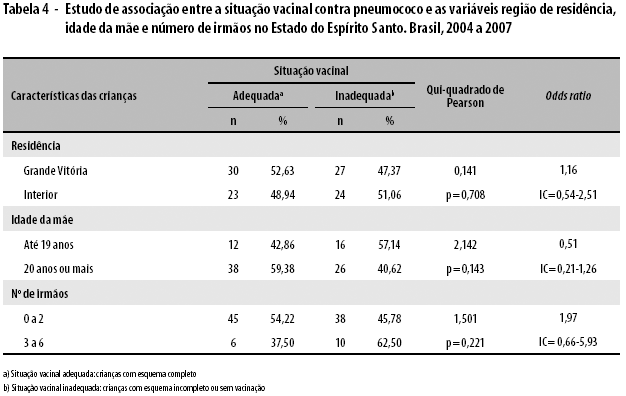
No entanto, a região de residência, a idade materna e o número de irmãos não influenciaram significativamente a situação vacinal das crianças quando esta situação foi categorizada em adequada ou inadequada, este último grupo sendo formado pelas crianças com esquema vacinal incompleto e pelas não vacinadas (Tabela 4).
Entre as 93 crianças que pelo menos iniciaram vacinação, 74,15% o fizeram entre dois a seis meses de idade. As demais, tiveram início tardio do esquema: 16,13% entre sete a 11 meses e idade; 5,38%, entre um e dois anos; e 4,30%, após os dois anos.
Foi utilizada Pnc7 na vacinação destas 93 crianças, porém três delas, nascidas em 2004, usaram também Pn23, aplicada após os dois anos de idade, na sequência de esquemas iniciados no primeiro ano de vida e nos quais houve falhas de intervalo e de número de doses.
Discussão
O grande percentual dos nascidos vivos do Espírito Santo nos quais o SRTN-APAE realiza triagem neonatal para hemoglobinopatias possibilita estimar a incidência de doença falciforme no estado, na população alvo do programa, com razoável confiabilidade.
Nesta perspectiva, cabe discutir alguns aspectos em relação à distribuição das crianças estudadas segundo características demográficas.
Sabe-se que a prevalência da doença falciforme na população negra é maior do que na população branca, o que não foi observado na presente pesquisa, talvez pelo fato de que, nos prontuários utilizados como fonte de dados, raça/cor é uma classificação em geral autoatribuída e de caráter subjetivo. No entanto, é preciso registrar a possível interferência da expressiva quantidade de brancos existente na população residente no Espírito Santo - sete vezes maior que a de negros, segundo o censo do Instituto Brasileiro de Geografia e Estatística (IBGE) de 2000.13
Outra característica da população do estado, que concentrava, em 2007, 48,47% de seus habitantes na região da Grande Vitória, pode explicar o predomínio desta região como local de residência das crianças.14
Por outro lado, como a população de estudo tem tamanho comparável à incidência esperada de doença falciforme entre os nascidos vivos do Espírito Santo, estima-se que a cobertura vacinal contra pneumococo existente nesse grupo populacional seja semelhante à encontrada nesta pesquisa.
Ressalva-se, como limitação quanto ao método utilizado na presente pesquisa, o fato de não se ter realizado inquérito domiciliar para leitura dos cartões de vacinação, visando obter classificação adequada de crianças que eventualmente foram vacinadas em clínicas particulares ou em outros estados, bem como corrigir erros de registro.15-17
As dificuldades operacionais inerentes à realização de inquéritos domiciliares justificam a realização de levantamento de registros rotineiros,18 como o prontuário do paciente, que, neste estudo, foi ainda confrontado com o registro de vacinação arquivado no CRIE-ES, em uma estratégia que certamente aumentou a confiabilidade da fonte.
Considerando a limitação acima descrita, o esquema vacinal completo, condição que define cobertura vacinal, foi observado em 50% das crianças estudadas. Ainda que possa estar subestimada em função de eventuais falhas relacionadas às fontes de dados utilizadas, tal proporção indica que existem, no estado, muitas crianças com doença falciforme desprotegidas contra pneumococo e, portanto, uma baixa cobertura vacinal.
A não vacinação ou a não conclusão de esquemas vacinais podem ser justificadas, entre outros, por fatores como esquecimento, dificuldade na percepção da doença, medo de reação vacinal, desconhecimento da vacina e medo do procedimento, questões que não foram abordadas nesta pesquisa.16,17,19
Da mesma forma, esta pesquisa não investigou que impacto causaria sobre a vacinação a ocorrência de eventos como as internações, mais frequentes nas crianças com doença falciforme do que na população geral,20 nem a interferência da mortalidade, que chega a 0,59 óbitos por 100 pacientes-ano.21
Também não foram estudados problemas relacionados ao serviço de saúde e aos produtos ali disponibilizados.15,16,19 Por exemplo, o horário de funcionamento do CRIE-ES, de 7 às 16 horas em dias úteis, bem como eventuais períodos de falta de imunobiológico, podem ter contribuído para os resultados observados.
Explorou-se nesta pesquisa, especificamente, a distância existente entre o local de residência e o serviço, bem como a idade materna e o número de irmãos, fatores que também podem interferir no cumprimento dos esquemas vacinais.16,17 Não se encontrou diferença significativa entre os grupos de comparação nestas variáveis, embora a proporção de crianças com esquema de vacinação completo, ou seja, adequadamente vacinadas, tenha se mostrado maior nas residentes na Grande Vitória, com mãe de 20 anos ou mais e com menor número de irmãos.
A alta proporção de crianças não vacinadas, das que iniciaram tardiamente o esquema e daquelas que não o completaram permitem levantar a hipótese de que não tenha sido realizada ou que tenha ocorrido falha na busca domiciliar dos pacientes, a qual seria da responsabilidade inicial do SRTN-APAE ou, em caso de interrupção de esquema, do CRIE-ES.
A vulnerabilidade dos pacientes com doença falciforme ao S. pneumoniae e os efeitos daí decorrentes no aumento da morbimortalidade, a possibilidade de obtenção de proteção precoce e efetiva contra este bioagente patogênico nesta população cuja resposta imune fica mais prejudicada com o aumento da idade e a disponibilidade de vacina no serviço público de saúde tornam importante a realização de ações concretas para garantir alta cobertura vacinal específica o mais cedo possível a partir do momento em que ocorre o diagnóstico da hemoglobinopatia.
Acredita-se que é fundamental promover a educação permanente dos profissionais de saúde, que são os grandes responsáveis pela indicação, prescrição e administração de vacinas, bem como pela orientação aos pais sobre a importância do cumprimento dos esquemas vacinais. Além disso, descentralizar o CRIE-ES, disponibilizar suprimento adequado de imunobiológicos e ampliar o horário de funcionamento do serviço poderiam beneficiar os pacientes. Ainda se faz necessário investir na vigilância e busca domiciliar de pacientes, no registro correto de dados e no aprofundamento de estudos sobre cobertura vacinal contra pneumococo nas crianças com doença falciforme.
Adicionalmente, registra-se que a administração de Pn23 em três crianças de dois anos de idade ocorreu em 2006, quando a recomendação para o uso da vacina Pnc7 nos CRIE's foi ampliada dos dois aos cinco anos.10 É possível que isto represente uma falha transitória relacionada à capacitação imediata de pessoal sobre as novas normas que entravam em vigor naquela época.
Agradecimentos
Às equipes do SRTN-APAE e do CRIE-ES, por sua dedicação e compromisso com a busca contínua da qualidade nos serviços de saúde.
Referências
1. Ministério da Saúde, Secretaria de Atenção à Saúde. Manual de condutas básicas na anemia falciforme. Brasília: MS; 2006.
2. Di Nuzzo DVP, Fonseca SF. Anemia falciforme e infecções. Jornal de Pediatria 2004;80:347-354.
3. Loggetto SR, Pellegrini-Braga JA, Costa-Carvalho BT, Solé D. Alterações imunológicas em pacientes com anemia falciforme. Revista Brasileira de Hematologia e Hemoterapia 2007;29(3):233-238.
4. Braga JAP. Medidas gerais no tratamento das doenças falciformes. Revista Brasileira de Alergia e Imunopatologia 1999;22(3):77-82.
5. Cançado RD, Jesus JA. A doença falciforme no Brasil. Revista Brasileira de Hematologia e Hemoterapia 2007;29(3):203-206.
6. Ministério da Saúde. Doença falciforme e outras hemoglobinopatias [Internet]. Brasília: MS [acessado durante o ano de 2008]. Disponível em: http://portal.saude.gov.br/portal/saude/visualizar_texto.cfm?idtxt=27777&janela=1.
7. Ministério da Saúde, Secretaria de Vigilância em Saúde. Manual dos centros de referência para imunobiológicos especiais. Brasília: MS; 2006.
8. Adamkiewicz TV, Silk BJ, Howgate J, Baughman W, Strayhorn G, Sullivan K, et al. Effectiveness of the 7-valent pneumococcal conjugate vaccine in children with sickle cell disease in the first decade of life. Pediatrics 2008;121(3);562-569.
9. Davies EG, Hirst C, Lottenberg R, Dower N. Pneumococcal vaccines for sickle cell disease. Cochrane Database of Systematic Reviews 2009;(3):CD003885.
10. Bricks LF. Novas recomendações para vacinação nos Centros de Referência de Imunobiológicos Especiais (Cries). Pediatria (São Paulo) 2006;28(3):204-208.
11. Secretaria Estadual de Saúde do Espírito Santo. Histórico do programa de imunizações [Internet]. Vitória: SES [acessado durante o ano de 2008]. Disponível em: http://www.saude.es.gov.br/default.asp
12. Associação de Pais e Amigos dos Excepcionais de Vitória. CEDAB: Centro de Diagnóstico Dr. Américo Buaiz [Internet]. Vitória: APAE [acessado durante o ano de 2008]. Disponível em: http://www.apaevitoria.org.br/centro_de_diagnostico.asp
13. Instituto Brasileiro de Geografia e Estatística. Censo demográfico 2000 [Internet]. Rio de Janeiro: IBGE; 2000 [acessado durante o ano de 2008]. Disponível em: http://www.ibge.gov.br/home/estatistica/populacao/tendencia_demografica/analise_populacao/1940_2000/tabela07.pdf.
14. Ministério da Saúde. População estimada segundo município [Internet]. Brasília: MS [acessado durante o ano de 2008 para informações de 2007]. Disponível em: http://tabnet.datasus.gov.br/cgi/tabcgi.exe?ibge/cnv/poptES.def.
15. Moraes JC, Ribeiro MCSA. Desigualdades sociais e cobertura vacinal: uso de inquéritos domiciliares. Revista Brasileira de Epidemiologia 2008;11 Supl 1:113-124.
16. Gatti MAN, Oliveira LR. Crianças faltosas à vacinação, condições de vida da família e concepção sobre vacina: um inquérito domiciliar. Salusvita 2005;24(3):427-436.
17. Silva AAM, Gomes UA, Tonial SR, Silva RA. Cobertura vacinal e fatores de risco associados à não vacinação em localidade urbana no nordeste brasileiro, 1994. Revista de Saúde Pública 1999;33(2):147-156.
18. Pereira MG. Epidemiologia: teoria e prática. Rio de Janeiro: Guanabara Koogan; 1995.
19. Silva LMV, Formigli VL, Cerqueira MP, Kruchevsky L. Coberturas vacinais superestimadas? Novas evidências a partir do inquérito de Pau de Lima. Revista Panamericana de Salud Publica 1997;1(6):444-450.
20. Raphael JL, Dietrich CL, Whitmire D, Mahoney DH, Mueller BU, Giardino AP. Healthcare utilization and expenditures for low income children with sickle cell disease. Pediatric Blood Cancer 2009;52(2):263-267.
21. Quinn CT, Rogers ZR, Buchanan GR. Survival of children with sickle cell disease. Blood 2004;103(11):4023-4027.
 Endereço para correspondência:
Endereço para correspondência:
Hospital Infantil Nossa Senhora da Glória,
Núcleo Hospitalar de Epidemiologia,
Alameda Mary Ubirajara, 205, Santa Lúcia,
Vitória-ES, Brasil.
CEP:29050-010
E-mail:diana@ebrnet.com.br
Recebido em 29/04/2009
Aprovado em 13/09/2009