Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Epidemiologia e Serviços de Saúde
Print version ISSN 1679-4974On-line version ISSN 2237-9622
Epidemiol. Serv. Saúde vol.21 no.4 Brasília Dec. 2012
http://dx.doi.org/10.5123/S1679-49742012000400010
ARTIGO ORIGINAL
Prevalência de marcadores sorológicos do vírus da hepatite B em profissionais de saúde de um laboratório de pesquisa na Amazônia oriental, Estado do Pará, Brasil, 2007 a 2009*
Prevalence of serological markers of hepatitis B virus in health professionals from a research laboratory in the eastern Amazon, State of Pará, Brazil, 2007 to 2009
Candida Maria Abrahão de Oliveira; Márcio Roberto Teixeira Nunes; Heloisa Marceliano Nunes; Manoel do Carmo Pereira Soares
Instituto Evandro Chagas, Secretaria de Vigilância em Saúde, Ministério da Saúde, Belém-PA, Brasil
RESUMO
OBJETIVO: determinar a prevalência dos marcadores sorológicos da infecção pelo vírus da hepatite B (VHB) entre trabalhadores de um instituto de pesquisas na Amazônia oriental, estado do Pará, Brasil.
MÉTODOS: estudo descritivo, desenvolvido entre 2007 e 2009, com trabalhadores que concordaram em participar mediante entrevista e investigação dos marcadores sorológicos da hepatite B, por técnicas imunoenzimáticas.
RESULTADOS: entre 528 trabalhadores pesquisados, encontrou-se prevalência de 0,4% do antígeno de superfície do VHB, 8,0% anticorpos contra o antígeno core do VHB/anticorpos contra o antígeno de superfície do VHB, 2,5% anticorpos contra o antígeno core do VHB isolado e 28,8% anticorpos contra o antígeno de superfície do VHB isolado, entre 68,4% de suscetíveis ao VHB que correspondiam aos indivíduos não vacinados.
CONCLUSÃO: identificou-se prevalência e soroconversão inadequadas, abaixo da média informada pelo Ministério da Saúde, em que três doses da vacina devem conferir proteção de aproximadamente 90,0% em adultos.
Palavras-chave: Hepatite B; Prevalência; Profissionais da Saúde; Vacinação; Epidemiologia Descritiva.
ABSTRACT
OBJECTIVE: to determine the prevalence of serological markers of infection by hepatitis B virus (HBV) among workers at a research institute in eastern Amazon, state of Pará, Brazil.
METHODS: descriptive study, carried between 2007 and 2009, with workers who agreed to participate through interview and investigation of serological markers of hepatitis B by immu-noenzymatic techniques.
RESULTS: among 528 individuals surveyed, was found the prevalence of 0,4% of surface antigen of HBV, 8.0% of antibodies against hepatitis B core antigen/antibody against the surface antigen of VHB, 2.5% antibodies against hepatitis B core isolated antigen and 28.8% antibodies against surface antigen of isolated HBV, 68.4% susceptible to HBV that corresponded to non-vaccinated individuals.
CONCLUSION: the research identified inadequate prevalence of seroconversion below the average reported by the Ministry of Health, in which three doses of the vaccine should confer protection of approximately 90.0% in adults.
Key words: Hepatitis B; Prevalence; Health Personnel; Vaccination; Epidemiology, Descriptive.
Introdução
A hepatite B - causada pelo vírus da hepatite B (VHB) - é uma infecção potencialmente grave e transmissível. Segundo a Organização Mundial da Saúde (OMS), cerca de dois bilhões de pessoas já foram infectadas pelo vírus, o que corresponde a 30,0% da população do planeta. São aproximados 350 milhões de portadores crônicos do vírus no mundo, e um a dois milhões de mortes atribuídas à doença, a cada ano. Mesmo sendo uma doença imunoprevenível, a hepatite B continua a ser um sério problema de Saúde Pública.1
A Norma Regulamentadora no 32/2008, do Ministério do Trabalho e Emprego, estabeleceu as diretrizes básicas para a implementação de medidas de proteção à segurança e à saúde dos trabalhadores em serviço de saúde.2
Estudo de Olkner mostrou que o risco de infecção pelo VHB adquirida ocupacionalmente representava 4,0% do total de casos e que a transmissão do VHB poderia ocorrer por meio de um único episódio de exposição.3
Bonanni e Bonaccorsi, em seu trabalho 'Vaccination against hepatitis B in health care workers', afirmaram que a hepatite B é a doença ocupacional infecciosa mais importante para os trabalhadores da Saúde.4
A cobertura vacinal contra a hepatite B em trabalhadores da área da Saúde, em diferentes países, é bastante variável. Estudo transversal realizado na Suécia, envolvendo trabalhadores de um hospital universitário, detectou que apenas 40,0% dos avaliados teriam completado o esquema vacinal.5 Pesquisa em Rotterdam, Holanda, com 144 trabalhadores extra-hospitalares que haviam sofrido lesões percutâneas e exposição ocupacional a sangue, mostrou que 65,0% deles estavam vacinados contra hepatite B e que a maior ocorrência de vacinação era entre os enfermeiros (81,0%), outros trabalhadores (79,0%) e auxiliares de enfermagem (53,0%).6
No Hospital de Base de São José do Rio Preto-SP, obteve-se prevalência de 73,5% vacinados contra a hepatite B. No Rio de Janeiro, estudo com 298 trabalhadores da Saúde mostrou prevalência de vacinação contra a hepatite B de 56,0%.7,8
No Brasil, entre os casos confirmados de hepatite B, 0,4% (308/81.443) foram considerados ocupacionais, conforme dados do Sistema de Informação de Agravos de Notificação (Sinan) para o período de 1999 a 2008.9
Estudos sobre o assunto, realizados no Rio de Janeiro em 1999 e em São José do Rio Preto-SP em 2005, referiam-se exclusivamente a programas realizados de forma individualizada, em hospitais universitários e outros serviços de saúde.10
Bensabath e Soares, em estudos conduzidos na Amazônia oriental, mostraram prevalência de antígeno de superfície do vírus B (HBsAg) variando de 0,0 a 2,7%; e de anticorpo contra o antígeno de superfície do vírus B (anti-HBs), entre 6,7 e 13,8%.11,12
Existe, portanto, a necessidade de sensibilizar os profissionais da área da Saúde sobre a importância da vacinação contra a hepatite B como medida pontual a ser posta em prática. Ressalta-se, também, a utilização de técnicas de proteção individual (precauções básicas de isolamento, prevenção de acidentes com materiais perfurocortantes, uso de equipamentos de proteção individual e coletivos) como forma de minimizar os riscos de contrair doenças infecciosas, por exemplo, na exposição a sangue e fluídos orgânicos a que esses profissionais estão sujeitos quando realizam pesquisas de campo. Especialmente na Amazônia, área endêmica para a hepatite B.13
Marcadores sorológicos disponíveis podem ser utilizados para diagnóstico de hepatite B aguda ou crônica, acompanhamento dos pacientes e indicação e monitorização do tratamento. São eles:
a) HBsAg (antígeno de superfície do vírus B), cuja presença indica infecção em curso; sendo o primeiro marcador a aparecer, se continuar presente por mais de seis meses, caracteriza infecção crônica;
b) anti-HBcIgM (anticorpo IgM contra o antígeno core do vírus B), cuja presença indica infecção aguda; é o primeiro anticorpo detectável, encontrado no soro até 32 semanas após a infecção;
c) anti-HBcIgG (anticorpos contra o antígeno do núcleo do VHB), é o marcador que indica contato prévio com o vírus, permanecendo por toda a vida nos indivíduos que tiveram a infecção;
d) anti-HBc total (anticorpos totais contra o antígeno core do vírus B), melhor marcador de exposição ao vírus, indica contato prévio com o vírus;
e) HBeAg (antígeno 'e' do vírus B), marcador de replicação viral, sua positividade é indicativa de alta infectividade;
f) anti-HBe (anticorpo contra o antígeno "e" do vírus B), detectado geralmente após o desaparecimento do HBeAg, sugere redução ou ausência de replicação viral - exceção para as cepas que sofreram mutação pré-core, não produtoras da proteína 'e' -; e
g) anti-HBs (anticorpo contra o antígeno de superfície do vírus B), protetor e neutralizante; aparece, geralmente, quando desaparece o HBsAg, indicando resolução da infecção e imunidade; encontrado isoladamente, em pessoas vacinadas.14
A presente pesquisa objetivou determinar a prevalência dos marcadores sorológicos da infecção pelo VHB, HBsAg, anti-HBs e anti-HBc total entre trabalhadores de diferentes categorias em um instituto de pesquisas, por meio de estudo descritivo e epidemiológico.
Métodos
Esta pesquisa foi desenvolvida no período de janeiro de 2007 a janeiro de 2009. As coletas de material foram realizadas entre os meses de janeiro e abril de 2008, nos campi I e II do Instituto Evandro Chagas, localizados respectivamente nos municípios de Belém e Ananindeua, estado do Pará, Brasil. O instituto, vinculado à Secretaria de Vigilância em Saúde do Ministério da Saúde (IEC/SVS/MS), atua nas áreas de pesquisas biomédicas e na prestação de serviços em Saúde Pública. À época da coleta de dados, havia 833 trabalhadores na instituição.
O estudo incluiu trabalhadores do IEC/SVS/MS efetivos, contratados, terceirizados, estagiários e outros que concordaram em participar, independentemente do estado vacinal contra a hepatite B, todos avaliados segundo a faixa etária, sexo, escolaridade e local de trabalho por meio da busca ativa nos serviços, seções e setores, e segundo critérios de inclusão e exclusão acima descritos. A coleta de dados foi realizada mediante entrevistas, com aplicação de Ficha de Inquérito Individual pela autora principal.
A metodologia não inclui a investigação do tempo entre a 3a dose da vacina e a coleta do sangue para exame da situação sorológica.
As fontes de consulta para avaliação do estado vacinal foram: banco de dados, alimentado pelo modelo 'Cadastro Individual do Trabalhador'; aplicação de Ficha de Inquérito Individual, em que se verificou a presença de indivíduos vacinados e/ou com resposta sorológica prévia, por haverem participado de outros projetos de avaliação de resposta vacinai; e entrevista, ocasião quando os que dispunham do cartão de vacinação o apresentaram. Para aqueles que não possuíam o documento, foi realizada a busca da situação vacinal nas fontes citadas (banco de dados) e providenciada a confecção e preenchimento do cartão conforme preconizado pelo Programa Nacional de Imunização.
A coleta, o processamento e os kits utilizados na realização das sorologias para a pesquisa seguiram o estabelecido pelo Laboratório da Seção de Hepatologia do Instituto Evandro Chagas, referência em hepatites virais para a região Norte.
A média de tempo entre a coleta e a realização dos exames foi de cerca de 7,5 meses, durante os quais o material permaneceu acondicionado de maneira adequada.
De cada participante da pesquisa, coletou-se aproximadamente 8mL de sangue, por meio de punção venosa utilizando agulha e tubo vacutainer siliconizado, com separador inerte e ativado não contendo anticoagulante. O material, após identificação nominal e numérica, permaneceu em repouso de 1 a 3 horas, à temperatura ambiente, para retração do coágulo; em seguida, foi centrifugado por 15 minutos, a 3.000 rotações por minuto. Os soros obtidos foram acondicionados em criotubos (tubo KMA, de 3mL), refrigerados em gelo comum e posteriormente congelados a -20oC, até a realização dos exames.
No laboratório de sorologia, realizaram-se os testes de marcadores sorológicos da hepatite B, por técnica imunoenzimática do tipo Enzyme Linked Immunosorbent Assay (ELISA), utilizando kits comerciais. Todas as amostras foram examinadas para a presença de HBsAg (Hepanostika HBsAg Ultra, Biomérieux®, anti-HBc total (Hepanostika anti-HBc Uni-Form, Biomérieux® e anti-HBs (ETI-AB-AUK-3, Diasorin®, segundo as recomendações do fabricante. Os resultados foram considerados duvidosos quando a densidade óptica ficou situada entre 20,0% para cima ou para baixo do limite de corte, levando a nova coleta e repetição do teste.
Os dados obtidos e os resultados dos testes foram armazenados em base de dados, pelo programa Epi Info 2002, versão 3.3. As análises estatísticas foram realizadas pelo programa BioEstat, versão 5.0;15 e as proporções foram avaliadas pelo teste não paramétrico qui-quadrado, para amostras esperadas iguais, sendo estabelecido o nível de significância igual a 0,05.
Com base na Resolução CNS no 196/1996,16 do Conselho Nacional de Saúde, que normaliza as pesquisas envolvendo seres humanos no país, os trabalhadores do IEC/SVS/MS concordaram em participar do estudo mediante assinatura de Termo de Consentimento Livre e Esclarecido e o projeto do estudo foi aprovado por um Comitê de Ética em Pesquisa envolvendo seres humanos, mediante o Certificado de Apresentação para Apreciação Ética (CAAE) no 0029.0.072.000-07, em 19 de dezembro de 2007.
Resultados
Foram examinados (528/833) indivíduos, o que correspondeu a 63,4% do total de trabalhadores da instituição cadastrados no Serviço de Recursos Humanos até dezembro de 2007; 36,6% não concordaram em participar do estudo.
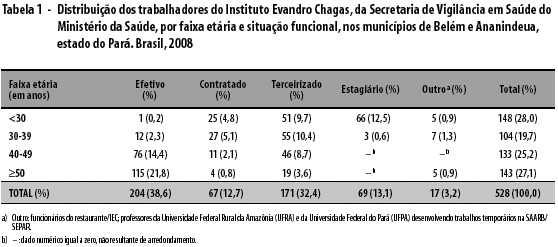
Entre os examinados, observou-se frequência de 54,2% (286/528) para indivíduos do sexo masculino e de 45,8% (242/528) para indivíduos do sexo feminino. A média de idade foi de 39,5±12,6 anos (variação de 15 e 69 anos); e a mediana, 41 anos. A população estudada constituiu-se, principalmente, de pessoas nas faixas etárias <30 anos. A distribuição dos trabalhadores por situação funcional e faixa etária mostrou que os efetivos e terceirizados concentraram a maioria desses trabalhadores (Tabela 1).
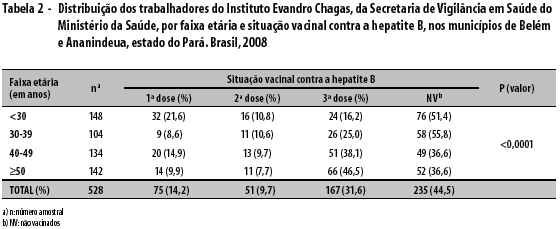
Conforme apresentado na Tabela 2, 31,6% completaram o esquema vacinal contra a hepatite B e 44,5% não haviam recebido qualquer dose da vacina. O maior número de vacinados (46,5%) encontrava-se na faixa etária ≥50 anos, e o menor número, nos indivíduos com idade inferior a 30 anos (16,2%). Verificou-se significância estatística para a terceira dose por meio do teste qui-quadrado de aderência para amostras esperadas iguais: p (valor) <0,0001.
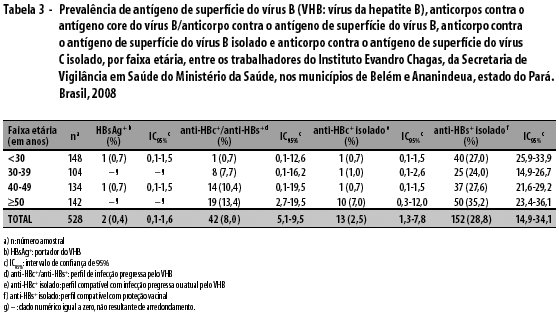
A análise das amostras demonstrou prevalência total de 39,7% para algum marcador do VHB. Na Tabela 3, demonstra-se (i) o perfil compatível com o estado de portador (HBsAg+), (ii) os indicadores de infecção pregressa pelo VHB (anti-HBc+/anti-HBs+), (iii) o marcador isolado compatível com infecção pregressa ou atual pelo vírus (anti-HBc+ isolado) e (iv) o perfil de proteção vacinal (anti-HBs+ isolado). Não se observou significância estatística para a variável 'perfil de portador do VHB', com p (valor) = 0,5221 e para a variável 'perfil compatível com infecção pregressa ou atual pelo VHB', com p (valor) = 0,2685. Entretanto, encontrou-se significância estatística para a variável 'perfil de infecção pregressa pelo VHB', com p (valor) = 0,0002, e para a variável 'perfil compatível com proteção vacinal', com p (valor) = 0,0395, ambas identificadas pelo teste qui-quadrado de aderência.
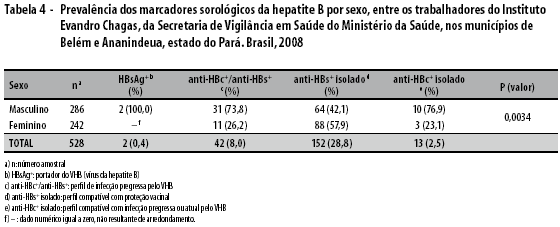
Quanto à predominância dos marcadores sorológicos da hepatite B por sexo, observou-se, para a variável 'perfil de infecção pregressa pelo VHB', significância estatística com p (valor) = 0,0034 pelo teste qui-quadrado de aderência (Tabela 4).
Do total de trabalhadores examinados, 68,4% (361/528) eram indivíduos não vacinados (receberam apenas 1 ou 2 doses de vacina, ou nenhuma dose de vacina foi-lhes aplicada anteriormente), portanto suscetíveis ao VHB.
Na distribuição dos trabalhadores por área da instituição - Saúde e Administração -, entre os trabalhadores da área da Saúde, 151 não foram vacinados e 38 tinham história prévia de vacinação. Aqui, a aplicação do teste qui-quadrado de aderência, em nível de significância de 5% (0,05), encontrou significância estatística para trabalhadores suscetíveis, com p (valor) = 0,0228.
Discussão
A cobertura vacinal contra a hepatite B preconizada pelo Ministério da Saúde do Brasil é de 90,0%. Entretanto, o estudo atual detectou que apenas 31,6% dos trabalhadores receberam o esquema vacinal completo, uma medida fundamental, principalmente para os que se encontram na faixa etária abaixo dos 30 anos. Para os profissionais da Saúde, é necessário que, 30 dias após a administração da última dose do esquema vacinal, seja realizado teste sorológico para controle dos títulos de anticorpos e avaliação da resposta imunológica, uma vez que o aumento do número de susceptíveis pode proporcionar o surgimento de infectados e/ou portadores do vírus.17
O resultado de 31,6% de prevalência do esquema vacinal completo, observado nesta pesquisa, foi inferior ao de estudos realizados no Hospital de Base de São José do Rio Preto-SP, onde se obteve uma prevalência de 73,5% de vacinados contra hepatite B; o resultado também foi inferior à prevalência encontrada em pesquisa desenvolvida no Rio de Janeiro.7,8
A pesquisa mostrou um padrão de endemicidade moderada (2,0% e 7,0%), segundo a classificação adotada por Beasley e Whang, corroborando o apontado nos estudos de Bensabath e Soares sobre a Amazônia oriental, onde os percentuais de HBsAg variam de 0,0 a 2,7%, e do anti-HBs, entre 6,75 e 13,8%.11,12
A prevalência de 0,4% obtida para o HBsAg+ revelou a presença de portadores do VHB na população estudada, achado semelhante a 0,6% encontrado para os cirurgiões-dentistas e auxiliares odontológicos avaliados no Município de Ribeirão Preto-SP, em 2002.18 Não obstante, valores quatro vezes inferiores de HBsAg+ (0,1%) foram obtidos entre doadores de sangue em Ribeirão Preto-SP, em 2005.19 A avaliação de profissionais de saúde em Hospital de São José dos Campos-SP no ano de 2005, contudo, encontrou prevalência de VHB de 0,8%,7 o dobro da apresentada neste estudo.
A prevalência de 8,0% dos marcadores anti-HBc+/ anti-HBs+ indicou a presença de indivíduos previamente infectados, que desenvolveram imunidade natural ao VHB, sendo esse percentual maior que o encontrado entre trabalhadores de hospital universitário de Natal, capital do estado do Rio Grande no Norte, no ano de 1999, quando a presença simultânea desses marcadores foi de 4,3%.20
No atual estudo, o anti-HBs+ isolado mostrou elevada prevalência (28,8%) quando comparada à prevalência intermediária (5,2%) desse marcador, encontrada no estudo realizado em Natal-RN (1999).20 Ademais, no estudo de São José dos Campos-SP, de 2005, 86,4% da população analisada mostrou resposta positiva para o marcador, sugerindo imunização contra o VHB.7
A prevalência de anti-HBc+ isolado em 2,5% dos indivíduos foi equivalente à observada por vários estudos com doadores de sangue.8,18
Na avaliação da relação da prevalência de marcadores sorológicos com o sexo, observou-se predomínio do sexo masculino para o HBsAg+, anti-HBc+/anti-HBs+ e anti-HBc+ isolado, enquanto para o anti-HBs+ isolado, a prevalência maior foi do sexo feminino. Em estudo de soroprevalência da hepatite B desenvolvido em 2007, com profissionais de um Laboratório de Saúde Pública, não foi observada diferença estatisticamente significativa entre o sexo feminino e o sexo masculino, para os títulos de anti-HBs+ isolado.21
A pesquisa identificou baixa cobertura vacinal entre os trabalhadores da instituição, com soroconversão de 28,8% para o anti-HBs e presença de não respondedores à vacinação. A taxa de soroconversão para o anti-HBs encontrada mostrou-se inferior à relatada em outros estudos,22,23 em caso de exposição ocupacional à material biológico, de acordo com o que preconiza o Programa Nacional para a Prevenção e o Controle das Hepatites Virais/SVS/MS.24
Relacionando-se as áreas de atuação dos trabalhadores do IEC/SVS/MS a sua situação vacinal, a taxa de soroconversão para o anti-HBs+ (28,8%) entre os trabalhadores, tanto da área da Saúde como da Administração, mostrou-se muito abaixo da média informada pelo Ministério da Saúde, o qual considera que a aplicação de três doses da vacina deveria conferir proteção de aproximadamente 90,0% em adultos.14
Entre os trabalhadores da Administração do IEC/SVS/MS, a prevalência (58,1%) de suscetíveis ao vírus estava muito acima do percentual encontrado na área da Saúde, no instituto (31,3%). Segundo um estudo da prevalência de anti-HBs+ em função do tipo de atividade hospitalar, realizado em 1999, as categorias que apresentaram maiores índices de prevalência foram os trabalhadores do laboratório de análises clínicas (24,0%), da enfermagem (23,6%), médicos (20,8%) e pessoal da limpeza (18,2%). Nas atividades administrativas e em outras áreas onde os trabalhadores não mantinham contato direto com os pacientes, essa prevalência foi de 9,1%.20
Como limitações do estudo, destacam-se a elevada proporção de perdas, assim como o desconhecimento do tempo decorrido entre a administração da terceira dose e a coleta do material para exame. A titulação de anticorpos tende a declinar com o passar do tempo pós-vacinação, de maneira que a prevalência de imunização com titulação adequada de anticorpos pode ter sido subestimada caso a coleta do sangue para mensuração da titulação de anticorpos tenha se realizado muito tempo após a vacinação, em uma proporção elevada de trabalhadores.
Não se tem dúvida sobre a necessidade de imunização do profissional da Saúde, no cumprimento do que determina a legislação vigente: a Norma Regulamentadora 32 (NR-32), que versa sobre a segurança do trabalhador em saúde.2
Ressalta-se a importância da realização de estudos na área dos laboratórios, no sentido de contribuir para esta discussão sobre a necessidade de se conhecer a situação vacinal e o perfil sorológico da hepatite B entre os trabalhadores da Saúde, particularmente os profissionais envolvidos em atividade de pesquisa extra-institucional, para a confirmação da imunidade por eles adquirida, não se limitando à realização de testes sorológicos unicamente após a ocorrência dos acidentes ocupacionais ou quando solicitados por serviços de medicina do trabalho.
Agradecimentos
A Direção do Instituto Evandro Chagas - IEC/SVS/MS -, pelo auxílio recebido, aos funcionários de sua Seção de Hepatologia e a todos que contribuíram para a realização do projeto.
Contribuição dos autores
Oliveira CMA, foi responsável por todas as fases do estudo, incluindo a elaboração do projeto e dos instrumentos, realização das análises e redação final do artigo.
Nunes MRT colaborou no desenho do estudo, orientou, revisou e implementou modificações necessárias.
Nunes HM participou integralmente de todas as fases do trabalho, desde o desenho do estudo à redação final.
Soares MCP colaborou no desenho do estudo e na discussão dos achados.
Todos os autores aprovaram a versão final do manuscrito.
Referências
1. Organização Mundial de Saúde. Hepatite B [Internet]. Geneva: Organização Mundial de Saúde; 2007 [acessado em 06 nov. 2007]. Disponível em http://www.who.int/vaccines-diseases/diseases/hepatitis_b.htm
2. Portaria no 939, de 18 de novembro de 2008. O Ministro do Trabalho e Emprego, no uso das atribuições que lhe confere o artigo 87, parágrafo único, inciso II, da Constituição Federal, e os artigos 155, inciso I, e 200 da Consolidação das Leis do Trabalho. Diário Oficial da União, Brasília, p. 238, 19 de novembro 2008. Seção 1.
3. Olkner RK. Acute viral Hepatitis. In: Cecil RLF. Textbook of Medicine, editor. Philadelphia: Saunders; 1996. p. 762-772.
4. Bonanni P, Bonaccorsi G. Vaccination against hepatitis B in health care workers. Vaccine. 2001; 19(17-19):2389-2394.
5. Dannetun E, Tegnell A, Giesecke J. Coverage of hepatitis B vaccination in swedish healthcare workers. Journal of Hospital Infection. 2006; 63(2):201-204.
6. Vos D, Götz HM, Richardus JH. Needlestick injury and accidental exposure to blood: the need for improving the hepatitis B vaccination grade among health care workers outside the hospital. American Journal of Infection Control. 2006; 34(9):610-612.
7. Ciorlia LAS, Zanetta DMT. Hepatitis B in healthcare workers: prevalence, vaccination and relation to occupational factors. The Brazilian Journal of Infectious Diseases. 2005; 9(5):384-389.
8. Andrade AFB, Oliveira-Silva M, Silva SGC, Motta IJ, Bonvicino CR. Seroprevalence of hepatitis B and C virus markers among blood donors in Rio de Janeiro, Brazil, 1998-2005. Memórias do Instituto Oswaldo Cruz. 2006; 101(6):673-676.
9. Ministério da Saúde. Departamento de AIDS, DST e Hepatites virais. Hepatites Virais. Boletim Epidemiológico. 2010; 1(1):1-62.
10. Rapparini C. Implementação de um programa de vigilância e instituição de quimioprofilaxia pós-exposição ocupacional ao HIV no município do Rio de Janeiro [Dissertação de Mestrado]. Rio de Janeiro (RJ): Universidade Federal do Rio de Janeiro, Faculdade de Medicina; 1999.
11. Beasley RP, Whang LY. Overview on the epidemiology of hepatocelular carcinoma. In: Hollinger FB, Lemon SM, Margolis HM, editors. Proceedings of the 1990 International Symposium on Viral Hepatitis and Liver Disease. Baltimore: Williams & Wilkins; 1991. p. 532-535.
12. Bensabath G, Soares MCP, Maia MMS. Hepatites por vírus. In: Fundação Serviços de Saúde Pública. Instituto Evandro Chagas: 50 anos de contribuição às ciências biológicas e à Medicina tropical. Belém: Fundação Serviços de Saúde Pública; 1986.
13. Bensabath G, Leão RNQ. Epidemiologia na Amazônia Brasileira. In: Focaccia R, editor. Tratado de hepatites virais. São Paulo: Atheneu; 2003. p. 1-26.
14. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Guia de Vigilância Epidemiológica. Brasília: Ministério da Saúde; 2009.
15. Ayres M, Ayres Jr M, Ayres DL, Santos AS. Bio Estat 5.0: aplicações estatísticas nas áreas das ciências biológicas e médicas. 5a ed. Belém: Sociedade Civil Mamirauá; 2007.
16. Ministério da Saúde. Comissão Nacional de Ética em Pesquisa. Resolução no 196, de 10 de outubro de 1996. Brasília: Ministério da Saúde; 1996.
17. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Guia de Vigilância Epidemiológica. Brasília: Ministério da Saúde; 2005.
18. Rodrigues VC. Hepatite B no Município de Ribeirão Preto (SP): um estudo envolvendo cirurgiões dentistas e auxiliares odontológicos [Dissertação de Mestrado]. Ribeirão Preto (SP): Universidade de São Paulo; 2002.
19. Valente VB, Covas DT, Passos AD. Hepatitis B and C serologic markers in blood donors of the Ribeirão Preto Blood Center. Revista da Sociedade Brasileira de Medicina Tropical. 2005; 38(6):488-492.
20. Fernandes JV, Braz RFS, Neto FVA, Silva MA, Costa NF, Ferreira AM. Prevalence of serologic markers of the hepatitis B virus in hospital personnel. Revista de Saúde Pública. 1999; 33(2):122-128.
21. Moreira RC, Saraceni CP, Oba IT, Spina AMM, Pinho JRR, Souza LTM, et al. Soroprevalência da hepatite B e avaliação da resposta imunológica à vacinação contra a hepatite B por via intramuscular e intradérmica em profissionais de um laboratório de saúde pública. Jornal Brasileiro de Patologia Médica Laboratorial. 2007; 43(5):313-318.
22. Havlichek DJ, Rosenman K, Simms M, Guss P. Age-related hepatitis B seroconversion rates in health care workers. American Journal of Infection Control. 1997; 25(5):418-420.
23. Marinho RT, Pedro M, Ramalho F, Velosa J, Moura MC. Vacinação contra hepatite B: oito anos de experiência. Acta Médica Portuguesa. 1998; 11(11):971-977.
24. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Hepatites Virais: o Brasil está atento. Brasília: Ministério da Saúde; 2008.
 Endereço para correspondência:
Endereço para correspondência:
Instituto Evandro Chagas,
Rodovia BR 316, Km 7, S/N,
Levilândia, Ananindeua-PA,
Brasil.
CEP: 67030-000
E-mail: candidaoliveira@iec.pa.gov.br
Recebido em 03/09/2010
Aprovado em 11/10/2012
*Dissertação de mestrado pelo Programa de Pós-Graduação em Biologia de Agentes Infecciosos e Parasitários, do Instituto de Ciência Biológicas da Universidade Federal do Pará, defendida em 27 de agosto de 2009.