Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Epidemiologia e Serviços de Saúde
versión impresa ISSN 1679-4974versión On-line ISSN 2237-9622
Epidemiol. Serv. Saúde v.22 n.1 Brasília mar. 2013
http://dx.doi.org/10.5123/S1679-49742013000100011
ARTIGO ORIGINAL
Prevalência de infecção pelo T. cruzi em doadores de sangue nos hemocentros coordenadores do Brasil em 2007
Trypanosoma cruzi infection prevalence among blood donors in the Brazilian Coordinating Blood Centers in 2007
Vera Lúcia Carvalho da SilvaI; Expedito José de Albuquerque LunaII
ICoordenadoria Estadual de Vigilância Epidemiológica, Secretaria de Estado da Saúde de Mato Grosso do Sul, Campo Grande-MS, Brasil
IIUniversidade de São Paulo, São Paulo-SP, Brasil
RESUMO
OBJETIVO: conhecer a prevalência de Trypanosoma cruzi entre os doadores de sangue, analisar a organização da rede de hemoterapia e as normas de segurança do sangue para transfusão no Brasil no ano de 2007.
MÉTODOS: estudo descritivo utilizando-se os Regulamentos Técnicos para hemoterapia definidos pela Agência Nacional de Vigilância Sanitária (Anvisa) e o questionário aplicado aos Hemocentros Coordenadores (HC) do Brasil.
RESULTADOS: responderam 84% dos hemocentros, onde doaram sangue 3.251.361 indivíduos, sendo 1.192 (0,04%) excluídos na triagem clínica por risco presumido para doença de Chagas; foram realizadas 2.726.668 sorologias; 5.432 (0,20%) foram reagentes para Trypanosoma cruzi e 3.065 (0,11%) inconclusivas.
CONCLUSÃO: a falta de resposta dos Estados de Pernambuco, Bahia, Paraíba, Goiás e Rondônia constituiu limitação ao estudo; entretanto, os resultados obtidos sugerem baixa prevalência de Trypanosoma cruzi entre os doadores de sangue e indicam o cumprimento dos procedimentos para a segurança do sangue definidos pela Anvisa.
Palavras-chave: Doença de Chagas; Transfusão de Sangue; Trypanosoma cruzi; Segurança do Sangue; Epidemiologia Descritiva.
ABSTRACT
OBJETIVE: To assess T. cruzi infection prevalence among blood donors, to analyze the Brazilian hemotherapy network and its compliance with safety standards in 2007.
METHODS: descriptive study using the Brazilian health regulatory agency (ANVISA) technical regulations for hemotherapy as a reference. A questionnaire was also applied to Brazil's Coordinating Blood Centers.
RESULTS: 84% of the Coordinating Blood Centers answered the questionnaire. In these Blood Centers3,251,361 individuals donated blood, of whom 0.04% were excluded after clinical screening forpresumed T. cruzi infection risk. 2,726,668 serological tests for T. cruzi were carried out, of which 5,432 (0.2%) were positive and 3,065 (0.11%) presented inconclusive results.
CONCLUSION: A limitation of this study was thatfive of the Coordinating Blood Centers did not answer the questionnaire. The data indicate low T. cruzi infection prevalence among blood donors and suggest compliance with the technical regulations defined by ANVISA for blood safety.
Key words: Chagas disease; Blood Transfusion; Blood Safety; Trypanosoma cruzi; Epidemiology Descriptive.
Introdução
A doença de Chagas tem como agente etiológico um protozoário flagelado, o Trypanosoma cruzi (T. cruzi). A transmissão natural ocorre com a contaminação de lesões da pele ou das mucosas pelas fezes dos vetores, insetos hematófagos estritos da família Triatominae. Os mecanismos secundários de transmissão são por via transfusional sanguínea, transmissão vertical, por via oral, transplante de órgãos e acidental em laboratórios.1
A transmissão transfusional da doença de Chagas foi confirmada no Brasil em São Paulo, por Pedreira de Freitas & col, em 1952.2 Dias3 relata que até o final da década de 1970, as transfusões de sangue se concentravam nas grandes cidades brasileiras onde a tecnologia era rudimentar, existia alta proporção de doadores remunerados, não havia controle do produto transfundido e a cobertura de testes sorológicos para doença de Chagas em doadores de sangue era menor que 20%. Segundo o autor, estimava-se que, entre os 100 mil casos novos que ocorriam a cada ano, 20 mil correspondiam à transmissão transfusional, e que até 1979 ainda eram detectados em torno de 15 mil casos novos da doença por essa forma de transmissão.
Em 1976, o Ministério da Saúde realizou um diagnóstico sobre a coleta e a distribuição de sangue no território brasileiro. Diante da situação encontrada, foi definida a necessidade de se implantar hemocentros públicos nas capitais dos Estados, baseados na doação voluntária de sangue. Assim, em 1977, foi inaugurado o Centro de Hemoterapia e Hematologia de Pernambuco (Hemope). A partir de 1980, com a implantação do Programa de Sangue do Ministério da Saúde, que determinou o fim da remuneração de doadores, a rede de hemocentros foi se expandindo para todos os Estados brasileiros.4
Em 1986, foi realizada a VIII Conferência Nacional de Saúde, destacando-se nos temas abordados, a segurança do sangue para transfusão. O produto do Relatório Final dessa Conferência forneceu subsídios para a Constituição Federal Brasileira, Artigo 199, parágrafo 4.5 Vários dispositivos legais definem, desde então, a política de segurança do sangue para transfusão no País, com destaque para o Programa de Avaliação Externa de Qualidade (AEQ) em Imunohematologia e Sorologia,6 o Sistema de Hemovigilância7 e as Resoluções de Diretoria Colegiada (RDC) da Agência Nacional de Vigilância Sanitária (Anvisa).8,9
Diversos fatores podem contribuir para a persistência do risco de transmissão da doença de Chagas por transfusão sanguínea, com destaque para a triagem clínica e sorológica, o nível de cobertura de sorologia de infecções por T. cruz e a sensibilidade dos testes para diagnóstico sorológicos utilizados, além da prevalência da doença na região.10
Em 1990, a doença de Chagas passou a ser parte da agenda política internacional, sendo instituída a Iniciativa Intergovernamental do Cone Sul (Inconsul), programa de cooperação entre países do qual participam Argentina, Bolívia, Brasil, Chile, Paraguai e Uruguai. No documento de criação da Iniciativa, foram estabelecidos dois objetivos: o primeiro com foco na eliminação do vetor domiciliado Triatoma infestans, e na redução e na eliminação da infestação domiciliar por outras espécies de triatomíneos; o segundo com vistas à redução e à eliminação da transmissão transfusional, mediante o fortalecimento da rede de bancos de sangue e o controle dos doadores dos países envolvidos.11
Considerando os requisitos definidos, ressalta-se a situação do Brasil em relação ao cumprimento das metas estabelecidas para os Estados-parte da Iniciativa do Cone Sul: o país foi certificado em 2006 como área livre da transmissão vetorial pelo T. Infestans.12 A transmissão por vetor autóctone é acidental não domiciliar, ocorrendo basicamente fora da área onde havia T. infestans no passado.13 Além disso, deve ser considerado o arcabouço jurídico-legal que regulamenta a questão do sangue para transfusão no Brasil.
O presente estudo teve como objetivo descrever a prevalência de T. cruzi entre os doadores de sangue, a organização da rede de hemoterapia no Brasil e outros fatores que contribuem para a segurança do sangue para transfusão, a fim de fornecer subsídios para a certificação do País como área livre da transmissão transfusional da doença de Chagas.
Métodos
Trata-se de um estudo descritivo realizado durante o ano de 2009, desenvolvido a partir de dados da Anvisa sobre a organização da rede de hemoterapia brasileira14 e do resultado do questionário semiestruturado que foi aplicado nos 32 hemocentros coordenadores do Brasil, com informações referentes ao ano de 2007. Esses hemocentros constituíram-se na população de estudo e estão localizados nas 27 nas capitais dos Estados e no Distrito Federal, e em cinco municípios do interior do Estado de São Paulo.15
Para elaborar o questionário, utilizou-se a Resolução de Diretoria Colegiada - RDC/153/Anvisa -,9 que trata do Regulamento Técnico para Procedimentos de Hemoterapia. As perguntas foram organizadas em cinco áreas:
i) Área técnica do hemocentro, com questões referentes ao programa de garantia de qualidade e biossegurança, Procedimento Operacional Padrão (POP), Painéis de Soro e Avaliação Externa de Qualidade;
ii) Seleção de doadores, em que são abordadas situações da triagem clínica e sorológica, dados referentes à exclusão de doadores e sorologias reagentes;
iii)Métodos utilizados para realizar diagnóstico sorológico de infecções por T. cruzi, com questões sobre a sensibilidade e a especificidade dos testes;
iv) Procedimentos adotados em relação ao doador que apresenta sorologia positiva para a infecção por T. cruzi e notificação à vigilância sanitária e epidemiológica dos exames reagentes para T. cruzi; e
v) Procedimentos adotados em relação aos hemocomponentes dos doadores de repetição com sorologia reagente para T. cruzi e que apresentavam sorologias não reagentes em doações prévias.
O critério utilizado para a definição da amostra foi pesquisar em 100% dos estabelecimentos de hemoterapia de gestão pública, classificados como Hemocentros Coordenadores,8 conforme abaixo:
Hemocentro Coordenador - HC
Entidade de âmbito central, de natureza pública, localizada preferencialmente na capital, referência do Estado na área de Hemoterapia e/ou Hematologia, com a finalidade de prestar assistência e apoio hemoterá-pico e/ou hematológico à rede de serviços de saúde. Deverá prestar serviços de assistência às áreas a que se propõe, de ensino e pesquisa, formação de Recursos Humanos (RH), controle de qualidade, suporte técnico, integração das instituições públicas e filantrópicas, e apoio técnico à Secretaria de Estado de Saúde na formulação da Política de Sangue e Hemoderivados no Estado, de acordo com o Sistema Nacional de Sangue e Hemoderivados - SINASAN - e o Plano Nacional de Sangue e Hemoderivados - PLANASHE -, e em articulação com as Vigilâncias Sanitária e Epidemiológica.
A inclusão dos Hemocentros do interior de São Paulo foi baseada no Decreto n° 32.849, de 23 de janeiro de 1991, de São Paulo,15 que define em seu Artigo 2o os Hemocentros que compõem a Rede Estadual de Hematologia-Hemoterapia: Fundação Pró-Sangue - Hemocentro de São Paulo; Centro de Hematologia-Hemoterapia da Unicamp, Hemocentro de Ribeirão Preto (Hospital das Clínicas); Hemo-Oncocentro de Marília, da Fundação Faculdade de Medicina de Marília; e Divisão Hemocentro de Botucatu, da UNESP.
Os questionários foram enviados pela Empresa Brasileira de Correios e Telégrafos em janeiro de 2009 e por meio eletrônico.
Foram analisados os resultados das sorologias para T. cruzi realizadas nos Hemocentros Coordenadores do Brasil e referentes ao ano de 2007, e a oferta de serviços de hemoterapia segundo região geográfica, natureza de gestão [público, privado, privado contratado pelo Sistema Único de Saúde (SUS) ou filantrópico], por níveis de complexidade, por nomenclatura e por conceituação definidas na RDC Anvisa n° 151.8
No ano do estudo, havia 2.364 unidades de hemoterapia cadastradas no banco de dados da Anvisa. Identificou-se que a maior concentração de serviços encontra-se na região Sudeste, com 926 estabelecimentos, e quanto ao tipo de serviço executado, os hemocentros coordenadores representam 1,1% de toda a rede e são enquadrados no nível I de complexidade. As unidades de hemoterapia com gestão pública são 878 e as de gestão privada conveniada ao SUS são 681; juntas, equivalem a 66% de todo o serviço disponível no País.
Os resultados do questionário foram analisados por região geográfica e por unidade da Federação. Para as perguntas referentes à inaptidão clínica e sorológica, foram utilizados os indicadores de banco de sangue preconizados pela Organização Panamericana-Organização Mundial da Saúde (OPAS-OMS),16 quais sejam:
1. Proporção de inaptidão clínica (percentual de inaptos na triagem clínica entre os candidatos a doação);
2. Proporção de inaptidão sorológica para todas as doenças passíveis de transmissão sanguínea (DPTS) (percentual das amostras reagentes para alguma DPTS entre as amostras de sangue triadas);
3. Proporção de inaptidão sorológica para T. cruzi (percentual de amostras reagentes para infecção por T. cruzi entre as amostras de sangue triadas);
4. Proporção de sorologia inconclusiva para T. cruzi (percentual de amostras inconclusivas para infecção por T. cruzi entre as amostras de sangue triadas); e
5. Proporção de descarte de bolsa de sangue por T. cruzi (percentual de bolsas positivas ou das positivas somadas às inconclusivas, entre as amostras de sangue triadas).
A consolidação dos dados foi realizada pelo aplicativo Epi Info Windows 3.5.1. Os resultados epidemiológicos e o detalhamento dos dados referentes à hemorrede nacional foram apresentados em tabela e figura construídas pelo programa Excel 2007.
O estudo foi aprovado no dia 25 de março de 2009 pelo Comitê de Ética em Pesquisa da Faculdade de Ciências Médicas da Santa Casa de São Paulo (São Paulo-SP), com o registro n° 070/09. Foram utilizados dados secundários, fornecidos pelos hemocentros, sendo mantida a confidencialidade e preservada a privacidade dos sujeitos.
Resultados
O questionário foi enviado para 32 hemocentros coordenadores do Brasil, sendo 26 localizados nas capitais dos Estados, um no Distrito Federal e cinco em municípios do interior do Estado de São Paulo. Atenderam à solicitação da pesquisa 27 dos hemocentros requisitados. Não responderam os seguintes Estados: Pernambuco, Bahia, Paraíba, Goiás e Rondônia.
Dados do questionário apontam que os hemocentros participam do programa de Avaliação Externa de Qualidade - AEQ -, e em 26 deles o resultado de concordância nos painéis de soro foi de 100%. Todos relataram fazer uso de equipamentos de proteção individual e do Manual de Procedimento Operacional Padrão, devidamente atualizado para a realização dos testes para a infecção por T. cruzi. Os hemocentros pesquisados referiram que validam cada lote de conjunto diagnóstico antes de sua colocação na rotina de trabalho, e que realizam o controle de qualidade interno, utilizando seus próprios painéis de soro caracterizados ou fornecidos por empresa terceirizada.
Em relação à triagem clínica, 16 dos hemocentros responderam que fazem uso de questionário com perguntas específicas sobre doença de Chagas ou fazem perguntas ao candidato a doação durante a anamnese; 24 responderam que registram as não conformidades detectadas em seus laboratórios e 23 realizam as análises críticas e o plano de ação sempre que as observam em qualquer etapa do processo.
Os testes Elisa (Enzyme-Linked Imunosorbent Assay) para diagnóstico de infecção por T. cruzi são utilizados por 100% dos HC; a sensibilidade referida foi de 100% e a especificidade variou entre 92 e 100%. Os testes reagentes para infecção por T. cruzi são repetidos e os resultados informados aos doadores em 100% dos HC. O doador com resultado sorológico positivo para infecção por T. cruzi é excluído definitivamente em 100% dos HC. A avaliação clínica desses doadores é realizada em algum dos serviços citados: ambulatórios de especialidade de hospitais universitários, laboratórios de saúde pública dos Estados, laboratórios de referência nacional, serviço próprio do hemocentro e unidade básica de saúde do município de procedência.
A notificação à Vigilância Sanitária sobre doadores positivos é realizada por 11 HC, e 15 notificam à Vigilância Epidemiológica sem, entretanto, obedecer à rotina pré-estabelecida.
Quando o teste é reagente para infecção por T. cruzi em doador de repetição que não era reagente em doações prévias, as amostras de sangue da última doação são encaminhadas para testes confirmatórios em 19 dos hemocentros pesquisados. Se esse for reagente para infecção por T. cruzi, 100% dos hemocentros verificam o destino de todos os hemocomponentes da doação anterior.
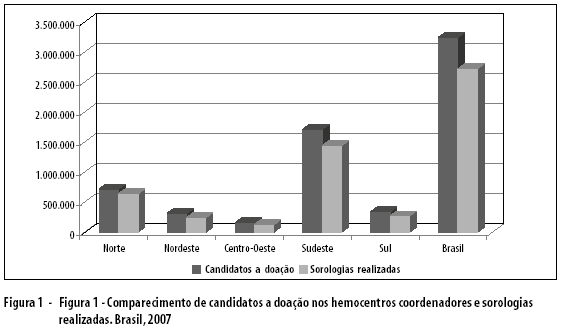
No ano de 2007, compareceram aos hemocentros coordenadores do Brasil 3.251.361 candidatos a doação, e foram realizadas 2.726.668 (83,86%) sorologias (Figura 1). Foram excluídos 1.192 candidatos a doação na triagem clínica (0,04%) com risco presumido para doença de Chagas. Entre os 32 Hemocentros Coordenadores do Brasil, não responderam sobre este critério de exclusão: cinco da Região Norte, três do Nordeste, um do Centro-Oeste, três do Sudeste e um da Região Sul.
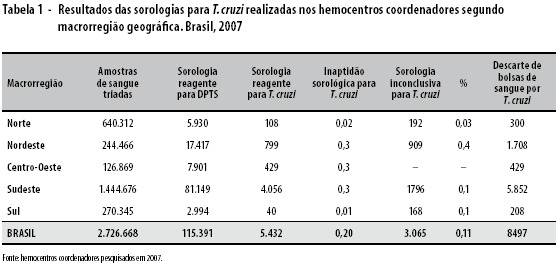
Os resultados dos indicadores epidemiológicos podem ser observados na Tabela 1. As sorologias reagentes para alguma das doenças passíveis de transmissão sanguínea - DPTS - relatadas pelos HC somaram 115.391, em um universo de 2.726.668 sorologias realizadas (4,2%); entre as DPTS, 5.432 foram reagentes para infecção por T.cruzi (4,7%). A taxa de inaptidão sorológica observada em relação a todas as amostras de sangue triadas foi de 0,20%, com variação da mínima de 0,01 na região Sul e 0,3 no Centro-Oeste. Os resultados inconclusivos foram 3.065, representando 2,7% de todas as DPTS e 0,11% em relação ao total das amostras de sangue triadas. Estes resultados remetem para o descarte de bolsas de sangue por T. cruzi em todos os HC, que foi de 8.497 e representou uma taxa de 0,31%.
Discussão
A prevalência de T. Cruzi entre doadores de sangue no presente estudo foi considerada baixa (0,20%). Acredita-se que as medidas de controle vetorial para erradicação do inseto transmissor domiciliar da doença de Chagas, e as normas e procedimentos adotados na rede de hemoterapia brasileira no que diz respeito à segurança do sangue para transfusão, tenham apresentado impacto positivo na redução do risco de transmissão transfusional desse agravo.
Houve grande progresso no controle da doença de Chagas transfusional no Brasil, nas décadas de 1970 a 2000. No presente trabalho, a frequência de sorologia positiva para a infecção chagásica entre os doadores que compareceram aos Hemocentros Coordenadores do Brasil, no ano de 2007, foi compatível com estudos realizados em HC do Estado de São Paulo: Sales e colaboradores (0,83%)17 e Soussumi (1,1%).18 O mesmo foi observado no hemocentro regional de Igatu no Estado do Ceará (1,9%),19 e no Estado do Rio Grande do Sul (0,17%).20 Em 2007, a proporção de inaptidão sorológica por infecção pelo T. cruzi, somada aos resultados inconclusivos, foi de 0,31%; em 2008, de 0,18%; foi de 0,16% em 2009; e de 0,17% em 2010.21
Em estudo transversal para determinação de soro-prevalência da infecção pelo T. cruzi entre os doadores do hemocentro do Estado de Goiás, no período de 2005 a 2009, foi detectada uma prevalência de 1,3% em doadores novos, enquanto em doadores de retorno, a prevalência foi de 0,02%.22 Estes dados contrastam com a elevada prevalência de doadores chagásicos nas décadas passadas: anos 1970, 11,08%; anos 1980, 7,03%; anos 1990, 3,18%; e 2000, 0,73%.21
Em países endêmicos da América Latina, no ano de 2005, a prevalência de sorologia positiva para T. cruzi em doadores de sangue foi, em média, de 1,40%, variando entre 0,01% na Guatemala e 8,0% na Bolívia. Nessa avaliação, o Brasil apresentou 0,21% de prevalência.23 Segundo os autores, nos últimos anos vêm-se registrando redução na prevalência de doença de Chagas entre os doadores, resultado do controle sistemático ou até eliminação da transmissão vetorial, como ocorreu no Brasil. Além disso, a obrigatoriedade da triagem sorológica, imposta na quase totalidade dos países endêmicos, reduz o risco da transmissão transfusional do agravo em toda a América Latina.
Foi considerada uma limitação deste estudo a dificuldade para definir a amostra, já que a RDC Anvisa no 151/2001 deixa dúvidas sobre quais serviços poderão ou não realizar exames marcadores sorológicos para as doenças passíveis de transmissão sanguínea, incluindo a doença de Chagas. Ressalta-se, ainda, a não participação dos Estados com história significativa de transmissão de doença de Chagas: Pernambuco, Goiás e Bahia, este que foi o último a ser certificado como área livre de transmissão vetorial em virtude da persistência de focos residuais do vetor T. infestans. A abstenção de resposta ao questionário sobre resultados inconclusivos para infecção por T. cruzi, por parte de nove HC, e sobre o número de doadores excluídos na triagem clínica por risco presumido de doença de Chagas, não respondido por 13 HC, também foi uma limitação do estudo.
Com o intuito de fornecer subsídios para a resposta brasileira ao compromisso internacional com a Organização Pan-Americana da Saúde - OPAS - de eliminar a transmissão transfusional da doença de Chagas nas Américas, este estudo descreveu a rede de hemoterapia brasileira, a situação dos hemocentros coordenadores em relação ao cumprimento das normas que definem procedimentos técnicos de hemoterapia, e a prevalência de infecção por T. cruzi nos candidatos a doação de sangue. Desse modo, observou-se a existência de uma ampla rede de hemoterapia, hierarquizada e organizada segundo os preceitos legais, e baixa prevalência de infecção por T. cruzi em doadores de sangue nos Hemocentros Coordenadores do Brasil, no ano de 2007.
A eliminação de uma doença pode ser definida como a redução a zero da incidência em uma área geográfica, sendo necessárias contínuas medidas de intervenção. Enquanto problema de Saúde Pública, essa eliminação consiste em reduzir drasticamente a carga de doença a um nível aceitável, tendo em vista as ferramentas disponíveis e a situação sanitária da região.24 Considerando-se esta definição, é possível sugerir que o Brasil está apto a pleitear a certificação de área livre de transmissão transfusional da doença de Chagas. Os resultados deste estudo indicam que os hemocentros brasileiros atendem as recomendações da OPAS quanto à segurança do sangue para transfusão.25 Os inúmeros procedimentos obedecem ao arcabouço jurídico e regulador preconizado pelos órgãos competentes; 100% dos HC realizam triagem clínica e sorológica para doença de Chagas e participam de Programa de AEQ e, ademais, o País conta com o Sistema de Hemovigilância, de avaliação e alerta após a utilização do sangue e seus componentes.
Quanto à segurança na triagem sorológica para doença de Chagas, de uma forma geral, o diagnóstico fundamenta-se na detecção de anticorpos anti-Trypa-nosoma cruzi e a resposta imunológica do hospedeiro tem levado pesquisadores a buscar antígenos altamente sensíveis e específicos. No Brasil, o teste Elisa é utilizado para diagnóstico sorológico de infecção por T. cruzi em bancos de sangue por ser sensível, específico, com leitura objetiva e passível de automação.26 Neste estudo, os resultados de sensibilidade do teste Elisa relatados pelos HC são compatíveis com os encontrados por alguns pesquisadores, 87 a 99%,27,28 98 a 100%28 e 100%.29
Embora não esteja disponível um documento oficial com as regras para a certificação de um país como área livre de transmissão transfusional da doença de Chagas, recomenda-se a elaboração de um instrumento de avaliação e a realização de visita, por equipe internacional, aos serviços de hemoterapia do Brasil para avaliar o cumprimento das metas estabelecidas pela OPAS, nos moldes do processo adotado para a certificação de área livre de transmissão vetorial.
Contribuição dos autores
Ambos os autores participaram da concepção do estudo, análise, redação e aprovaram a versão final do manuscrito.
Referências
1. Ministério da Saúde. Secretaria de Vigilância em Saúde. Guia de vigilância epidemiológica. 6a ed. Brasília, DF; 2005a.
2. Freitas JLP, Amato Neto V, Sonntag R, Biancalana A, Nussenzweig V, Barreto JG. Primeiras verificações de transmissão acidental da moléstia de Chagas ao homem por transfusão de sangue. Revista Paulista de Medicina. 1952; 40:36-40.
3. Dias JCP Doença de Chagas e transfusão de sangue no Brasil: vigilância e desafios. Ver. Bras. Hematol. Hemoter. 2006;.28(2):81-87 [acessado em 16 nov 2009]. Disponível em http://www.scielo.br/scielo.php?pid=S1516-84842006000200003&script=sci_arttext
4. Junqueira PC, Rosenblit J, Hamerschlak N. História da hemoterapia no Brasil. Rev. Bras. Hematol. Hemoter. 2005; 27(3):201-207 [acessado em 20 jul. 2009]. Disponível em http://www.scielo.br/pdf/rbhh/v27n3/v27n3a13.pdf
5. Brasil. Constituição (1988). Constituição da República Federativa do Brasil. Brasília, DF: Senado Federal; 1988a.
6. Ministério da Saúde. Programa de Qualidade do Sangue - auto-suficiência em sangue, componentes, derivados sanguíneos e correlatos. Programa Avança Brasil/Plano Plurianual (PPA) [monografia na internet]. Brasília, DF; 1998 [acessado em 20 jun. 2009]. Disponível em: http://www.abrasil.gov.br/avalppa/RelAvalPPA2002/
7. Agência Nacional de Vigilância Sanitária. Manual técnico de hemovigilância. Brasília, DF; 2003.
8. Agência Nacional de Vigilância Sanitária. Resolução RDC no 151, de 21 de agosto de 2001. Aprova o regulamento técnico sobre níveis de complexidade dos serviços de hemoterapia. Diário Oficial da União, Brasília, 22 ago. 2001. Seção 1 [acessado em 25 out. 2008]. Disponível em: http://www.anvisa.gov.br/legis/resol/151_01rdc.htm
9. Agência Nacional de Vigilância Sanitária. Resolução RDC no 153, de 14 de junho de 2004. Determina o regulamento técnico para os procedimentos hemoterápicos, incluindo a coleta, o processamento, a testagem, o armazenamento, o transporte, o controle de qualidade e o uso humano de sangue, e seus componentes, obtidos do sangue venoso, do cordão umbilical, da placenta e da medula óssea [resolução na internet]. Diário Oficial da União, Brasília, 24 jun. 2004b. Seção 1:000068 [acessado em 25 ago. 2008]. Disponível em http://portal.saude.gov.br/portal/arquivos/pdf/resolucao_153_2004.pdf
10. Wendel S. Risco residual da transmissão da infecção por Trypanosoma cruzi por via transfusional no Brasil [Tese de doutorado]. São Paulo: Faculdade de Medicina da USP; 2005.
11. Dias JCP, Schofield CJ. A iniciativa do Cone Sul (Inconsul). Centro de Pesquisas René Rachou. Belo Horizonte, MG, Brasil. [acessado em 12 ago. 2009]. Disponível em http://www.fiocruz.br/chagas/cgi/cgilua.exe/sys/start.htm?sid=65
12. Ministério da Saúde. Secretaria de Vigilância em Saúde. Brasil recebe certificado internacional da interrupção da transmissão vetorial da Doença de Chagas pelo Triatoma Infestam. Brasília, DF; 2006 [acessado em 12 ago. 2008]. Disponível em http://portal.saude.gov.br/portal/saude/profissional/visualizar_texto.cfm?idtxt=3215
13. Ministério da Saúde. Secretaria de Vigilância em Saúde. Consenso Brasileiro em Doença de Chagas. Revista da Sociedade Brasileira de Medicina Tropical. 2005b; 38 Supl 3:3-30
14. Agência Nacional de Vigilância Sanitária. Proteção à saúde. Sangue, Tecidos e Órgãos. Hemocad - Sistema Nacional de Serviços de Hemoterapia. Banco de Dados. Sangue e Hemoderivados: Relatório Serviços de Hemoterapia. [acessado em 15 ago. 2009] Disponível em http://www1.anvisa.gov.br/anvisa/hemocad/RelatoriosHemocad.jsp
15. São Paulo. Decreto no 32.849, de 23 de janeiro de 1991. Cria, no âmbito da Secretaria da Saúde, a Hemo-Rede - Rede Estadual de Hematologia-Hemoterapia e dá outras providências. São Paulo; 2007. [acessado em 5 jun. 2009]. Disponível em http://www.jusbrasil.com.br/legislacao/183292/decreto-32849-91-sao-paulo-sp
16. Organización Panamericana de la Salud. Programa de control de enfermedades transmisibles. Guía de evaluación de los procesos de control de triatomineos y del control de la transmisión transfusional del T. cruzi. Montevideo; 2002. Washington, D.C.; 2002 [acessado em 10 ago. 2008]. Disponível em http://www.bvsops.org.uy/pdf/chagas03.pdf
17. Salles NA, Sabino EC, Barreto CC, Barreto AME, Otani MM, Chamone DF. Descarte de bolsas de sangue e prevalência de doenças infecciosas em doadores de sangue da Fundação Pró-Sangue/Hemocentro de São Paulo. Revista Panamericana de La Salud Publica. 2003; 13(2/3):111-116.
18. Soussumi LMT. Estudo da distribuição de doadores reativos para a doença de Chagas no hemocentro de Ribeirão Preto, SP [Dissertação de Mestrado]. Ribeirão Preto: Faculdade de Medicina de Ribeirão Preto da USP; 2004.
19. Sobreira ACM, Ferreira Gomes FVBA, Silva MAM, Oliveira MF. Prevalência de infecção chagásica em doadores de sangue do Hemocentro Regional de Iguatu, CE. Revista da Sociedade Brasileira de Medicina Tropical de São Paulo. 2001; 34(2):193-196.
20. Lunardelli A, Borges FP, Mello KF, Zeferino ASA. Soroprevalência da doença de Chagas em candidatos a doadores de sangue. Rev. Bras. Anal. Clin. 2007; 39(2):139-141 [acessado em 10 set. 2009]. Disponível em http://bases.bireme.br/cgi-bin/wxislind.exe/iah/online/?IsisScript=iah/iah.xis&src=g oogle&base=LILACS&lang=p&nextAction=lnk&exprS earch=477000&indexSearch=ID
21. Ministério da Saúde. Secretaria de Atenção à Saúde. Coordenação-Geral de Sangue e Hemoderivados. Caderno de informação: sangue e hemoderivados: produção hemoterápica: Sistema Único de Saúde - SUS (serviços públicos e privados contratados): serviços privados não contratados pelo SUS. 5a ed. Brasilia: Ministério da Saúde; 2011. (Série G. Estatística e Informação em Saúde). [acessado em 30 out. 2012]. Disponível em http://bvsms.saude.gov.br/bvs/publicacoes/caderno_informacao_sangue_hemoderivados_5ed.pdf
22. Santos CAT. Infecção pelo Trypanosoma cruzi em doadores de sangue: revisão sistemática da literatura e estudo de prevalência no hemocentro de Goiás. Rev. Patol. Trop. 2012; 4l(1):249-252. [acessado em 12 nov. 2012]. Disponível em http://www.revistas.ufg.br/index.php/iptsp/article/download/19335/11235.
23. Moraes-Souza H, Ferreira-Silva MM. O controle da transmissão transfusional. Rev. Soc. Bras. Med. Trop. 2011; 44 Supl 2:64-67 [acessado em 2 mar. 2013]. Disponível em http://www.scielo.br/pdf/rsbmt/v44s2/a10v44s2.pdf
24. World Health Organization. Global disease elimination and eradication as public health strategies. Atlanta, GA. 23-25 Feb 1998 [relatório técnico e científico na internet]. Bull. WHO. 1998; 76(2):22-25. [acessado em 20 dez. 2009]. Disponível em http://www.cdc.gov/mmwr/pdf/other/mm48SU01.pdf.
25. Organização Pan-Americana da Saúde. 46° Conselho Diretor. 57a Sessão do Comitê Regional. Relatório de progresso sobre a iniciativa regional para segurança sanguínea e plano de ação para 2006-2010. Washington, D.C.; 2005 [acessado em 20 ago. 2008]. Disponível em http://www.paho.org/Portuguese/GOV/CD/cd46.r5-p.pdf
26. Ferreira WA, Ávila SLM. Diagnóstico laboratorial das principais doenças infecciosas e auto-imunes. 2a ed. Rio de Janeiro: Guanabara Koogan; 2001. p. 241-249.
27. Umezawa ES, Bastos SF, Camargo ME, Yamandu LM, Santos MR, Gonzalez A, et al. Evaluation of recombinant antigens for serodiagnosis of Chagas' Disease in South and Central America. J. Clin. Microbiol. 1999; 37(5):1554-1560. [Acesso em 12 nov. 2009]. Disponível em http://jcm.asm.org/content/37/5/1554.abstract
28. Gadelha AAM. Avaliação do desempenho do "Kit" EIE - Recombinante - Chagas - Biomanguinhos frente ao ELISA convencional e ao teste de hemoaglutinação indireta [Dissertação de Mestrado]. Recife (PE): Centro de Pesquisas Aggeu Magalhães da Fiocruz; 2003. [acessado em 15 nov. 2009]. Disponível em www.cpqam.fiocruz.br/bibpdf/2003gadelha-aam.pdf
29. Saéz-Aquézar A, Marques WP, Botini MB, Alves A. Avaliação de um Kit ELISA para detecção de anticorpos Anti-T cruzi. Laes Haes. 2005;27(157):136-42.
 Endereço para correspondência:
Endereço para correspondência:
Vera Lúcia Carvalho da Silva -
Coordenadoria Estadual de Vigilância Epidemiológica,
Secretaria de Estado da Saúde de Mato Grosso do Sul,
Avenida do Poeta, Bloco 7, Parque dos Poderes,
Campo Grande-MS, Brasil.
CEP: 79031-902
E-mail: vcarvalhodasilva@gmail.com
Recebido em 21/11/2012
Aprovado em 13/03/2013