Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Epidemiologia e Serviços de Saúde
versão impressa ISSN 1679-4974versão On-line ISSN 2237-9622
Epidemiol. Serv. Saúde v.22 n.4 Brasília dez. 2013
http://dx.doi.org/10.5123/S1679-49742013000400011
ARTIGO ORIGINAL
Avaliação normativa do processo de prescrição e dispensação de imunossupressores para pacientes transplantados renais no estado de Minas Gerais, Brasil, 2008*
Normative evaluation of the immunosuppressive drug prescription and dispensing process for renal transplant patients in the state of Minas Gerais, Brazil, 2008
Daniel Emílio da Silva AlmeidaI; Maria das Graças Braga CeccatoII; Augusto Afonso Guerra JúniorII; Francisco de Assis AcurcioII
IPrograma de Pós-Graduação em Saúde Pública, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil
IIFaculdade de Farmácia, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil
RESUMO
OBJETIVO: avaliar o processo de prescrição e dispensação de imunossupressores para pacientes transplantados renais face às recomendações dos Protocolos Clínicos e Diretrizes Terapêuticas (PCDT, 2002 e 2012).
MÉTODOS: avaliação normativa, enfocando solicitações de imunossupressores à Secretaria de Estado de Saúde de Minas Gerais em 2008, sobre dados de arquivos administrativos informatizados.
RESULTADOS: analisados 915 processos referentes a 687 pacientes, considerando-se o PCDT 2002, a maioria das solicitações foi de medicamento de segunda escolha, representando acréscimo de pelo menos 301% no gasto; com a inclusão do tacrolimo como primeira escolha no PCDT 2012, essa proporção diminuiu, embora ainda preponderassem solicitações de segunda escolha/mista. A Gerência Regional de Saúde de Belo Horizonte-MG dispensou 3,5 vezes mais medicamentos de segunda escolha e apresentou tempo menor de tramitação dos processos.
CONCLUSÃO: constatou-se discordância entre diretrizes terapêuticas e dispensação dos imunossupressores; avaliações de tecnologias de saúde e epidemiológicas contribuem para aprimorar os serviços em saúde.
Palavras-chave: Transplante de Rim; Imunossupressores; Avaliação em Saúde; Gastos em Saúde.
ABSTRACT
OBJECTIVE: to evaluate the process of immunosuppressive drug prescription and dispensing for kidney transplant patients in view of the recommendations of the Clinical Protocols and Therapeutic Guidelines (CPTG, 2002 and 2012).
METHODS: normative evaluation of requisitions for immunosuppressive drugs made to the Minas Gerais State Department of Health in 2008, based on computerized administrative data files.
RESULTS: we analyzed 915 requisitions relating to 687 patients. With regard to CPTG 2002, most of the drugs delivered were classified as second choice, representing increased cost of at least 301%. With the inclusion of Tacrolimus as first choice in CPTG 2012 this percentage has decreased second choice/mixed requests still prevail. Belo Horizonte Regional Health Management dispensed 35 times more second choice drugs and showed a shorter time for requisition process evaluation.
CONCLUSION: there was discordance between therapeutic guidelines and immunosuppressive drug dispensing. Health technology and epidemiological assessments contribute to improved health services.
Key words: Kidney Transplantation; Immunosuppressive Drugs; Health Evaluation; Health Expenditures.
Introdução
A doença renal crônica (DRC) em seu estágio cinco, relacionada com o grau de lesão renal ou ritmo de filtração glomerular menor que 15 ml/min/1,73m2 por período igual ou maior que três meses,1 apresenta magnitude considerável na população brasileira. A perda progressiva da função renal requer o acesso à terapia renal substitutiva (TRS), para sobrevivência do paciente. Estima-se que 2,9 milhões de brasileiros tenham um terço ou menos da taxa de filtração glomerular de indivíduos normais.2
As TRS disponíveis são a hemodiálise, a diálise peritoneal e o transplante renal (TR). O transplante renal, financiado pelo Sistema Único de Saúde (SUS) em mais de 95% dos procedimentos, representou cerca de 38 mil procedimentos entre 2002 e 2011.3 Para a manutenção deste procedimento, é necessária a utilização de medicamentos imunossupressores de alto custo,4 dispensados pelo Componente Especializado da Assistência Farmacêutica (CEAF) do SUS.
No âmbito do CEAF, os medicamentos devem ser dispensados de acordo com as demandas dos pacientes, segundo os critérios estabelecidos nos Protocolos Clínicos e Diretrizes Terapêuticas (PCDT) elaborados pelo Ministério da Saúde.5 O não cumprimento dos PCDT pode interferir na qualidade da assistência prestada.6 O PCDT para transplantados renais foi estabelecido por Portaria da Secretaria de Atenção à Saúde do Ministério da Saúde - SAS/MS no 1018, de 26 de dezembro de 2002.7 Em 17 de julho de 2012, o protocolo foi atualizado pela Portaria no 666.8 No PCDT, estão descritos o tratamento e o acompanhamento dos indivíduos sob imunossupressão. Recomenda-se que essa terapia se constitua de esquemas tríplices, compostos por um esteroide mais dois medicamentos de classes farmacológicas distintas. As classes disponíveis são os inibidores da calcineurina (ciclosporina e tacrolimo), antimetabólitos (azatioprina e micofenolato de sódio/mofetila) e os inibidores da enzima mTOR - mammalian target of rapamicin - (sirolimo e everolimo).
No protocolo vigente até 2012,indicava-se a utilização da ciclosporina em associação com azatioprina como primeira escolha para os receptores de doador vivo (HLA - antígeno leucocitário humano - idêntico ou distinto) e cadavérico com baixa reatividade.7
No PCDT vigente a partir de 2012, recomenda-se a utilização da ciclosporina ou tacrolimo em associação com azatioprina como primeira escolha para receptores de doador vivo (HLA idêntico ou distinto) ou falecido.8 O atual PCDT detalhou as substituições de forma mais criteriosa, quando comparado com o PCDT de 2002.4
No estado de Minas Gerais, os imunossupressores para transplante renal, medicamentos essenciais para a manutenção do transplante, são dispensados provisoriamente, para 30 dias, no momento da solicitação. Esta solicitação segue para análise e somente ao concluir todo o trâmite, o processo é deferido ou não; se for o caso, a dispensação é suspensa.
Considerando-se a situação epidemiológica atual e o direito universal à saúde, em que as atividades assistenciais - inclusive farmacêuticas - devem ser prestadas integralmente, o Brasil se encontra diante do desafio de dar sustentabilidade ao maior sistema público de transplantes do mundo e ofertar medicamentos para manutenção dos enxertos.9
Nesse contexto, estudos focados no perfil de utilização dos medicamentos podem fornecer subsídios para a otimização dos serviços, na perspectiva de manter viável um sistema universal que objetive a melhor qualidade de saúde possível.10
Este estudo teve por objetivo avaliar o processo de prescrição e dispensação de imunossupressores para pacientes transplantados renais no estado de Minas Gerais, Brasil, face às recomendações dos PCDT de 2002 e 2012.
Métodos
Trata-se de uma avaliação normativa, a partir da abordagem de todos os transplantados renais que solicitaram imunossupressores mediante abertura de processo de primeira solicitação ou terapia inicial na Secretaria de Estado de Saúde de Minas Gerais (SES/MG), junto ao Componente Especializado da Assistência Farmacêutica (CEAF), no ano de 2008. A solicitação foi realizada via formulários padronizados, em que consta a justificativa para o pedido.
Os dados foram coletados do arquivo informatizado da Gerência de Medicamentos de Alto Custo (GMAC), que forneceu a lista de pacientes cadastrados na rotina do serviço, no ano de 2008, nas 28 Gerências Regionais de Saúde (GRS) do estado.
Esses dados foram complementados a partir de consultas ao sistema informatizado do setor de apoio à Superintendência de Assistência Farmacêutica (SAF) da Companhia de Tecnologia da Informação do Estado de Minas Gerais (Prodemge) e ao Sistema Informatizado de Gestão Hospitalar (SIGH), além de documentos arquivados na sede da SES/MG e visitas a oito GRS com maior número de informações pendentes. Para o relacionamento dos diversos bancos de dados, foram considerados o nome, sexo e data de nascimento do paciente, além da GRS de origem do processo.
Para as análises, foram selecionadas variáveis relacionadas (i) ao perfil demográfico (sexo e idade), (ii) às características do processo (GRS de origem e situação atual - deferido, indeferido ou sob avaliação) e (iii) aos medicamentos dispensados (apresentações, gasto mensal e priorização no PCDT).
Foi calculado o gasto mensal das terapias de um adulto com peso de 70 kg, para as apresentações de cada medicamento, adotando-se as maiores dosagens recomendadas no protocolo.7 Para esse cálculo, utilizou-se o valor de aquisição constante nas atas de registros de preços da SES/MG em 2008. No caso de mais de um valor de aquisição no período, foi coletado o valor mais frequente.
Para a análise da adequação dos esquemas imunossupressores solicitados, foram consideradas, de acordo com o PCDT 2002, as indicações gerais de priorização de medicamentos segundo os principais tipos de transplantes, obedecendo a uma sequência racional de continuidade em relação à terapêutica inicial de imunossupressão.7 Em seguida, realizou-se uma análise comparativa entre os dois PCDT, de modo a contrastar suas possíveis diferenças em um mesmo cenário:
- PCDT 2002 - primeira escolha (ciclosporina e azatioprina), segunda escolha (micofenolato mofetil ou sódico, tacrolimo e sirolimo) ou mista (incluindo medicamentos de primeira e segunda escolha);7 e
- PCDT 2012 - primeira escolha (ciclosporina ou tacrolimo e azatioprina), segunda escolha (micofenolato mofetil ou sódico, e sirolimo) ou mista (incluindo medicamentos de primeira e segunda escolha).8
Para a comparação estatística, foram considerados apenas os processos de primeira solicitação de medicamentos em 2008, realizados nos 15 dias iniciais desde o registro e vínculo do paciente ao sistema. A análise descritiva incluiu medidas de frequência, tendência central e dispersão. O teste de qui-quadrado foi utilizado para comparação de proporções entre variáveis categóricas; e o teste t de Student, para comparação de médias. A significância considerada foi de 5%. O programa estatístico utilizado foi o SPSS® versão 17.0 para Windows.
A pesquisa foi aprovada pelo Comitê de Ética em Pesquisa da Universidade Federal de Minas Gerais e integra o projeto 'Análise do processo de programação, prescrição e dispensação no programa de medicamentos excepcionais do SUS/MG no ano de 2008' (Parecer COEP UFMG no 0433.0.203.000-11).
Os preceitos éticos foram rigorosamente observados. Quaisquer dados possíveis de identificar os pacientes foram codificados de forma a garantir sua privacidade e a confidencialidade das informações existentes nas bases estaduais de dados secundários.
Resultados
No ano de 2008, foram abertos 964 processos com o código de transplante renal (Z94.0), segundo a Décima Revisão da Classificação Estatística Internacional de Doenças e Problemas Relacionados à Saúde (CID-10). Desses processos, 915 (94,9%) solicitaram pelo menos um imunossupressor (total de 1.473 no período) e referiam-se a 687 pacientes. Observou-se maior concentração de pedidos no segundo semestre do período de estudo: 518 processos, que corresponderam a 56,6% do total.
A maioria dos pacientes solicitou um (n=480; 69,9%) ou dois medicamentos (n=188; 27,4%), seguidos por poucos que solicitaram três (n=17; 2,5%) e quatro (n=2; 0,3%) medicamentos. Predominaram pacientes do sexo masculino (n=423, 61,6%), com média de idade igual a 42,9 anos (desvio padrão [DP] = 14,1 anos) e amplitude de 2 a 79 anos.
A maioria das solicitações de medicamentos teve origem na GRS de Belo Horizonte-MG (n=614, 67,1%), seguida pelas GRS de Juiz de Fora-MG (n=43; 4,7%) e Uberlândia-MG (n=35; 3,8%).
Quanto à situação dos processos, 91,9% deles (841) foram deferidos, 7,4% (68) encontravam-se sob avaliação no momento da pesquisa e apenas 0,7% (6) foram indeferidos. Os motivos de indeferimento foram: pedido para diagnóstico incompatível; apresentação farmacêutica não disponibilizada; justificativas clínicas ausentes ou incompatíveis; e apenas um caso sem descrição do motivo. A maioria dos medicamentos solicitados foi de imunossupressores (96,3%). Apenas 57 medicamentos para outras finalidades foram identificados, indicados para possíveis comorbidades entre esses usuários, como, por exemplo, anemia ou prevenção de infecções.
Considerando-se o conjunto de solicitações, segundo o PCDT 2002,7 a maioria dos medicamentos (n=1.288; 87,4%) foi classificada como de segunda escolha (micofenolato de sódio, tacrolimo e sirolimo), e somente 12,6% (185) de primeira escolha (azatioprina e ciclosporina) (Tabela 1).
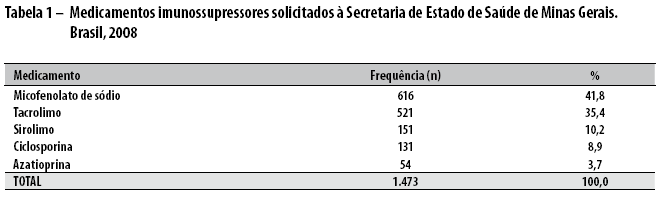
Os medicamentos imunossupressores abrangiam 12 formulações diferentes (cinco de primeira escolha e sete de segunda). Dessas, a mais solicitada foi de tacrolimo 1 mg, seguida por micofenolato de sódio 360 mg e micofenolato de mofetila 500 mg, todos de segunda escolha (58,4%). As seis formulações mais solicitadas foram de segunda escolha, sendo que, para todas elas, havia alternativas de primeira escolha a custos relativamente mais baixos (Tabela 2).
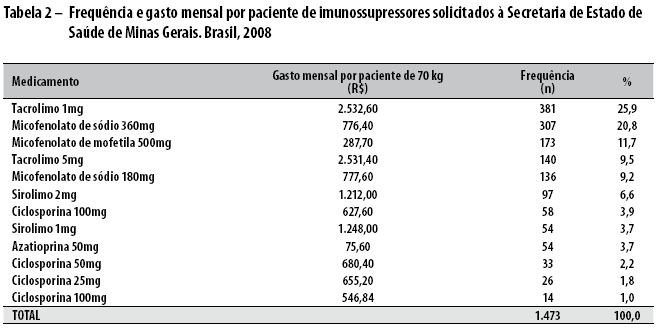
O gasto mensal da terapia para as formulações de medicamentos de primeira escolha, considerando-se a via oral, variou de R$ 703,20 (azatioprina 50 mg e ciclosporina 100 mg) a R$ 756,00 (azatioprina 50 mg e ciclosporina 50 mg). Entre as formulações de segunda escolha, essa variação foi de R$ 2.819,10 (tacrolimo 5 mg e micofenolato de mofetila 100 mg) a R$ 3.780,60 (tacrolimo 1 mg e sirolimo 1 mg). Comparando-se o menor custo da terapia de primeira escolha frente ao de segunda escolha, observou-se um incremento de 301% nos gastos executados (Tabela 2).
Da mesma forma, a avaliação dos esquemas de medicamento por processo, ao longo do ano de 2008, mostrou que a maioria das dispensações foi classificada como de segunda escolha, tanto no primeiro (n=340; 85,6%) como no segundo semestre (445; 85,9%), sendo as porcentagens de deferimento das solicitações de 88,2% e 94,8% respectivamente. A mesma tendência de concentração de dispensação de medicamento de segunda escolha foi observada na avaliação de todas as solicitações (n=785; 84,5%) ou somente dos primeiros requerimentos de medicamentos (n=739; 85,5%). No período analisado, o trâmite do processo levou, em média, 22 dias para ser concluído.
À luz do PCDT 2012,8 mesmo com a inclusão do tacrolimo como medicamento de primeira escolha, a análise também demonstrou maior proporção de solicitação de medicamentos de segunda escolha, 52,1% (n=767) (Tabela 1). Em relação às 12 formulações encontradas, sete seriam de primeira escolha. As formulações mais solicitadas foram de tacrolimo 1 mg (primeira escolha; 25,9%), seguidas pelas de micofenolato de sódio 360mg (20,8%) e micofenolato de mofetila 500mg (11,7%) (segunda escolha; 32,5%) (Tabela 2). Os gastos mensais com as terapias de medicamentos de primeira escolha, considerando-se a via oral, variaram de R$ 703,20 (azatioprina 50 mg mais ciclosporina 100mg) a R$ 2.608,20 (azatioprina 50mg mais tacrolimo 1mg), o que representa uma variação de 269,6% (Tabela 2).
Comparando-se o perfil dos processos abertos pelos pacientes que fizeram o pedido dos medicamentos de primeira escolha com o perfil daqueles que solicitaram esquemas de segunda escolha ou mista, não se observaram diferenças quanto ao sexo, idade, tempo de tramitação do processo e deferimento. A média de idade (desvio-padrão [DP]) dos pacientes com esquemas de 1a escolha comparada com a daqueles de 2a escolha, de acordo com o PCDT de 2002, foi de 40,8 (15,5) e 42,9 (13,8), respectivamente. Quando se considerou o PCDT de 2012, esses valores foram de 41,9 (14,4) e 43,2 (13,6). Quanto ao tempo médio (DP) de tramitação do processo, de acordo com o PCDT 2002, observou-se um período de 22,9 (9,3) dias ou de 22,1 (16,1) dias para os grupos com esquemas de 1a ou de 2a escolha, respectivamente. À luz do PCDT de 2012, esses períodos foram de 21,1 (8,5) dias ou de 22,8 (18,2) dias. Diferenças significativas ocorreram apenas quando se comparou a proporção de processos segundo a origem da solicitação do medicamento (p<0,05) (Tabela 3).
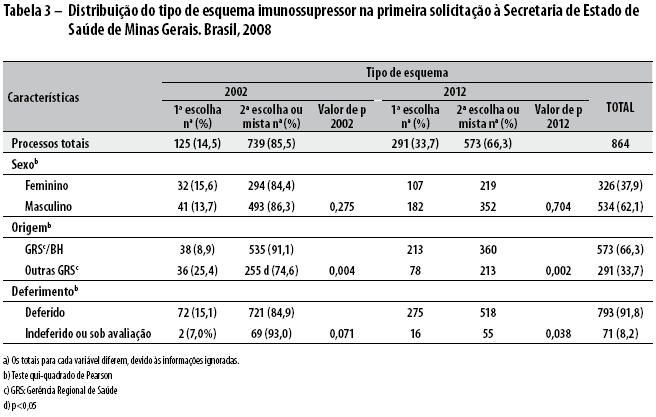
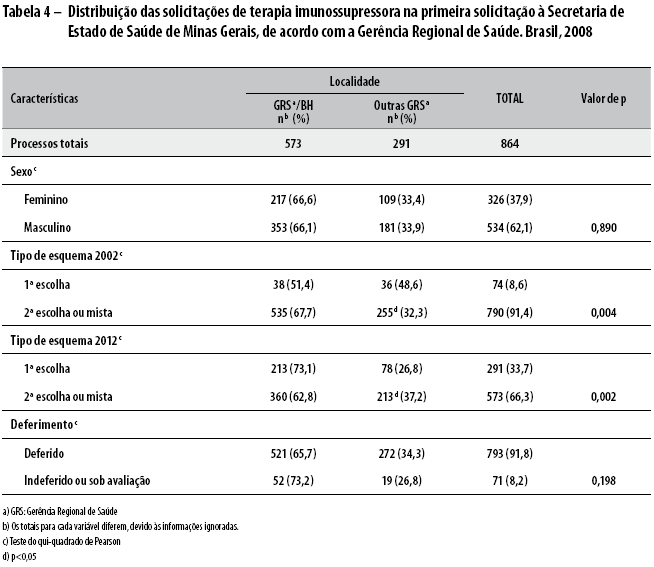
A análise dos processos abertos pelos pacientes, considerando-se o PCDT de 2012,8 demonstrou que mais pacientes apresentaram pedidos de medicamentos de segunda escolha ou mista na GRS/BH, como também houve mais pedidos indeferidos ou sob avaliação para esse tipo de medicamento, com diferenças estatisticamente significantes (p<0,05) (Tabela 3). A avaliação do perfil dos processos de dispensação dos medicamentos por origem da solicitação (da GRS/BH, frente às das outras GRS) mostrou diferença estatisticamente significante quanto ao tempo médio de tramitação, além da diferença já observada na proporção de solicitações de primeira escolha quando comparada com a proporção de solicitações de medicamentos de segunda escolha ou mista (Tabela 4). O tempo médio (DP) de tramitação dos processos observado na GRS/BH foi de 20,0 (9,6) dias; nas outras GRS, esse tempo foi, em média, de 26,3 (22,6) dias (p<0,001).
Discussão
Os medicamentos para insuficiência renal crônica e transplantes, dispensados por meio do CEAF, representaram o maior percentual dos gastos em relação ao total, no período de 2000 a 2007, no Brasil.11 Nesse cenário, destaca-se a relevância da avaliação normativa do processo de prescrição e dispensação de imunossupressores para pacientes transplantados renais, aqui descrita.
Os resultados deste estudo sobre a prescrição/dispensação dos imunossupressores para transplantados renais mostram que não houve consonância entre esses procedimentos e os PCDT de 20027 e 2012.8 Considerando-se o PCDT vigente até 2012, a maioria das solicitações referia-se a medicamentos de segunda escolha e, mesmo com as modificações incorporadas no PCDT de 2012, esse achado se manteve. A utilização de azatioprina, prioritariamente indicada, ficou muito aquém da utilização do micofenolato de sódio/mofetila e sirolimo. Com a inclusão do tacrolimo como medicamento de primeira escolha no protocolo vigente a partir de 2012, essa proporção diminuiu, não obstante continuassem a predominar as solicitações de segunda escolha ou mista.
O objetivo do PCDT é estabelecer diretrizes técnico-administrativas e gerenciais diante de situações clínicas prioritárias para a Saúde Pública, visando difundir informação técnica de qualidade, baseada na melhor evidência científica existente.12 A falta de adesão aos protocolos estabelecidos pode influir desfavoravelmente na racionalidade do uso de medicamentos. A não consonância entre a prescrição/dispensação e os PCDT também foi encontrada em estudo realizado no Rio de Janeiro: seus autores apontam que esse fato contribui para a descontinuidade das diretrizes formuladas, além de interferir na qualidade da assistência prestada.6
Tal situação é ainda mais preocupante quando se leva em conta que produções científicas de alto nível de evidência suscitam sérias discussões a respeito da utilização de medicamentos de segunda escolha em tão larga escala.13-15 Considerando-se aspectos relacionados à eficácia e efetividade, há evidências de que o uso de tacrolimo e de micofenolato de mofetila (medicamentos de segunda escolha no PCDT 2002) apresenta menor risco de rejeição aguda de enxerto. Entretanto, a vantagem observada mostra-se inconclusiva ao se observar outros desfechos, como a sobrevida do paciente e do enxerto. Comparando-se esses desfechos, os medicamentos de primeira e segunda escolha não apresentam diferenças significantes estatisticamente, na maioria dos estudos em diferentes períodos de acompanhamento.16,17
Também há evidências de que imunossupressores de segunda escolha estão associados com uma incidência considerável de eventos adversos, contraindicando-os em diversas situações clínicas.16,18 O perfil de eficácia/efetividade e segurança encontrado da literatura sugere, fortemente, que a farmacoterapia imunossupressora deveria levar em consideração outros aspectos, como características da população (por exemplo, fatores de risco imunológicos e não imunológicos), do paciente e do doador.13,19 Na indicação da farmacoterapia, negligenciar aspectos importantes do perfil dos transplantados renais pode resultar em indicadores de sobrevida piores do que aqueles possíveis de serem alcançados caso seja utilizada a primeira linha de terapia do PCDT.20
Além dos aspectos clínicos, é relevante ressaltar o impacto econômico gerado pela opção por medicamentos de segunda escolha, mais recentes e mais dispendiosos para o serviço de saúde, ainda que não necessariamente mais efetivos. Ao persistir - ou mesmo ampliar - tal situação, pode-se desestabilizar o sistema de dispensação do CEAF. Estudo com enfoque nos gastos referentes a esse componente ressalta a importância da identificação de alternativas custo-efetivas que imprimam maior qualidade no uso dos medicamentos. Os PCDT propiciam racionalidade no uso; contudo, a grande pressão de usuários, médicos, laboratórios farmacêuticos e do Poder Judiciário pelo fornecimento de medicamentos, sem os estudos necessários para respaldar sua indicação, dificultam a organização dos serviços.11
A crescente participação dos gastos com medicamentos nos gastos totais do Ministério da Saúde, impulsionada pelas novidades terapêuticas, também tem sido objeto de estudos e debates e reforça a importância de uma gestão eficiente da assistência farmacêutica.21
As análises de gastos consideraram as doses máximas de imunossupressores, uma vez que não foi possível identificar completamente os pacientes transplantados há mais tempo. Esses pacientes tendem a usar doses menores e os valores referentes ao gasto dos medicamentos podem estar superestimados. Este fato prejudica, embora não invalide, a análise comparativa, que indica o importante impacto da utilização de medicamentos de segunda escolha nos gastos com a imunossupressão.
A situação observada nesta análise ressalta a necessidade de mais estudos sobre esse impacto nos gastos e na efetividade dessa medicação, tanto da tendência de utilização de medicamentos de segunda escolha como das atualizações no PCDT. Também devem ser mencionados os recentes esforços do governo brasileiro pela transferência de tecnologia para o país, cujos laboratórios oficiais passarão a produzir o tacrolimo, micofenolato de sódio e everolimo a partir de acordos realizados em 2012, podendo acarretar reduções consideráveis nos gastos com essa terapia.22,23
A utilização de banco de dados administrativos com grande cobertura possibilita a produção de informações epidemiológicas úteis ao planejamento e organização das ações, embasando eventuais mudanças nas políticas públicas voltadas ao aprimoramento do cuidado em saúde. Vale ressaltar que não se trata de um banco concebido especialmente para a pesquisa, que está sujeito a erros como informações incompletas, inconsistentes, de qualidade e fidedignidade possivelmente comprometidas. Para aumentar a confiabilidade desses dados, foram realizadas análises visando suprimir eventuais registros duplicados.
O número de 687 pacientes registrados como primeira solicitação mostrou-se superestimado. Segundo a Associação Brasileira de Transplante de Órgãos (ABTO), no ano de 2008, foram realizados 435 transplantes em Minas Gerais.3 Parte desses processos pode-se referir a pacientes transplantados em anos anteriores, que estavam renovando/modificando seus esquemas imunossupressores, situação em que, segundo o PCDT 2002, os medicamentos de segunda escolha são mais demandados.7 De qualquer forma, apenas 8,6% das primeiras solicitações referiam-se a terapias de primeira escolha (segundo o PCDT 2002), em um conjunto de 687 pacientes, dos quais se estima que 63,3% foram transplantados em 2008. Frente a um cenário terapêutico complexo, no qual a maioria das prescrições não seguiu as indicações de primeira escolha dos PCDT, e à escassez de estudos sobre a adesão a protocolos e diretrizes, é oportuno considerar as potencialidades da atuação do farmacêutico na equipe de saúde. Esse profissional tem como atribuições (i) avaliar a prescrição médica, (ii) assegurar condições adequadas de conservação e dispensação dos produtos, além de (iii) prestar assistência farmacêutica com acompanhamento farmacoterapêutico.24,25 No desenvolvimento desse acompanhamento farmacoterapêutico junto ao paciente e ao prescritor, o farmacêutico poderia participar diretamente do processo de avaliação da consonância entre as prescrições, o PCDT vigente e o projeto terapêutico do paciente considerado, e assim contribuir na identificação de problemas relacionados aos medicamentos e na promoção de seu uso racional, nessa condição de saúde.6
No âmbito do SUS, a avaliação normativa do processo de prescrição e dispensação de imunossupressores demonstrou lacunas importantes e um gasto elevado com esses medicamentos. Os resultados encontrados apontam para a necessidade de maior consonância das dispensações com os protocolos, melhor adequação da organização das ações e estruturação do CEAF, bem como a utilidade da implementação do acompanhamento farmacoterapêutico de pacientes, visando aprimorar a qualidade da assistência farmacêutica. Disponibilizar PCDT atualizados com as melhores alternativas terapêuticas, fundamentados em evidências científicas e estudos de custo-efetividade disponíveis, e avaliar sistematicamente o processo de atenção constituem condutas capazes de contribuir para a melhoria da qualidade no uso de medicamentos e sua efetividade, além de maior eficiência na gestão da assistência farmacêutica. Estudos comparativos entre os distintos estados brasileiros, dedicados à análise das ações desenvolvidas no âmbito do CEAF, serão de grande valia no debate da estrutura organizacional e de um processo de atenção à saúde que vise à ampliação do acesso aos medicamentos e à resolubilidade dos serviços de saúde responsáveis pela implementação da assistência farmacêutica no SUS.
Agradecimentos
O apoio do Grupo de Farmacoepidemiologia da Universidade Federal de Minas Gerais - UFMG - e o apoio financeiro do Conselho Nacional de Desenvolvimento Científico e Tecnológico - CNPq.
Contribuição dos autores
Almeida DES e Ceccato MGB participaram da elaboração do artigo e do banco de dados, análise dos dados e revisão final do texto.
Guerra Júnior AA contribuiu com o planejamento do estudo, análise e interpretação de dados e revisão crítica do artigo.
Acurcio FA contribuiu com o planejamento do estudo, elaboração do artigo, fornecimento e análise de dados e revisão final do texto.
Todos os autores aprovaram a versão final do manuscrito, e são responsáveis por todos os aspectos do trabalho, incluindo a garantia de sua precisão e integridade.
Referências
1. Levey AS, Eckardt KU, Tsukamoto Y, Levin A, Coresh J, Rossert J, et al. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int. 2005 Jun;67(6):2089-100.
2. Bastos MG, Kirsztajn GM. Doença renal crônica: importância do diagnóstico precoce, encaminhamento imediato e abordagem interdisciplinar estruturada para melhora do desfecho em pacientes ainda não submetidos à diálise. J Bras Nefrol. 2011 jan-mar;33(1):93-108.
3. Associação Brasileira de Transplante de Órgãos. Registro Brasileiro de Transplantes [Internet]. Dados numéricos da doação de órgãos e transplantes realizados por estado e instituição no período: janeiro/setembro-2012. [citado 2012 nov 2]. Disponível em: http://www.abto.org.br/abtov02/portugues/populacao/rbt/mensagemRestrita6.aspx?idCategoria=2
4. Medina-Pestana JO, Vaz MLS, Park SI, Garcia VD, Abbud-Filho M, Campos HH. Organ transplantation in Brazil in the year 2002. Transplant Proc. 2004 May;36(4):799-801.
5. Ministério da Saúde (BR). Portaria GM/MS no 2981, de 26 de novembro de 2009. Aprova o componente especializado da assistência farmacêutica. Diário Oficial da União, Brasília, p.725, 30 nov. 2009. Seção 1.
6. Lima-Dellamora EC, Caetano R, Osorio-de-Castro CGS. Dispensação de medicamentos do componente especializado em polos no estado do Rio de Janeiro. Cien Saude Colet. 2012 set;17(9):2387-96.
7. Ministério da Saúde (BR). Portaria da SASMS no 1018, de 26 de dezembro de 2002. Protocolo Clínico e Diretrizes Terapêuticas (PCDT) para transplantados renais. Diário Oficial da União, Brasília, p. 44, 26 dez. 2002. Seção 1.
8. Ministério da Saúde (BR). Portaria da SASMS no 666, de 17 de julho de 2012. Protocolo Clínico e Diretrizes Terapêuticas (PCDT): imunossupressão no transplante renal. Diário Oficial da União, Brasília, p. 69, 20 jul. 2012. Seção 1.
9. Sociedade Brasileira de Nefrologia. Perfil da doença renal crônica: o desafio brasileiro [Internet]. [citado 2010 set 6]. Disponível em: http://www.prefeitura.sp.gov.br/cidade/secretarias/upload/saude/arquivos/programas/Doenca_Renal_Cronica.pdf
10. Sawyer DO, Leite IC, Alexandrino R. Perfis de utilização dos serviços de saúde no Brasil. Cien Saude Colet. 2002 jan;7(4):757-76.
11. Carias CM, Vieira FS, Giordano CV, Zucchi P. Medicamentos de dispensação excepcional: histórico e gastos do Ministério da Saúde do Brasil. Rev Saude Publica. 2011 abr;45(2):233-40.
12. Ministério da Saúde (BR). Secretaria de Atenção à Saúde. Protocolos Clínicos e Diretrizes Terapêuticas. Brasília: Ministério da Saúde; 2010. (Série A. Normas e Manuais Técnicos)
13. National Institute for Clinical Excellence. Immunosuppressive therapy for renal transplantation in adults. Technology appraisal guidance 85 [cited 2012 set 2]. Available from: http://publications.nice.org.uk/immunosuppressive-therapy-for-renal-transplantation-in-adults-ta85
14. National Institute for Clinical Excellence. Immunosuppressive therapy for renal transplantation in children and adolescents. Technology appraisal guidance 99 [Internet]. [cited 2012 Set 2]. Available from: http://publications.nice.org.uk/immunosuppressive-therapy-for-renal-transplantation-in-children-and-adolescents-ta99
15. Guerra Júnior AA, Cesar CC, Cherchiglia ML, Andrade EI, Queiroz OV, Silva GD, et al. Cyclosporine versus tacrolimus in immunosuppressive maintenance regimens in renal transplants in Brazil: survival analysis from 2000 to 2004. Ann Pharmacother. 2010 Jan;44(1):192-201.
16. Webster AC, Woodroffe RC, Taylor RS, Chapman JR, Craig JC. Tacrolimus versus cyclosporin as primary immunosuppression: meta-analysis and meta-regression of randomised trial data for kidney transplant recipients. BMJ [Internet]. 2005 Oct [cited 2012 Nov 2];331(7520):810. Available from: http://cochrane.bvsalud.org/cochrane/main.php?lib=COC&s earchExp=CD003961&lang=pt
17. Woodroffe R, Yao GL, Meads C, Bayliss S, Ready A, Raftery J, et al. Clinical and cost-effectiveness of newer immunosuppressive regimens in renal transplantation: a systematic review and modelling study. Health Technol Assess. 2005 May;9(21):1-179.
18. Salomão A. Imunossupressão em transplante renal em adultos: conceitos básicos e aplicação clínica. Prat Hosp. 2007;52(9):177-82.
19. Bunnapradist S, Daswani A, Takemoto SK. Graft survival following living-donor renal transplantation: a comparison of tacrolimus and cyclosporine microemulsion with mycophenolate mofetil and steroids. Transplantation. 2003 Jul;76(1):10-5.
20. Haynes B, Haines A. Barriers and bridges to evidence based clinical practice. BMJ. 1998 Jul;317(7153):273-6.
21. Vieira FS, Zucchi P. Aplicações diretas para aquisição de medicamentos no Sistema Único de Saúde. Rev Saude Publica. 2011 Oct;45(5):906-13.
22. Instituto de Tecnologia em Fármacos. Tacrolimo [Internet]. [citado 2013 mai 2]. Disponível em: http://www.far.fiocruz.br/farmanguinhos/index.php?option=com_content&view=article&id=469&catid=53&Itemid=94
23. Ministério da Saúde (BR). Portal da Saúde. Brasil vai produzir mais 19 remédios e duas vacinas [Internet]. [citado 2013 mai 2]. Disponível em: http://portalsaude.saude.gov.br/portalsaude/noticia/7952/162/brasil-vai-produzir-mais-19-medicamentos-e-duas-vacinas.html
24. Ministério da Saúde (BR). Conselho Federal de Farmácia. Resolução no 357, de 20 de abril de 2001. Aprova o regulamento técnico das boas práticas de Farmácia. Diário Oficial da União, Brasília, p. 137, 26 set. 2013. Seção 1.
25. Angonesi D. Dispensação farmacêutica: uma análise de diferentes conceitos e modelos. Cien Saude Colet. 2008 abr;13Suppl:629-40.
 Endereço para correspondência:
Endereço para correspondência:
Daniel Emílio da Silva Almeida
- Rua Irmãos Kennedy, no 100,
Esplanada, Santa Luzia, Minas Gerais,
Brasil. CEP: 33015-0800
E-mail: daniel.almeidamg@gmail.com
Recebido em 29/11/2012
Aprovado em 28/10/2013
*O estudo recebeu o apoio financeiro do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) - processo no 5.76624/2008-0 - e da Secretaria de Estado de Saúde de Minas Gerais - processo no 1321127-173 (2007). Este manuscrito foi baseado na dissertação "Avaliação do processo de dispensação de imunossupressores para transplantados renais, SES/MG, 2008", defendida no Programa de Pós-Graduação em Saúde Pública da Faculdade de Medicina da Universidade Federal de Minas Gerais (UFMG), em 2012.












 Curriculum ScienTI
Curriculum ScienTI
