Introdução
As anomalias congênitas (ACs) são distúrbios de desenvolvimento de origem pré-natal presentes ao nascimento, e podem ser estruturais (deformidades físicas), funcionais (alterações neuromotoras) ou metabólicas (por exemplo, os erros inatos de metabolismo, fenilcetonúria, entre outros). Suas causas podem ser genéticas, ambientais ou multifatoriais.1,2 Na maioria dos casos, a etiologia permanece desconhecida e as causas ambientais (teratógenos) ainda são pouco estudadas, especialmente em países em desenvolvimento como o Brasil.1,3 Estima-se que as anomalias congênitas estão presentes em 2 a 3% dos nascidos vivos, e que podem chegar a 5% se as alterações diagnosticadas mais tardiamente, como as anomalias cardíacas, renais e pulmonares, forem contabilizadas.2 Entre 1980 e 2007, houve grande redução proporcional dos óbitos infantis secundários devidos a causas infecciosas e respiratórias, enquanto as ACs permaneceram estáveis, sendo estas a segunda causa de mortalidade infantil no Brasil.1,4 Semelhante fenômeno foi descrito em outro país latino-americano, o Chile, entre 2001 e 2010.5
O Sistema de Informações sobre Nascidos Vivos (Sinasc) foi instituído em 1990 pelo Ministério da Saúde com o objetivo de fornecer dados sobre os nascidos vivos, extraídos da Declaração de Nascido Vivo (DNV).6,7 A partir de 1999, foi incluído um campo na DNV para registro das ACs, codificadas conforme o Capítulo XVII da 10a Revisão da Classificação Estatística Internacional de Doenças e Problemas Relacionados com a Saúde (CID-10),3 o que torna o Sinasc um instrumento importante para monitoramento de ACs no Brasil.8
Com a emergência nacional causada pelo vírus Zika e sua associação com microcefalia,9 o serviço de vigilância epidemiológica do município de Tangará da Serra, Mato Grosso, Brasil, percebeu a importância de ter o registro do perímetro cefálico e do comprimento ao nascer dos nascidos vivos (dados até então ausentes da DNV) e instituiu, em todas as maternidades locais, a obrigatoriedade de seu registro manual a partir de 2016. Em 2017, a iniciativa foi estendida a todo o território nacional em atendimento à recomendação do Ministério da Saúde.
Na busca por compreender o comportamento das anomalias congênitas em Tangará da Serra nos últimos 11 anos (2006-2016), período que antecedeu a emergência da síndrome congênita por Zika (SCZ), bem como durante a ocorrência dessa doença com transmissão continuada do vírus, o presente estudo teve como objetivo descrever as anomalias congênitas em nascidos vivos de mães residentes em Tangará da Serra no período de 2006 a 2016.
Métodos
Trata-se de um estudo descritivo, com base nos dados da DNV e do Sinasc referentes ao período compreendido entre 1o de janeiro de 2006 e 31 de dezembro de 2016, consultados no segundo semestre de 2017. Foram incluídos todos os nascidos vivos residentes no município de Tangará da Serra, localizado na região sudoeste mato-grossense, a 240km de Cuiabá, capital do estado. A população local, estimada em 2017, era de 98.828 habitantes, com uma média anual de 1.445 nascidos vivos. Tangará da Serra é a principal cidade de sua microrregião e sexta maior de Mato Grosso, com cerca de 3% da população do estado;10 possui 211 estabelecimentos de saúde, públicos ou privados, inscritos no Cadastro Nacional de Estabelecimentos de Saúde (CNES). Entre esses estabelecimentos, encontram-se quatro hospitais, três com maternidade.11
Foram incluídos todos os nascidos vivos entre 1o de janeiro de 2006 e 31 de dezembro de 2016, com base em dados do Sinasc extraídos em 1o de setembro de 2017. O Sinasc é organizado a partir dos registros na Declaração de Nascido Vivo, feitos pelo profissional de saúde. Para esta análise, foram selecionadas as seguintes variáveis da DNV:
data de nascimento (dia, mês e ano);
sexo do nascido vivo (masculino; feminino);
peso ao nascer (em gramas: igual ou superior a 2.500g; inferior a 2.500g);
idade materna (em anos: menor que 35; 35 ou mais);
escolaridade materna (em anos de estudo: até 7; 8 a 11; 12 ou mais);
número de gestações anteriores (nenhuma; uma; duas; três ou mais);
número de filhos nascidos vivos (nenhum; um; dois; três ou mais);
número de perdas fetais (nenhuma; uma; duas ou mais);
duração da gestação (em semanas: menos de 36; 37 a 41; 42 ou mais);
tipo de gestação (única; dupla); e
presença de anomalias congênitas.
As anomalias congênitas são registradas em um campo especial na DNV. Esse campo permite o registro de uma ou mais anomalias congênitas. Cada diagnóstico deve ser informado tanto no formulário da DNV como no Sinasc. Compete ao médico diagnosticar os defeitos e/ou anomalias, bem como informar a quem preenche e/ou digita a DNV os códigos correspondentes, de acordo com a CID-10.3 O registro das informações no hospital pode ser dificultado pelo fluxo inadequado, especialmente quando diferentes pessoas coletam e preenchem os dados da DNV. Por isso, recomenda-se que o preenchimento da DNV seja feito até o momento da alta da mãe e por uma única pessoa. No caso de defeitos congênitos diagnosticados após a emissão da DNV, ou quando a confirmação diagnóstica laboratorial é tardia, é possível registrar o dado como ressalva e acrescentar a informação no banco de dados do Sinasc.
A análise estatística foi realizada utilizando-se o software Stata versão 13.0.12 Inicialmente, foram verificados os números anuais de nascidos vivos com qualquer anomalia congênita (isolada ou múltiplas) e sua prevalência por mil nascimentos. Logo, foram estimadas as prevalências de ACs (por mil nascimentos) por tipo, de acordo com a CID-10, para todo o período de 2006 a 2016, tendo como numerador o número de nascidos vivos com cada tipo/grupo de AC e como denominador o total de nascidos vivos no período. Foram calculadas as razões de prevalência (RP) e seus respectivos intervalos de confiança de 95% (IC95%), segundo características sociodemográficas, do parto e dos nascidos vivos.
O estudo foi realizado no âmbito das ações da Vigilância Epidemiológica do município de Tangará da Serra. Foram utilizados apenas dados secundários, sem identificação direta ou indireta das pessoas. Por seguir os padrões éticos definidos nas Resoluções do Conselho Nacional de Saúde (CNS) no 466, de 12 de dezembro de 2012, e no 510, de 7 de abril de 2016, o projeto do estudo foi dispensado de apreciação por Comitê de Ética em Pesquisa.
Resultados
Foram analisados 15.689 nascidos vivos de mães residentes no município de Tangará da Serra no período entre 2006 e 2016. Desses, 77 apresentaram alguma AC identificada até o momento da alta, representando uma prevalência de AC de 4,9/1.000 nascidos vivos.
A Figura 1 apresenta as prevalências do total de ACs entre os anos de 2006 e 2016. Chama a atenção que na década entre 2006 e 2015, os registros se mantiveram estáveis, embora houvesse um aumento de 80,7% na prevalência de ACs entre 2015 (5,7/1.000) e 2016 (10,3/1.000 nascidos vivos).
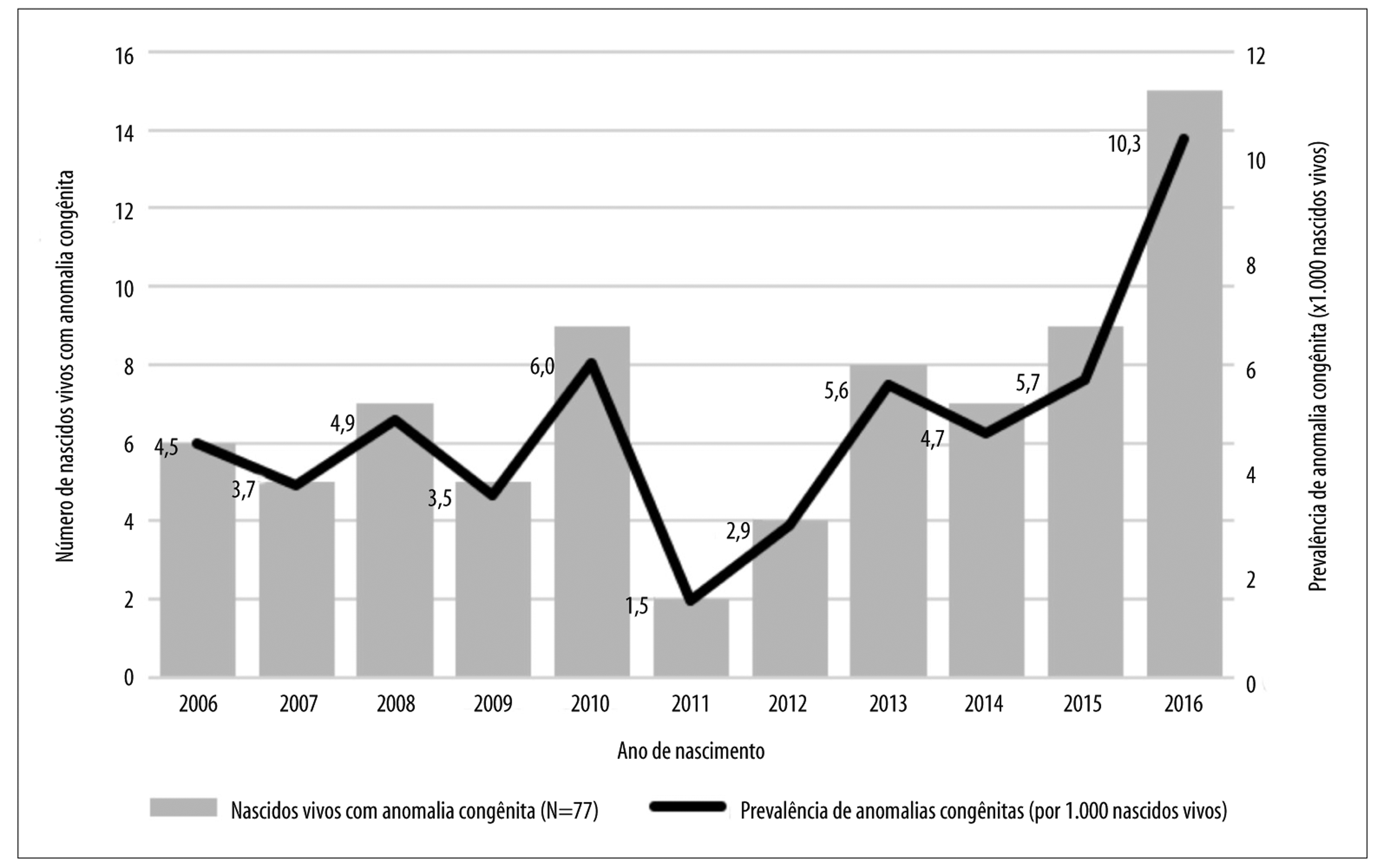
Fonte: Sistema de Informações sobre Nascidos Vivos (Sinasc); dados extraídos em 01/09/2017.
Figura 1 - Número de nascidos vivos com anomalia congênita e prevalência de anomalias congênitas (por 1.000 nascidos vivos), Tangará da Serra, Mato Grosso, 2006-2016
O número total de anomalias foi de 90, uma vez que sete nascidos vivos apresentavam mais de uma anomalia. As ACs do aparelho osteomuscular (27/90) foram as mais frequentes, seguidas pelas do sistema nervoso (23/90), aparelho digestivo (12/90), fenda labial e palatina (6/90) e cromossômicas (4/90). Entre as ACs do sistema osteomuscular, os diagnósticos mais registrados foram ‘pé torto’ (7/27) e polidactilia (5/27). Dos 23 registros de ACs do sistema nervoso, o diagnóstico mais encontrado foi de microcefalia, com seis registros - cinco deles apenas no ano de 2016 -, seguido de hidrocefalia (5/23), anencefalia (3/23), espinha bífida (2/23) e encefalocele (2/23) (Tabela 1).
Tabela 1 - Distribuição e prevalência dos tipos de malformações congênitas ao nascer segundo a 10a Revisão da Classificação Estatística Internacional de Doenças e Problemas Relacionados à Saúde, Tangará da Serra, Mato Grosso, 2006-2016
| Grupo de doença | Nascidos vivos com anomalias congênitas | Prevalência de anomalias congênitas ao nascer (por 1.000 nascidos vivos) |
|---|---|---|
| n | ||
| Malformações congênitas e deformidades do aparelho osteomuscular | 27 | 1,72 |
| ‘Pé torto’ | 7 | 0,45 |
| Polidactilia não especificada | 5 | 0,32 |
| Malformações congênitas não especificadas de membro | 3 | 0,19 |
| Gastrosquise | 3 | 0,19 |
| Deformidade congênita não especificada | 3 | 0,19 |
| Hérnia diafragmática congênita | 1 | 0,06 |
| Outras deformidades congênitas do pé | 1 | 0,06 |
| Ausência congênita da mão e de dedo(s) | 1 | 0,06 |
| Nanismo tanatofórico | 1 | 0,06 |
| Outras deformidades congênitas do crânio, da face e da mandíbula | 1 | 0,06 |
| Sindactilia não especificada | 1 | 0,06 |
| Malformações congênitas do sistema nervoso | 23 | 1,47 |
| Microcefalia | 6 | 0,38 |
| Hidrocefalia congênita não especificada | 5 | 0,32 |
| Anencefalia | 3 | 0,19 |
| Espinha bífida não especificada | 2 | 0,13 |
| Outras síndromes com malformações congênitas com outras alterações do esqueleto | 2 | 0,13 |
| Encefalocele não especificada | 2 | 0,13 |
| Holoprosencefalia | 1 | 0,06 |
| Síndrome de Arnold-Chiari | 1 | 0,06 |
| Hipoplasia e displasia da medula espinal | 1 | 0,06 |
| Malformações congênitas do aparelho digestivo | 12 | 0,76 |
| Malformações congênitas dos lábios | 5 | 0,32 |
| Ausência, atresia e estenose congênita | 2 | 0,13 |
| Malformação congênita não especificada | 1 | 0,06 |
| Outras malformações congênitas da boca | 1 | 0,06 |
| Ausência, atresia e estenose congênita | 1 | 0,06 |
| Malformação congênita não especificada | 1 | 0,06 |
| Atresia de esôfago com fístula traqueoesofágica | 1 | 0,06 |
| Fenda labial e fenda palatina | 6 | 0,38 |
| Fenda palatina não especificada | 3 | 0,19 |
| Fenda do palato com fenda labial | 3 | 0,19 |
| Malformações congênitas do aparelho circulatório | 4 | 0,25 |
| Malformação não especificada no coração | 2 | 0,13 |
| Comunicação interventricular | 1 | 0,06 |
| Síndrome do coração esquerdo hipoplásico | 1 | 0,06 |
| Outras malformações congênitas | 4 | 0,25 |
| Malformações congênitas múltiplas, não classificadas em outra parte | 2 | 0,13 |
| Síndromes com malformações congênitas afetando predominantemente o aspecto da face | 1 | 0,06 |
| Outras malformações congênitas especificadas do intestino | 1 | 0,06 |
| Anomalias cromossômicas, não classificadas em outra parte | 4 | 0,25 |
| Síndrome de Down não especificada | 4 | 0,25 |
| Malformações congênitas do aparelho osteomuscular | 4 | 0,25 |
| Outras malformações congênitas do aparelho osteomuscular | 2 | 0,13 |
| Ausência congênita e hipoplasia da artéria umbilical | 1 | 0,06 |
| Malformação congênita não especificada | 1 | 0,06 |
| Malformações congênitas do aparelho respiratório | 3 | 0,19 |
| Hipoplasia e displasia do pulmão | 2 | 0,13 |
| Fissura, entalhe ou fenda nasal | 1 | 0,06 |
| Malformações congênitas do aparelho urinário | 1 | 0,06 |
| Agenesia renal não especificada | 1 | 0,06 |
| Malformações congênitas do olho, do ouvido, da face e do pescoço | 1 | 0,06 |
| Malformação congênita não especificada | 1 | 0,06 |
| Malformações congênitas do órgão genital | 1 | 0,06 |
| Hipospádia peniana | 1 | 0,06 |
Fonte: Sistema de Informações sobre Nascidos Vivos (Sinasc); dados extraídos em 01/09/2017.
A Tabela 2 apresenta a distribuição dos nascidos vivos com ACs por tipo de anomalia e ano de nascimento, incluídas as dez ACs mais frequentes no período. De 2006 a 2015, apenas um caso de microcefalia havia sido registrado no município, enquanto no ano seguinte, 2016, foram notificados nada menos que cinco casos, todos de microcefalia grave.
Tabela 2 - Número de nascidos vivos com anomalia congênita, por tipo de anomalia e ano de nascimento, Tangará da Serra, Mato Grosso, 2006-2016
| Tipo de anomalia congênita | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | Total |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pé torto | - | - | 1 | - | 1 | 1 | - | 2 | 1 | - | 1 | 7 |
| Microcefalia | - | - | - | - | - | - | - | - | 1 | - | 5 | 6 |
| Malformações dos lábios | - | - | 1 | 1 | 1 | - | - | - | - | 2 | - | 5 |
| Polidactilia | 2 | - | - | - | - | - | - | - | 1 | - | 2 | 5 |
| Hidrocefalia congênita | - | 1 | - | - | 1 | - | - | - | 1 | - | 1 | 4 |
| Malformações de membro | - | - | 1 | - | - | - | 1 | - | - | 1 | 1 | 4 |
| Síndrome de Down | - | 1 | - | 2 | - | - | - | 1 | - | - | - | 4 |
| Fenda palatina | 1 | - | - | - | 1 | - | - | - | 1 | - | - | 3 |
| Anencefalia | - | - | - | - | - | - | - | 1 | 1 | 1 | - | 3 |
| Gastrosquise | 1 | 1 | 1 | - | - | - | - | - | - | - | - | 3 |
Fonte: Sistema de Informações sobre Nascidos Vivos (Sinasc); dados extraídos em 01/09/2017.
Nota: A tabela inclui as dez anomalias congênitas mais frequentes no período de 2006 a 2016.
Quanto às características maternas e dos nascidos vivos, as RP de ACs foram maiores entre os filhos de mulheres com idade superior a 35 anos, em relação àquelas com menos de 35 anos (RP=1,91; IC95% 1,01;3,60), entre crianças prematuras, na comparação com as nascidas a termo (RP=2,22; IC95% 1,26;3,92), e naquelas com peso ao nascer inferior a 2.500g (RP=3,21; IC95% 1,86;5,54) (Tabela 3).
Tabela 3 - Frequência de nascidos vivos e prevalência de anomalia congênita ao nascer, segundo características sociodemográficas, do parto e dos nascidos vivos, Tangará da Serra, Mato Grosso, 2006-2016
| Variável | Total de nascidos vivos (N= 15.689) | Nascidos vivos com anomalias congênitas | Prevalência de anomalias congênitas ao nascer (por 1.000 nascidos vivos) | Razão de prevalência | Valor de p | |||
|---|---|---|---|---|---|---|---|---|
| n | % | Prevalência | IC95% | RPa | IC95% b | |||
| Faixa etária (em anos) (n= 15.689) | 0,046 | |||||||
| <35 | 14.429 | 66 | 85,7 | 4,6 | 3,6;5,8 | 1,00 | ||
| ≥35 | 1.260 | 11 | 14,3 | 8,7 | 4,8;15,7 | 1,91 | 1,01;3,60 | |
| Escolaridade (em anos de estudo) (n= 15.668) | 0,456 | |||||||
| ≤7 | 3.609 | 18 | 24,0 | 5,0 | 3,1;7,9 | 1,00 | ||
| 8-11 | 8.719 | 37 | 49,3 | 4,2 | 3,1;5,9 | 0,85 | 0,49;1,49 | |
| ≥12 | 3.340 | 20 | 26,7 | 6,0 | 3,9;9,3 | 1,20 | 0,64;2,27 | |
| Número de gestações anteriores (n= 14.646) | 0,775 | |||||||
| Nenhuma | 5.270 | 28 | 36,3 | 5,3 | 3,7;7,7 | 1,00 | ||
| Uma | 4.637 | 24 | 31,2 | 5,2 | 3,5;7,7 | 0,97 | 0,57;1,68 | |
| Duas | 2.580 | 11 | 14,3 | 4,3 | 2,4;7,7 | 0,80 | 0,40;1,61 | |
| Três ou mais | 2.159 | 14 | 18,2 | 6,5 | 3,8;10,9 | 1,22 | 0,64;2,31 | |
| Número de filhos vivos (n= 14.519) | 0,354 | |||||||
| Nenhum | 5.836 | 36 | 46,7 | 6,2 | 4,5;8,5 | 1,00 | ||
| Um | 4.804 | 18 | 23,4 | 3,7 | 2,4;5,9 | 0,61 | 0,35;1,07 | |
| Dois | 2.381 | 14 | 18,2 | 5,9 | 3,5;9,9 | 0,95 | 0,52;1,76 | |
| Três ou mais | 1.498 | 9 | 11,7 | 6,0 | 3,1;11,5 | 0,97 | 0,47;2,02 | |
| Número de perdas fetais (n= 13.526) | 0,582 | |||||||
| Nenhuma | 11.206 | 61 | 79,2 | 5,4 | 4,2;7,0 | 1,00 | ||
| Uma | 1.907 | 14 | 18,2 | 7,3 | 4,4;12,4 | 1,35 | 0,76;2,41 | |
| Duas ou mais | 413 | 2 | 2,6 | 4,8 | 1,2;19,2 | 0,89 | 0,22;3,63 | |
| Duração da gestação (em semanas) (n= 15.667) | 0,014 | |||||||
| <37 | 1.621 | 15 | 20,0 | 9,3 | 5,6;15,3 | 2,22 | 1,26;3,92 | |
| 37-41 | 13.693 | 57 | 76,0 | 4,2 | 3,2;5,4 | 1,00 | ||
| ≥42 | 353 | 3 | 4,0 | 8,5 | 2,7;26,1 | 2,04 | 0,64;6,49 | |
| Tipo de gestação (n= 15.668) | 0,238 | |||||||
| Única | 15.376 | 74 | 96,1 | 4,8 | 3,8;6,0 | 1,00 | ||
| Dupla | 312 | 3 | 3,9 | 9,6 | 3,1;29,4 | 2,00 | 0,63;6,30 | |
| Sexo da criança (n= 15.689) | 0,648 | |||||||
| Masculino | 7.946 | 41 | 53,3 | 5,2 | 3,8;7,0 | 1,00 | ||
| Feminino | 7.743 | 36 | 46,7 | 4,6 | 3,4;6,4 | 0,90 | 0,58;1,41 | |
| Peso ao nascer (n= 15.688) | <0,001 | |||||||
| <2.500g | 1.186 | 16 | 20,8 | 13,5 | 8,3;21,9 | 3,21 | 1,86;5,54 | |
| ≥2.500g | 14.502 | 61 | 79,2 | 4,2 | 3,3;5,4 | 1,00 | ||
a) RP: razão de prevalência.
b) IC95%: intervalo de confiança de 95%.
Fonte: Sistema de Informações sobre Nascidos Vivos (Sinasc); dados extraídos em 01/09/2017.
Discussão
Foram avaliadas, retrospectivamente, as prevalências anuais de ACs registradas pelo Sinasc, entre 2006 e 2016, em um município no estado do Mato Grosso no Centro-Oeste brasileiro, onde ocorreu um surto de Zika vírus no final do ano de 2015 e início de 2016. A epidemia pelo vírus Zika (ZIKV), reconhecido teratógeno em humanos, enfatizou a importância do estabelecimento de protocolos de vigilância de ACs em países em desenvolvimento. A Organização Mundial da Saúde (OMS) preconiza como responsabilidade de cada país estabelecer protocolos e regulamentos para vigilância de ACs,13 responsáveis pelos 276 mil óbitos neonatais precoces por anomalia congênita no mundo, a cada ano.14
Na Europa, foi criada em 1979 a European Surveillance of Congenital Anomalies (Eurocat), uma rede de registros populacionais para a vigilância epidemiológica de ACs, com 23 países integrantes.15
Nas Américas, existem registros de ACs em diversos países, como Argentina, Brasil, Canadá, Chile, Colômbia, Costa Rica, México e Uruguai, além do Estudo Colaborativo Latino-Americano de Malformações Congênitas (ECLAMC), o qual reúne hospitais de diversos países da América do Sul. Nos Estados Unidos, o apontamento - de base estadual - é obrigatório e o serviço hospitalar repassa os dados de nascimentos com ACs e óbitos fetais por ACs mediante formulário padronizado. A maioria desses dados são reportados a instâncias maiores, como a International Clearinghouse for Birth Defects and Monitoring Systems (ICBDMS), encarregadas de uma vigilância internacional.16
No Brasil, a notificação é obrigatória desde 1999 e é feita no preenchimento da DNV; disponibilizados no Sinasc, seus dados permitem a monitoração das ACs.6,7
Em Mato Grosso, a cobertura do Sinasc entre os anos 2000 e 2012 foi de 94,9%, considerada satisfatória e com tendência de aumento17 acima da média do Brasil, de 92%.4
A frequência estimada de ACs é de 2 a 3% em nascidos vivos. O ECLAMC registra 2,73% dos nascidos vivos na América Latina com ACs, enquanto nos países europeus cobertos pela rede EUROCAT, essa média é de 9,5/1.000 nascimentos vivos e de 0,9/1.000 óbitos perinatais. Essas diferenças entre as frequências na América Latina e na Europa devem-se, em grande parte, à realização eletiva de interrupções da gestação (abortos eletivos) por anomalias fetais. Quando os registros incluem essas anomalias, a frequência de ACs chega a 2% nos países europeus.2,14
No Brasil, anualmente, são registrados em torno de 2,9 milhões de nascidos vivos e espera-se que aproximados 90 mil apresentem algum tipo de AC, se consideramos a prevalência estimada de 3% para a espécie humana.6 Entretanto, estudos baseados nos dados do Sinasc nos municípios do Rio de Janeiro, RJ, e de São Paulo, SP, apresentaram, respectivamente, frequência de 1,7% e 1,6% de AC nos nascidos vivos,6,18 valores superiores ao encontrado no presente estudo. Em Maringá, PR, e no Vale do Paraíba paulista, os dados se assemelham: respectivamente 0,7% e 0,76% de AC em nascidos vivos, próximos do observado neste trabalho, de 0,7.19,20 A questão do sub-registro de AC na DNV já foi investigada por Luquetti e Koifmann8 em oito hospitais de João Pessoa, PB, Salvador, BA, São Paulo e Campinas, SP, Belo Horizonte, MG, e Florianópolis e Joinville, SC.8 Em seu trabalho, no qual foi adotado como padrão ouro o ECLAMC, as autoras observaram, nesses hospitais, sub-registro de pelo menos 40% das ACs no Sinasc, nos anos de 2004 e 2007. Costa et al. (2008)18 também realizaram estudo de comparação do Sinasc com registros hospitalares dos nascidos vivos no estado do Rio de Janeiro no ano de 2004 e encontraram variabilidade de concordância entre o Sinasc e os registros hospitalares, dependendo do tipo de AC, sendo as taxas de concordância maiores em ACs do sistema osteomuscular.
Em Tangará da Serra, pode-se atribuir o sub-registro, principalmente, à falta de detecção de ACs de órgãos internos, como cardiopatias congênitas21 ou outras cujas características clínicas sejam menos visíveis ao nascimento.22 O predomínio de anomalias congênitas do sistema osteomuscular pode estar relacionado ao fato de incluir anomalias frequentes, como ‘pé torto’ e polidactilia, ademais de a maioria das anomalias desse sistema ser facilmente visível ao nascimento.2,6
Chama a atenção o aumento de ACs no ano de 2016, com a ocorrência de cinco nascimentos de crianças com microcefalia, comparativamente a apenas um caso registrado em todos os anos anteriores. Este resultado poderia decorrer de um maior registro após a incorporação da medida do perímetro cefálico na DNV. Entretanto, os cinco casos notificados eram de microcefalias graves, observáveis clinicamente, mesmo sem a ajuda de fita métrica. Posteriormente, esses cinco casos foram todos avaliados e registrados como compatíveis com a síndrome congênita de Zika. Esta observação sincroniza com a ocorrência do surto infeccioso por ZIKV no município, entre o final de 2015 e o início de 2016. No Brasil, os casos de microcefalia mantiveram-se estáveis de 2000 a 2014, com prevalência de 2/10 mil nascidos vivos, alterando-se significativamente a partir de 2015, com 54,6/10 mil nascidos vivos.7 Parte desse aumento é atribuída à adoção de critérios de inclusão de microcefalia mais amplos, como o perímetro cefálico entre -2 e -3 escores Z. Outrossim, a medida de perímetro cefálico é muitas vezes sujeita a viés, seja por erros na aferição, seja porque é realizada antes de a criança completar 24 horas de vida.23 Não obstante tais obliquidades, a utilização de dados do Sinasc foi fundamental para a confirmação de um aumento anormal e súbito de casos de microcefalia no Nordeste, no final de 2015.7 Em Mato Grosso como um todo, entre as semanas epidemiológicas 45/2015 e 35/2017, o estado registrou 386 notificações de casos de microcefalia, dos quais 19% confirmados como casos de síndrome de Zika congênita.24
No presente estudo, a razão de prevalência de ACs foi maior em nascidos vivos de mães com mais de 35 anos de idade. Trata-se de um efeito esperado, pois a idade materna é o principal fator de risco para anomalias cromossômicas.2,6,17 É também importante observar que foram registrados três casos de gastrosquise, anomalia mais frequente nos filhos de mães mais jovens. Mais ainda: aparentemente, existe uma tendência temporal mundial de aumento dessa AC a partir dos anos 1980, confirmada em registros norte-americanos.25 Peso inferior a 2.500g e prematuridade também foram fatores associados às anomalias congênitas, o que era de se esperar: defeitos congênitos, com frequência, são associados a esses desfechos.3,6,8
Como limitações adicionais do presente estudo, destaca-se a incompletude no preenchimento da DNV e a indisponibilidade de exames complementares na assistência pré-natal, para diagnóstico precoce das ACs.
Considerando-se a carência de estudos sobre ACs no Brasil, principalmente na região Centro-Oeste, os resultados apresentados por esta pesquisa poderão contribuir no planejamento das ações em Saúde Pública, direcionar e aprofundar discussões no que concerne à ampliação de ações nas políticas públicas para as ACs e todos os atores envolvidos nesse processo: familiares, amigos, profissionais e sociedade geral. Entre essas ações, destaca-se a importância do treinamento e conscientização dos profissionais quanto ao preenchimento da DNV, cujos dados sobre ACs, uma vez incluídos no Sinasc, constituem importante ferramenta para detecção de alterações nas frequências temporais ou espaciais das anomalias congênitas, a exemplo da ocorrência de microcefalia por infecção materna pelo vírus Zika.











 texto em
texto em 
 Curriculum ScienTI
Curriculum ScienTI

