Introdução
No contexto histórico, com o prestígio de haver salvado milhares de vidas, a vacinação em massa foi e é considerada uma das grandes conquistas da saúde pública, desde pesquisas fundamentais desenvolvidas em fins do século XIX, até os estudos e a implementação de programas de imunização nacionais nos dias atuais.1 Não obstante as evidências de anos de altas coberturas vacinais (>95%), em 2016, o Brasil apresentou um declínio vacinal de aproximadamente 10 a 20 pontos percentuais.2
As estimativas da cobertura vacinal são geralmente efetuadas pelo método indireto ou administrativo: toma-se para (i) o numerador, os dados agregados, com o total de doses aplicadas ou distribuídas, e para (ii) o denominador, uma estimativa populacional. Este método é útil para o planejamento das ações dos programas de imunização, porém bastante frágil em termos de acurácia.3 Da mesma forma que os inquéritos de cobertura vacinal, os registros informatizados de imunização permitem obter dados individuais da população vacinada e identificar microáreas de baixa cobertura, ou seja, bolsões de suscetíveis.3,4
O uso desse instrumento é antigo. Canadá, Reino Unido e Estados Unidos possuem registros informatizados de imunização desde a década de 1970.5 A partir de 2006, países da América Latina iniciaram a implantação de registros informatizados de imunização de abrangência nacional para aprimorar as estimativas das coberturas vacinais; à exceção do México e do Uruguai, que utilizam tal instrumento desde 1987 e 1991 respectivamente.6
No Brasil, os registros informatizados do Programa Nacional de Imunizações (PNI), reunidos pelo Sistema de Informação do PNI (SI-PNI), vêm-se desenvolvendo desde a década de 1990. Apenas a partir da década de 2010, o SI-PNI vem sendo implantado em todo o território nacional.7
Anteriormente à consecução do SI-PNI, algumas iniciativas municipais já existiam no país, a exemplo do Serviço Especial de Saúde de Araraquara (SESA), da Universidade de São Paulo (USP). Município do interior do estado de São Paulo, Araraquara conta com os registros de imunização informatizados desde 1987. Hoje denominado Sistema Juarez, o SESA é, provavelmente, o mais antigo serviço desse caráter no Brasil.5 Alguns estudos já foram realizados utilizando dados do Sistema Juarez,8-10 entretanto seu potencial para analisar a distribuição espacial das coberturas vacinais, bem como a validação desse sistema em relação aos dados constantes nas cadernetas de vacinação, ainda não foi explorado.
O objetivo desse artigo foi descrever a concordância entre os dados de imunização do Sistema Juarez e as informações da caderneta de vacinação e as coberturas vacinais em crianças aos 12 e aos 24 meses.
Métodos
Trata-se de estudo descritivo, com análise de dados secundários do Sistema Juarez e dados primários do inquérito domiciliar realizado no município de Araraquara, SP, em 2018.
Araraquara apresentava 236.072 habitantes em 2019, com aproximadamente 3 mil nascidos vivos por ano e taxa de mortalidade infantil de 10,46 óbitos por 1 mil nascidos vivos;11 seu índice de desenvolvimento humano municipal (IDH) é de 0,81512 e 97,2% da população está situada na área urbana.13 O município possuía, em 2020, 34 unidades de saúde, três hospitais gerais, dois prontos-socorros, um hospital psiquiátrico e um ambulatório de especialidades, com cerca de 60% da população local sob cobertura. O município também conta com um programa de vacinação identificado por altas coberturas vacinais, refletidas no controle das doenças imunopreveníveis desde a década de 1990.14
Localizado no município, o SESA/USP tem seus registros de imunização informatizados desde 1987, quando já contava com o registro vacinal individualizado da criança, nome completo do pai e da mãe, nome e data de aplicação da vacina, eventos adversos pós-vacinação, entre outras informações, tendo-se aprimorado nesse sentido, ao longo do tempo. Em 2011, o registro de imunização informatizado implementou um prontuário eletrônico de saúde municipal que inclui, além do registro nominal de vacina, dados de consultas e registro de doenças de notificação compulsória. Naquele mesmo ano, o SESA passou a se chamar Sistema Juarez, tornou-se online a partir de 2012 e, desde então, todas as unidades de saúde acessam e registram dados de vacinação em tempo real, no sistema, cuja cobertura é de 99,6% das crianças nascidas no município.9 Pelo Sistema Juarez, são verificados os esquemas de vacinação dos indivíduos nele cadastrados, com data e lote de cada dose de vacina administrada.
O objeto do estudo constituiu-se de crianças nascidas e residentes em Araraquara no ano de 2015, cadastradas no Sistema Juarez. Foram excluídas as crianças cujas mães não apresentaram caderneta de vacinação da criança durante o inquérito vacinal, realizado com amostra probalilística extraída do Sistema Juarez mediante sorteio sem reposição. Cada uma das 15 áreas de ponderação do Instituto Brasileiro de Geografia e Estatística (IBGE) foi considerada um estrato da amostra:15 houve coleta de dados em todos os 15 estratos, mediante entrevistas com as mães de 3.394 crianças nascidas naquele ano e residentes no município, proporcionalmente distribuídas entre as áreas ponderadas pelo IBGE.
Para o cálculo do tamanho amostral mínimo, considerou-se: nível de confiança de 95%, cujo valor foi de 1,96 para um alfa de 0,05; frequência da cobertura vacinal de 40%, com base no estudo de Ferreira et al.9 que analisou a cobertura vacinal de 49.741 crianças menores de 2 anos, nascidas de 1998 a 2013 em Araraquara; e erro máximo em valor absoluto de 0,05.16 Assim, obteve-se um tamanho amostral mínimo de 369 crianças.
De um total de 3.394 crianças cadastradas no Sistema Juarez em 2015, 3.054 tiveram seus endereços geocodificados e categorizados em suas respectivas áreas de ponderação do IBGE,15 de maneira a compor a população final para a amostra aleatória (Figura 1). A partir dessa população final, foram sorteadas 450 crianças; foram acrescentados 20% do tamanho mínimo amostral calculado, para compensar possíveis perdas.
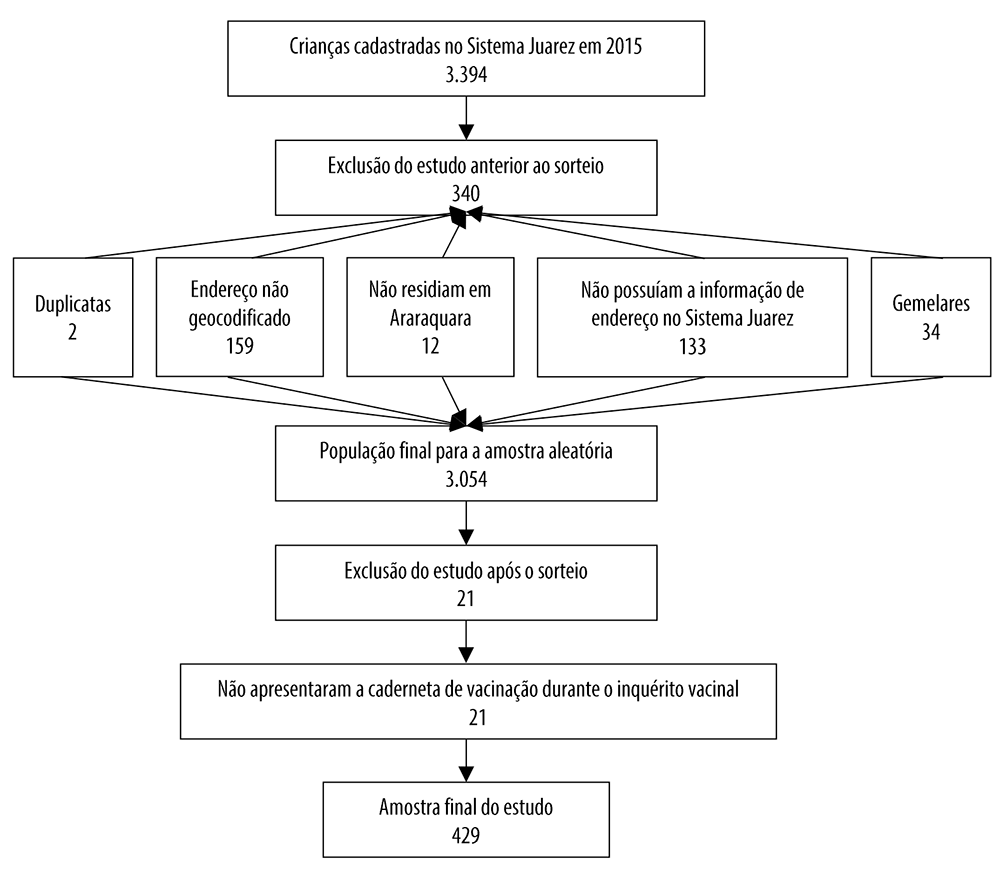
Figura 1 Processo de recrutamento e exclusão das crianças menores de 2 anos de idade, Araraquara, São Paulo, 2018
Na avaliação da completude do esquema vacinal, foram contempladas as seguintes recomendações de esquema vacinal pelo PNI:17
-
Esquema vacinal completo aos 12 meses de idade
- uma dose da vacina com o bacilo de Calmette-Guérin (BCG);
- três doses da vacina de difteria, tétano e coqueluche (DPT), Haemophilus influenzae tipo B (Hib) e hepatite B (HEP B) (pentavalente);
- três doses da vacina de poliomielite inativada (VIP);
- duas doses e um reforço da vacina pneumocócica 10 valente;
- duas doses da vacina de rotavírus humano;
- duas doses e um reforço da vacina meningocócica C (conjugada);
- uma dose da vacina de febre amarela; e
- uma dose da vacina de sarampo, caxumba e rubéola (SCR) - tríplice viral.
-
Esquema vacinal completo aos 24 meses de idade
- esquema vacinal completo aos 12 meses e reforço da vacina DTP;
- reforço da vacina de poliomielite atenuada (VOP);
- uma dose da vacina de hepatite A; e
- uma dose da vacina tetraviral - SCR e varicela.
Foram consideradas como doses válidas aquelas administradas respeitando-se as idades, mínima e máxima, de aplicação da dose, assim como o intervalo adequado entre as doses para vacinas com esquema multidose (Figura 2).
Figura 2 Critérios de avaliação de idade mínima e preconizada e intervalos entre doses de vacinas para crianças até 24 meses de idade, segundo o calendário vigente, Araraquara, São Paulo, 2015
| Vacina | Dose | Idade mínima | Intervalo até a próxima dose | Intervalo mínimo até a próxima dose | Atraso (a partir do) |
|---|---|---|---|---|---|
| Bacilo de Calmette-Guérin | 1 | Ao nascer | - | - | 2º mês |
| Poliomielite atenuada/ poliomielite inativada | 1 | 6 semanas | 2 meses | 4 semanas | 3º mês |
| 2 | 10 semanas | 2 meses | 4 semanas | 5º mês | |
| 3 | 14 semanas | 9 meses | 6 meses | 7º mês | |
| Reforço | 6 meses após a 3ª dose | - | - | 16º mês | |
| Difteria, tétano e coqueluche | 1 | 6 semanas | 2 meses | 4 semanas | 3º mês |
| 2 | 10 semanas | 2 meses | 4 semanas | 5º mês | |
| 3 | 14 semanas | 9 meses | 6 meses | 7º mês | |
| Reforço | 12 meses | - | - | 16º mês | |
| Haemophilus influenzae tipo B | 1 | 6 semanas | 2 meses | 4 semanas | 3º mês |
| 2 | 10 semanas | 2 meses | 4 semanas | 5º mês | |
| 3 | 14 semanas | - | - | 7º mês | |
| Hepatite B | 1 | Ao nascer | 2 meses | 4 semanas | 2º mês |
| 2 | 4 semanas | 4 meses | 8 semanas | 3º mês | |
| 3 | 24 semanas | - | - | 7º mês | |
| Rotavírus humano | 1 | 6 semanas | 2 meses | 4 semanas | 3º mês |
| 2 | 10 semanas | - | - | 5º mês | |
| Febre amarela | 1 | 9 meses | - | - | 10º mês |
| Tríplice viral | 1 | 12 meses | - | - | 13º mês |
| Pneumocócica 10 valentea | 1 | 6 semanas | 2 meses | 4 semanas | 3º mês |
| 2 | 10 semanas | 2 meses | 4 semanas | 5º mês | |
| Reforço | 12 meses | - | - | 16º mês | |
| Meningocócica C | 1 | 6 semanas | 2 meses | 4 semanas | 4º mês |
| 2 | 10 semanas | 7 meses | 8 semanas | 6º mês | |
| Reforço | 12 meses | - | - | 13º mês | |
| Hepatite A | 1 | 12 meses | - | - | 16º mês |
a) Até 2015, eram recomendadas 3 doses da vacina Pneumocócica 10 valente antes dos 12 meses de idade, entretanto, em 2016, houve uma mudança no calendário vacinal e passou-se a orientar a aplicação de apenas duas doses antes dos 12 meses de idade (1ª e 2ª dose, respectivamente).
A coleta de dados do inquérito vacinal aconteceu no período de agosto a outubro de 2018, mediante questionário aplicado em domicílio, por 10 entrevistadores de campo e quatro supervisores, os quais foram submetidos a um treinamento teórico-prático com carga horária de 10 horas, distribuídas em dois dias consecutivos. Previamente, realizou-se um estudo-piloto para adequação do instrumento, envolvendo 20 mães do município de Araraquara não incluídas no estudo. Os dados secundários foram obtidos do Sistema Juarez.
Foram verificados os níveis de concordância entre os dados de vacinação do Sistema Juarez e as informações da caderneta de vacinação coletadas no inquérito vacinal, pelo teste de Kappa, categorizado da seguinte forma: concordância quase perfeita quando o coeficiente Kappa foi ≥0,80; concordância substancial, 0,60 a 0,79; concordância moderada, 0,41 a 0,59; concordância regular, 0,21 a 0,40; e concordância ruim, quando o coeficiente Kappa foi <0,20.
O Sistema de Informação Geográfica foi utilizado para a descrição espacial dos dados de coberturas vacinais, calculadas para cada uma das 15 áreas de ponderação do município e utilizadas no desenho de mapas com sua distribuição. Para tanto, empregou-se o software QGIS 3.4.1 sobre base cartográfica do IBGE.18
O estudo em tela faz parte de um projeto maior, denominado ‘Hesitação materna em vacinar e a situação vacinal de crianças de até 2 anos de idade’, realizado em 2018. Ele foi novamente aprovado, desta vez pelo Comitê de Ética em Pesquisa da Faculdade de Saúde Pública da Universidade de São Paulo (CEP/FSP/USP): Parecer nº 3.617.912, de 3 de outubro de 2019; Certificado de Apresentação para Apreciação Ética (CAAE) nº 20721819.0.0000.5421. Foram incluídas no estudo apenas as crianças cujas mães assinaram o Termo de Consentimento Livre e Esclarecido antes do início da entrevista-base do inquérito vacinal.
Resultados
Do total de 450 crianças admitidas no estudo, 4,7% foram excluídas: 429 crianças compuseram a amostra final (Figura 1).
Verificou-se concordância entre as duas fontes de dados, em proporção variável de 84,1 a 99,1%. Houve mais doses registradas no cartão de vacinas do que no Sistema Juarez, sendo essa diferença menor que 5% para a maioria das vacinas (74,1%) (Tabela 1).
Tabela 1 Número de crianças vacinadas e concordância entre cadernetas de vacinação e Sistema Juarez (n=429), Araraquara, São Paulo, 2015
| Vacina | Caderneta de vacinação | Sistema Juarez | Diferença (%) | Concordância (%) | Coeficiente Kappa | p-valora |
|---|---|---|---|---|---|---|
| BCGb | 428 | 429 | -0,2 | 97,9 | 0,9 | <0,001 |
| Hepatite B ao nascer | 429 | 427 | 0,5 | 97,4 | 0,9 | <0,001 |
| DTPc/Hibd/hepatite B - 1ª dose | 429 | 427 | 0,5 | 98,1 | 0,9 | <0,001 |
| DTPc/Hibd/hepatite B - 2ª dose | 428 | 418 | 2,3 | 95,6 | 0,9 | <0,001 |
| DTPc/Hibd/hepatite B - 3ª dose | 426 | 422 | 0,9 | 94,1 | 0,9 | <0,001 |
| DTPc - Reforço | 415 | 406 | 2,1 | 92,2 | 0,9 | <0,001 |
| Poliomielite - 1ª dose | 429 | 426 | 0,7 | 99,1 | 0,9 | <0,001 |
| Poliomielite - 2ª dose | 428 | 423 | 1,2 | 97,2 | 0,9 | <0,001 |
| Poliomielite - 3ª dose | 426 | 420 | 1,4 | 94,8 | 0,9 | <0,001 |
| Poliomielite - Reforço | 417 | 487 | -16,3 | 92,4 | 0,9 | <0,001 |
| Rotavírus - 1ª dose | 424 | 421 | 0,7 | 97,8 | 0,9 | <0,001 |
| Rotavírus - 2ª dose | 414 | 411 | 0,7 | 96,6 | 0,9 | <0,001 |
| Pneumococo - 1ª dose | 429 | 425 | 0,9 | 97,9 | 0,9 | <0,001 |
| Pneumococo - 2ª dose | 426 | 423 | 0,7 | 97,2 | 0,9 | <0,001 |
| Pneumococo - reforço | 424 | 391 | 7,7 | 84,1 | 0,8 | <0,001 |
| Meningococo - 1ª dose | 425 | 424 | 0,2 | 95,5 | 0,9 | <0,001 |
| Meningococo - 2ª dose | 422 | 422 | 0,0 | 92,8 | 0,9 | <0,001 |
| Meningococo - Reforço | 413 | 404 | 2,1 | 94,6 | 0,9 | <0,001 |
| Febre amarela | 423 | 414 | 2,1 | 93,9 | 0,9 | <0,001 |
| Hepatite A | 427 | 409 | 4,2 | 93,6 | 0,9 | <0,001 |
| Sarampo/caxumba/rubéola - 1ª dose | 427 | 414 | 3,0 | 94,7 | 0,9 | <0,001 |
| Sarampo/caxumba/rubéola - 2ª dose | 354 | 381 | -6,3 | 92,6 | 0,9 | <0,001 |
| Varicela | 393 | 379 | 3,3 | 95,7 | 0,9 | <0,001 |
a) p-valor do teste de Kappa; b) BCG: bacilo de Calmette-Guérin; c) DTP: difteria, tétano e coqueluche; d) Hib: haemophilus influenzae tipo B.
O município de Araraquara apresentou coberturas vacinais de 86,1 a 100%. Ao se considerar o esquema completo, a cobertura da completude vacinal aos 12 meses de idade foi de 77,1%, enquanto para a completude vacinal aos 24 meses de idade, essa cobertura foi de 68,8% (Figura 3).
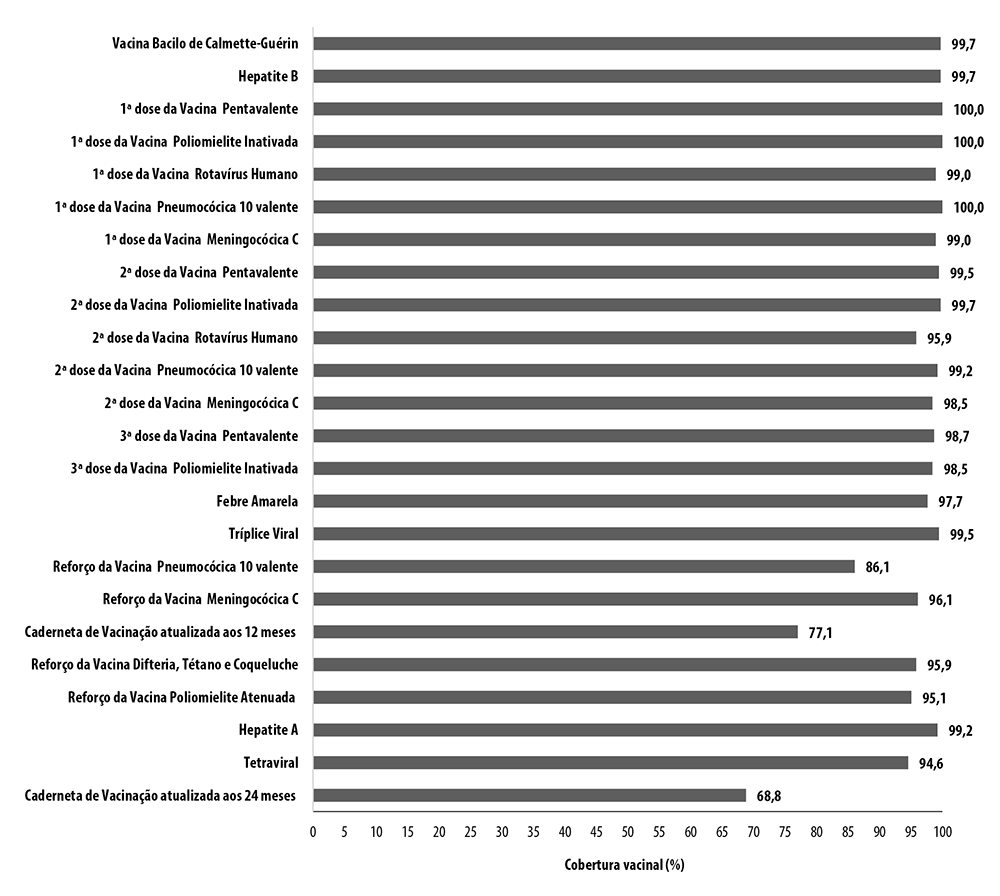
Figura 3 Coberturas vacinais atualizadas por dose de vacinas e esquema completo aos 12 e aos 24 meses de idade (n=429), Araraquara, São Paulo, 2018
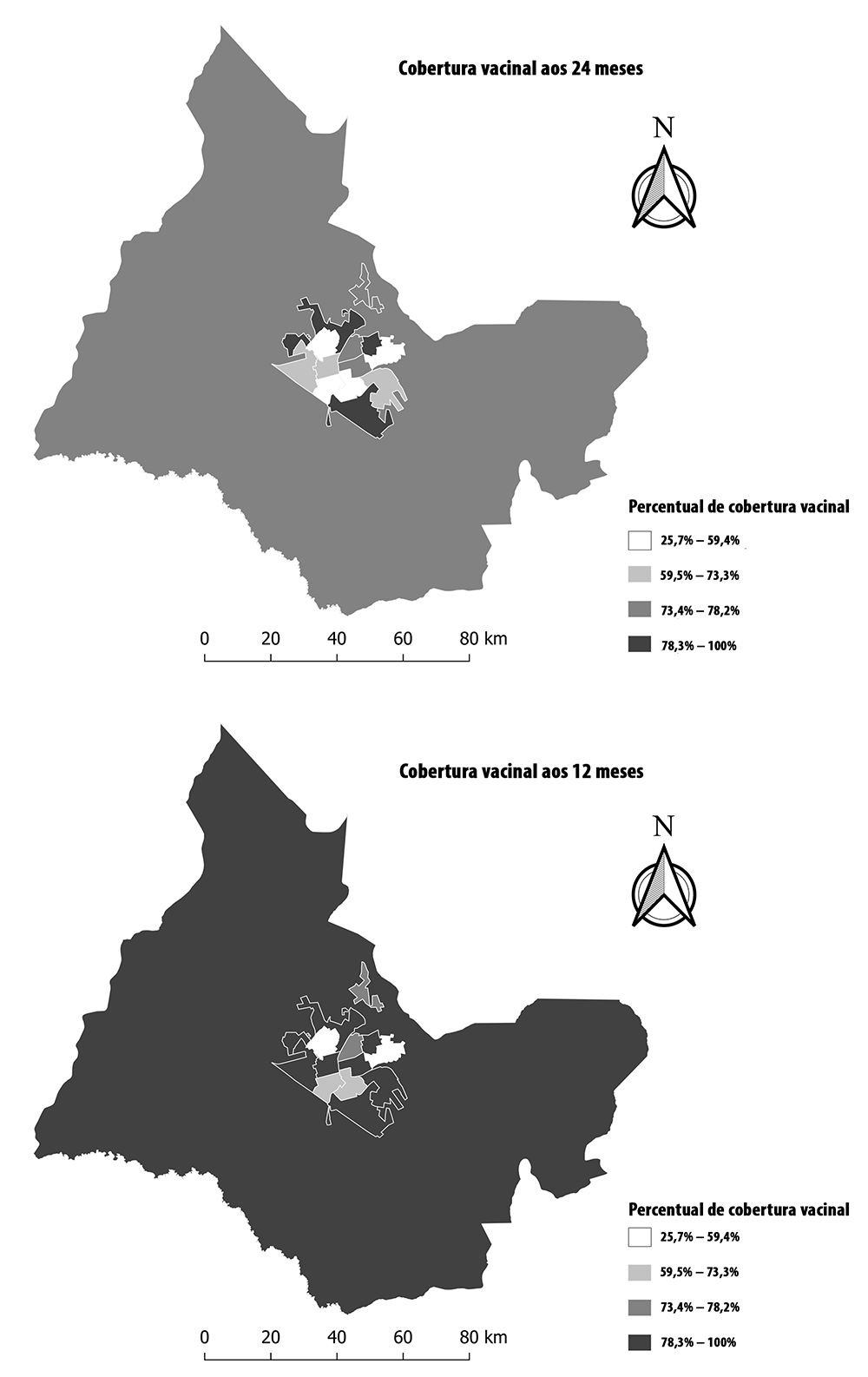
As distribuições espaciais das coberturas vacinais não exibiram um padrão definido, com uma cobertura vacinal heterogênea: variação de 25,7 a 100%. Além disso, a maioria das áreas de ponderação apresentou uma cobertura vacinal acima de 78% aos 12 meses; o que não se repetiu para o esquema aos 24 meses, quando essa cobertura se restringiu a apenas quatro áreas (Figura 4).
Discussão
Houve concordância entre o Sistema Juarez e os registros das cadernetas de vacinação; e altas coberturas vacinais, principalmente das vacinas aplicadas até os 12 meses de idade. As distribuições espaciais das coberturas vacinais não apresentaram um padrão definido; de fato, essa distribuição foi heterogênea, tanto para os esquemas de 12 meses quanto para os de 24 meses.
O uso de dados secundários pode ser considerado uma limitação do estudo, dada a possibilidade de apresentar incompletude e/ou inconsistências nos registros. Entretanto, ao se utilizar esses dados juntamente com os dados primários do inquérito vacinal, foi possível analisar a qualidade do registro informatizado de imunizações, estruturado e consolidado. A perda amostral, que também poderia representar uma limitação para o estudo, não só foi pequena como se manteve dentro da margem aceitável, prevista no cálculo amostral, sem poder de interferência nos resultados obtidos.
A alta cobertura vacinal encontrada também foi descrita em outros estudos, sobre nascidos em Araraquara nos anos de 1998 e 2013.9,10 Tal cobertura pode estar relacionada à organização do programa municipal de imunizações e ao bom desempenho do Sistema Juarez, sob contínua melhoria ao longo do tempo; e ao uso de ferramentas eficientes no monitoramento das coberturas vacinais, caso do relatório de faltosos/atrasados (recall), que permite a busca ativa para atualização de esquemas vacinais, e do relatório de crianças com vacinas agendadas (remind), para aumento da adesão e aproveitamento da oportunidade da vacinação.9
Assim como os resultados do presente estudo, o inquérito vacinal brasileiro de 2007, conduzido nas 26 capitais de estados e no Distrito Federal, mostrou que 82,6% das crianças receberam todas as vacinas até os 18 meses de idade.19 Outras pesquisas, como a realizada em São Luís, capital do estado do Maranhão, em 2006, por meio de um inquérito domiciliar, encontrou uma cobertura vacinal aos 12 meses de idade de 71,9%;20 em Pelotas, RS, dados da coorte de nascidos vivos de 2015 evidenciaram cobertura de 77,0%.21 Esses estudos reforçam a presença de boas coberturas vacinais.
A distribuição espacial permite visualizar a heterogeneidade das coberturas vacinais entre as áreas de ponderação e, por conseguinte, o monitoramento das coberturas vacinais das microáreas, um aspecto fundamental para o sucesso do PNI. Esse método tem sido cada vez mais utilizado na área da Saúde, tendo contribuído não só para a melhoria das atividades de vigilância mas, também para a identificação de áreas de risco, merecedoras de intensificação ou priorização de medidas de cobertura vacinal.22,23
Ainda sobre a cobertura vacinal, a heterogeneidade observada também foi relatada em pesquisa realizada no estado do Ceará, onde, apesar das altas coberturas vacinais contra o sarampo, quatro das 21 coordenadorias regionais de saúde não alcançaram a meta de 95%.24 Uma pesquisa dedicada à análise de uma série histórica (2013 a 2017) de coberturas vacinais em estado fronteiriço da Amazônia brasileira, sobre dados disponibilizados no Sistema de Informação do PNI, evidenciou a dificuldade em manter coberturas vacinais homogêneas em escala nacional, dadas as baixas coberturas vacinais de algumas regiões do país.25 Tais resultados podem se explicar pelas características do território brasileiro, sua grande diversidade social e cultural, e a influência de fatores sociodemográficos, como emprego/ocupação - especialmente entre as mães -, renda familiar, escolaridade pública das crianças, baixa escolaridade de seus responsáveis, número elevado de filhos por mãe e ordem de nascimento dessas crianças, compreensão das razões e da importância da vacinação, confiança no sistema público de saúde, e outros igualmente determinantes, como a distância física e o acesso a cuidados de saúde, ademais de questões programáticas, como o fornecimento de insumos e vacinas pela rede de frios.26,27
A ótima concordância observada entre o Sistema Juarez e a caderneta de vacinação da criança demonstra que em Araraquara, o registro informatizado dos dados de imunização apresenta uma cobertura vacinal de elevada acurácia. O achado corrobora o entendimento de que a experiência pioneira do SESA no desenvolvimento e uso do Sistema Juarez, ao longo de mais de três décadas, foi tanto exitosa quanto contribuiu para a qualidade do PNI e sua boa cobertura vacinal no município paulista. A eficiência no uso dos registros informatizados de imunização, ademais de favorecer o aumento das coberturas vacinais, conforme já foi relatado,28 reafirma a importância da precisão e da representatividade dos registros dos dados da população, possíveis de serem utilizados no planejamento das ações.29
Os resultados do presente estudo avalizam-no a orientar políticas públicas para o resto do país e servir de subsídio ao Sistema de Informação do Programa Nacional de Imunizações (SI-PNI). Eles evidenciam o potencial dos registros informatizados na ampliação da cobertura e qualificação dos programas de imunizações em curso, enquanto uma ferramenta eficiente de monitoramento e avaliação das coberturas vacinais, proporcionando a identificação de microáreas de baixa cobertura vacinal e bolsões de suscetíveis a doenças imunopreveníveis.
Conclui-se que o Sistema Juarez é um registro informatizado de imunização bastante confiável, nos dados que apresenta, útil ao monitoramento e vigilância das coberturas vacinais. Araraquara, outrossim, conta com uma boa cobertura vacinal, embora sua distribuição espacial tenha-se revelado heterogênea.










 texto en
texto en 
 Curriculum ScienTI
Curriculum ScienTI