Apresentação
O artigo aborda as infecções que causam corrimento uretral, tema que compõe o Protocolo Clínico e Diretrizes Terapêuticas (PCDT) para Atenção Integral às Pessoas com Infecções Sexualmente Transmissíveis (IST), publicado pela Secretaria de Vigilância em Saúde, do Ministério da Saúde do Brasil. Para a elaboração do PCDT, foram realizadas a seleção e a análise das evidências disponíveis na literatura e discussão em um painel de especialistas. O referido PCDT foi aprovado pela Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec)1 e atualizado pelo grupo de especialistas em IST em 2020.
Aspectos epidemiológicos
A uretrite é definida como uma inflamação da uretra, podendo ser infecciosa ou não. Vários agentes podem causar uretrite infecciosa, no contexto de práticas sexuais sem preservativos. As uretrites são classificadas, de acordo com o agente etiológico, em gonocócicas, causadas por Neisseria gonorrhoeae, e em não gonocócicas, causadas majoritariamente por Chlamydia trachomatis e Mycoplasma genitalium. Outros agentes, como Trichomonas vaginalis, enterobactérias (nas relações anais insertivas), o vírus do herpes simples (herpes simplex virus, HSV), o adenovírus e Candida sp. são menos frequentes. 2 3
São fatores associados à uretrite: idade jovem, baixo nível socioeconômico, múltiplas parcerias ou nova parceria sexual, histórico de IST e uso irregular de preservativos, bem como falta de acesso a diagnóstico e tratamento adequados.2 3
A Organização Mundial da Saúde (OMS), por meio de estudo de revisão sistemática, estimou, para o ano de 2016, a ocorrência de 370,4 milhões de novas infecções urogenitais curáveis por clamídia, gonorreia, e tricomoníase em mulheres e homens de 15 a 49 anos.4 A taxa de incidência global de clamídia em 2016 foi de 34 casos por 1.000 mulheres e 33 casos por 1.000 homens; de gonorreia, 20 casos por 1.000 mulheres e 26 casos por 1.000 homens; e, de tricomoníase, 40 casos por 1.000 mulheres e 42 casos por 1.000 homens.4 Estudo de revisão sistemática e metanálise sobre a prevalência de M. genitalium, que contemplou três estudos com um total de 3.809 pessoas, estimou uma prevalência de 1,3% desse agente em países desenvolvidos e 3,9% em países em desenvolvimento. A prevalência foi similar em homens e mulheres.5 Análises do sistema europeu de vigilância de doenças transmissíveis verificaram que, em 2018, dos 17 países que coletaram dados sobre o modo de transmissão de gonorreia, 48% de todos os casos confirmados e notificados ocorreram em homens que fazem sexo com homens.6
No Brasil, o cenário epidemiológico das infecções que causam corrimento uretral acompanha os altos índices mundiais. Estima-se que a prevalência de gonorreia na população de 15 a 49 anos seja de aproximadamente 1,4% e que a incidência na população geral esteja em torno de 500.000 novos casos por ano.7
Quanto ao risco de transmissão dos agentes infecciosos, verifica-se que a N. gonorrhoeae é transmitida do homem infectado para a mulher, com probabilidade que pode variar de 50% a 73%, independentemente do número de exposições. Já a probabilidade de o homem se infectar com mulher infectada varia de 20% a 35% em uma exposição.8 O sexo oral desprotegido resulta em infecção em cerca de 25% das vezes, pois a faringe é um dos maiores reservatórios assintomáticos do patógeno.9
No caso da C. trachomatis, a probabilidade de um homem contrair a infecção a partir de uma mulher é de 32%, e de a mulher contrair a infecção do homem, de 40%; essa proporção de transmissão se refere a contato com parceiro infectado por ato sexual desprotegido.10 Embora esteja bem estabelecido que o M. genitalium é sexualmente transmitido, não se sabe quantas vezes isso ocorre por episódio de relação sexual desprotegida.11 Estudos sugerem que a transmissão de M. genitalium é provavelmente menor do que a de C. trachomatis, o que seria consistente com a carga infecciosa desses agentes. É provável que homens com uretrite não gonocócica sintomática e, presumivelmente, cargas mais altas de M. genitalium sejam mais infecciosos do que homens com infecção assintomática.12 13
O risco de os homens se infectarem com parceiras infectadas por T. Vaginalis varia de 22% a 72%. Tendo em vista que há contaminação em até 5% das pessoas que relatam sexo anal receptivo recente, é necessário esclarecer se o reto pode ser um reservatório para infecção por T. Vaginalis.14 De acordo com o Centro de Prevenção e Controle de Doenças dos Estados Unidos (Centers for Disease Control and Prevention, CDC) não são recomendados testes retais e orais para T. Vaginalis devido à falta de evidências dessas infecções nesses locais.
A Figura 1 apresenta síntese dos riscos oferecidos por cada agente infeccioso causador de corrimento uretral.
Figura 1 Risco de transmissão dos agentes infecciosos causadores de corrimento uretral em práticas sexuais desprotegidas
| Agente infeccioso | Prática sexual | Transmissão do homem para mulher | Transmissão da mulher para o homem | Referência |
|---|---|---|---|---|
| Neisseria gonorrhoeae | Relação sexual | 50% a 73% | 20% a 35% | [8] |
| Sexo oral | 25% | 25% | [9] | |
| Chlamydia trachomatis | Relação sexual | 40% | 32% | [10] |
| Trichomonas vaginalis | Relação sexual | Não há informação | 22% a 72% | [14] |
Aspectos clínicos
O corrimento uretral é uma síndrome clínica, com identificação de um grupo de sintomas e sinais comuns a determinadas infecções, caracterizada por corrimento de aspecto que varia de mucoide a purulento, com volume variável, podendo estar associado a dor uretral (independentemente da micção), disúria, estrangúria (micção lenta e dolorosa), prurido uretral e eritema do meato uretral. O aspecto do corrimento uretral purulento corresponde a 75% das uretrites causadas por N. gonorrhoeae e de 11% a 33% das uretrites não gonocócicas; por sua vez, o aspecto mucoide apresenta-se em cerca de 25% dos casos de uretrites gonocócicas e 50% dos casos de uretrites não gonocócicas.2
A uretrite gonocócica é um processo infeccioso e inflamatório da mucosa uretral. Após o período de incubação, que dura em média de dois a cinco dias, variando de um a 10 dias, a infecção evolui sintomaticamente. A disúria é compreendida como a sensação de formigamento e prurido intrauretral seguido de dor à micção. O corrimento, inicialmente mucoide, torna-se purulento em um a dois dias, com grande volume e acompanhado de edema do meato uretral. Alguns homens podem apresentar febre, assim como manifestações de uma infecção aguda sistêmica. Cerca de 95% dos casos tornam-se assintomáticos em três meses, e uma proporção de casos não tratados pode evoluir para cura espontânea em algumas semanas.15
As complicações clínicas pelo não tratamento imediato ocorrem em até 50% dos casos, pela progressão da infecção para a uretra posterior. A epididimite aguda compreende a complicação mais frequente, podendo evoluir com obstrução do ducto epididimário, determinando oligospermia, azoospermia e esterilidade. Outras consequências da uretrite gonocócica são: prostatite, orquite, edema peniano (em particular do prepúcio), balanopostite, e, ainda, lesões das glândulas sebáceas e acinosas da região genital, tisonites (glândulas de Tyson), cowperites (glândulas de Cowper) e litrites (glândulas de Littré).15
A uretrite não gonocócica é a uretrite sintomática cuja bacterioscopia pela coloração de Gram, cultura e detecção de material genético por biologia molecular são negativas para o gonococo. A infecção por clamídia no homem é responsável por aproximadamente 50% dos casos de uretrites não gonocócicas. O período de incubação no homem é de 14 a 21 dias. Estima-se que dois terços das parceiras estáveis de homens com uretrite não gonocócica hospedem a C. trachomatis na endocérvice, podendo, assim, reinfectar seus parceiros sexuais e desenvolver quadro de doença inflamatória pélvica se não for realizado tratamento.16-18
No homem, a uretrite não gonocócica caracteriza-se, habitualmente, pela presença de corrimentos mucoides, discretos, com disúria leve e intermitente. A uretrite subaguda é a forma de apresentação em aproximadamente 50% dos homens com uretrite causada por C. trachomatis.19 Entretanto, em alguns casos, os corrimentos das uretrites não gonocócicas podem simular, clinicamente, os da gonorreia. As uretrites causadas por C. trachomatis podem evoluir para prostatite, epididimite, balanite, conjuntivite (por autoinoculação) e síndrome uretro-conjuntivo-sinovial ou síndrome de Reiter.
As mulheres com uretrite apresentam disúria leve, que pode estar associada a corrimento vaginal ou sangramento. O exame físico pode revelar a presença de cervicite mucopurulenta ou até mesmo lesões herpéticas símiles vulvovaginais.20
Nos casos de uretrites persistentes, deve-se realizar a avaliação principalmente por meio da história clínica, considerando a possibilidade de reinfecção ou tratamento inadequado para clamídia e gonorreia. Descartadas tais situações, devem-se pesquisar agentes não suscetíveis ao tratamento anterior (por exemplo, M. genitalium e T. Vaginalis), bem como a ocorrência de resistência aos antimicrobianos.2
Outras causas não infecciosas de uretrites, como trauma (ordenha continuada), instrumentalização, inserção de corpos estranhos intrauretrais ou parauretrais (piercings) e irritação química (uso de produtos lubrificantes e espermicidas) devem ser consideradas no diagnóstico diferencial de uretrites persistentes.2
Diagnóstico
O manejo do corrimento uretral pode ser realizado por meio da abordagem sindrômica para situações em que não há suporte laboratorial2 21 22 (Figura 2). Para os casos de corrimento uretral masculino, estima-se que a abordagem sindrômica tenha uma sensibilidade que varia de 84% a 95%.23
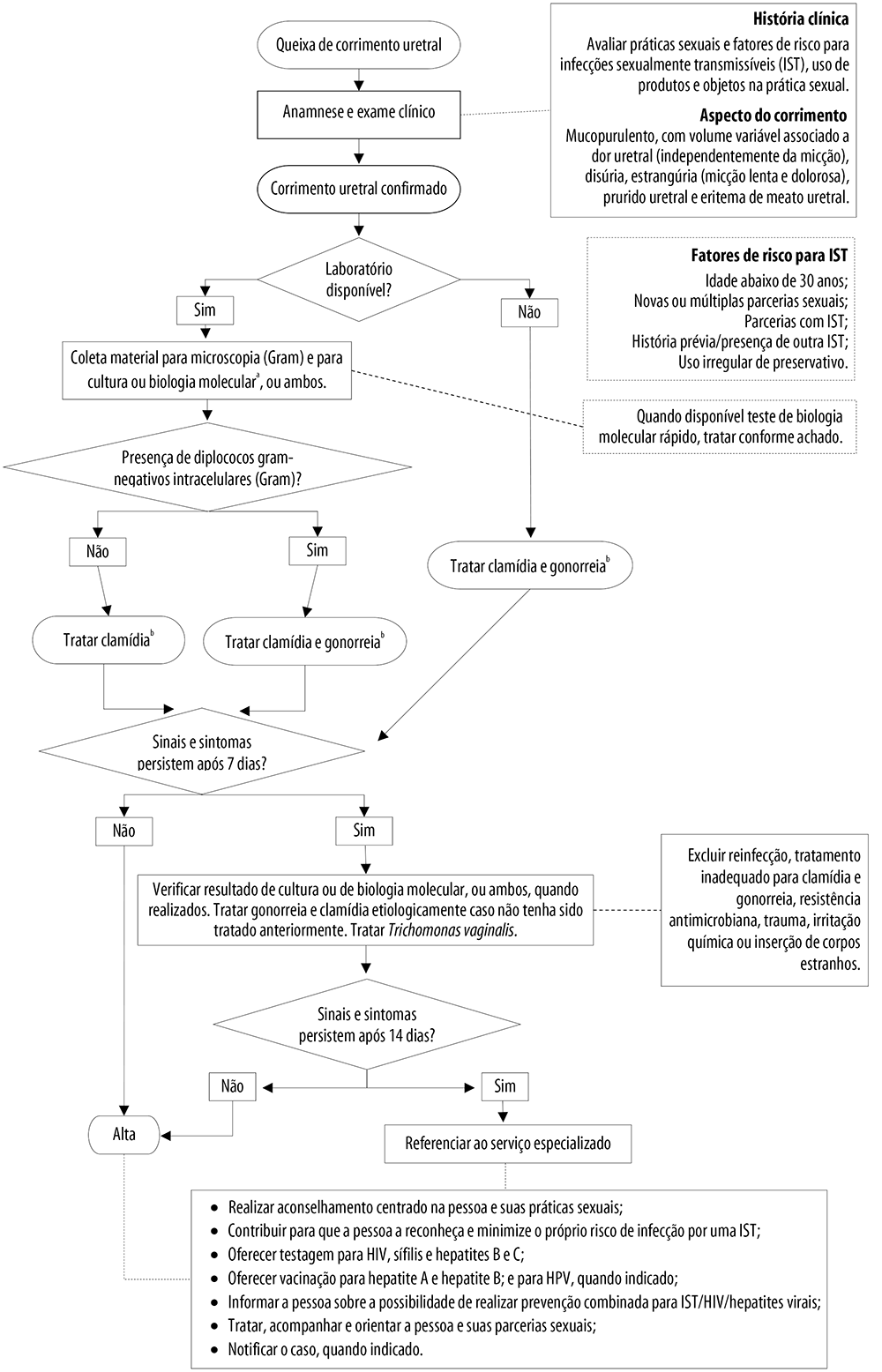
Fonte: adaptado do Protocolo Clínico e Diretrizes Terapêuticas para Atenção Integral às Pessoas com Infecções Sexualmente Transmissíveis, 2020.2
Notas: a) Existem kits de biologia molecular que detectam mais patógenos simultaneamente, além de clamídia e gonococo, e que também são úteis para o diagnóstico etiológico de uretrites, como M. genitalium; b) Esquema terapêutico também contempla tratamento para M. genitalium.
Figura 2 Recomendações para atendimento às pessoas com queixa de corrimento uretral
A utilização de testes diagnósticos é indicada para o rastreamento dos casos assintomáticos de uretrite e para investigação dos casos sintomáticos.2 O bom desempenho dos testes depende do rigoroso cumprimento de todas as etapas preconizadas pelos fabricantes, incluindo coleta, transporte e armazenamento das amostras.24
O rastreamento dos casos assintomáticos de uretrite deve ser realizado utilizando-se técnicas de biologia molecular, que incluem métodos com elevada sensibilidade e especificidade, como a reação em cadeia da polimerase e a amplificação mediada por transcrição. Esses testes, que se baseiam em amplificação de ácidos nucleicos (nucleic acid amplification test, NAAT), permitem a utilização de amostras de corrimento uretral masculino ou urina, ou ambos os tipos de amostra, e a identificação de um ou mais patógenos simultaneamente em uma única amostra, a depender do fabricante. Os resultados são emitidos discriminando-se os patógenos detectados.24-27
Para o diagnóstico de uretrites sintomáticas, podem ser realizados diversos testes para auxiliar na identificação do agente causador.2 Estão incorporados ao Sistema Único de Saúde (SUS) brasileiro a bacterioscopia, a cultura e os métodos de biologia molecular, disponíveis de forma heterogênea nos diferentes níveis de atenção dos serviços de saúde.
Na uretrite gonocócica, é possível visualizar, por meio da bacterioscopia, diplococos Gram-negativos intracelulares em leucócitos polimorfonucleares. O método possui alta sensibilidade e especificidade em amostras de corrimento uretral masculino.2 24 27 A cultura de amostras em meio seletivo (por exemplo, Thayer-Martin ou similar) é uma técnica com boa sensibilidade e alta especificidade para diagnóstico de N. gonorrhoeae, desde que empregada com rigor metodológico.27 Em suma, realiza-se o cultivo de amostras biológicas em meios de cultura que favoreçam o crescimento de Neisseria sp. Como o meio de cultura também permite o crescimento de outras espécies do gênero Neisseria, é importante que se faça o Gram das colônias típicas (visualização de diplococos Gram-negativos) e testes de oxidase e catalase, que deverão apresentar resultados positivos quando se tratar de N. gonorrhoeae. Para diagnóstico definitivo, podem-se submeter as colônias a provas bioquímicas (manuais ou automatizadas), pois o comportamento particular das bactérias na presença de diversos substratos possibilita a identificação das espécies de Neisseria.2 28 29 A cultura também permite a investigação do perfil de susceptibilidade do gonococo aos antimicrobianos por meio de técnicas para determinação da concentração inibitória mínima, e possui grande utilidade para fins de vigilância e estabelecimento de diretrizes de tratamento.24 29 Além da bacterioscopia e da cultura, estão disponíveis no SUS as técnicas de biologia molecular, como os NAAT, que apresentam ótimo desempenho para diagnóstico etiológico das uretrites sintomáticas e são fortemente recomendados no tratamento etiológico do corrimento uretral.
Na ausência dos métodos citados, é possível a utilização de testes que sugerem presença de infecção, porém não definem o agente infeccioso, como o teste positivo de esterase leucocitária na urina de primeiro jato ou o exame microscópico de sedimento urinário de primeiro jato apresentando mais de dez leucócitos polimorfonucleares por campo (aumento de 1.000 vezes).2
Tratamento
O tratamento recomendado das uretrites pode depender ou não de suporte laboratorial.2 Na presença de queixa de corrimento uretral, após anamnese e exame físico, com corrimento uretral confirmado, caso não haja suporte de laboratório (uretrite sem identificação do agente etiológico), é indicado o tratamento de clamídia e gonorreia com azitromicina 1g, via oral (VO), dose única, e ceftriaxona 500mg, intramuscular (IM), dose única. Na possibilidade de realização de bacterioscopia (Gram), com visualização de diplococos intracelulares Gram-negativos, deve-se tratar gonorreia e clamídia conforme descrito acima (ceftriaxona 500mg, IM, dose única, e azitromicina 1g, VO, dose única); a presença de diplococos intracelulares Gram-negativos indica infecção por gonococo, mas não exclui a possibilidade de infecção por clamídia. Na ausência desses achados, deve-se tratar apenas clamídia com azitromicina 1g, VO, dose única. Quando possível a realização de coleta de material biológico para cultura ou biologia molecular no laboratório, esta deverá ocorrer na primeira consulta. O tratamento deverá ser instituído de imediato e os resultados dos testes poderão ser analisados na consulta de retorno.2
Destaca-se que, a partir de resultados do Projeto SenGono 2015-2017 (descrito no subtópico Resistência aos antimicrobianos), a diretriz brasileira de tratamento recomenda nacionalmente a terapia dupla de ceftriaxona 500mg, IM, dose única, associada à azitromicina 1g, VO, dose única, para a infecção gonocócica anogenital não complicada (uretra, colo do útero e reto).2
Após sete dias do tratamento, deve-se garantir uma consulta para reavaliação de sinais e sintomas e entrega de resultados de exames de cultura ou de biologia molecular, ou ambos, quando realizados. A remissão da sintomatologia caracteriza cura. Na persistência de sintomas, é importante excluir reinfecção, realização de tratamento inadequado para clamídia e gonorreia, resistência antimicrobiana (principalmente relacionada ao gonococo e M. genitalium), trauma, irritação química ou inserção de corpos estranhos. Em complemento, deve-se tratar T. Vaginalis com metronidazol 250mg, dois comprimidos, VO, duas vezes ao dia, por sete dias, e analisar os resultados dos exames para avaliar a necessidade de instituir novo tratamento conforme achado. Uma consulta para reavaliação deverá ser agendada para após sete dias, com instituição de alta na ausência de sinais e sintomas, e referenciamento para serviços especializados, na persistência desses. As opções de tratamento para uretrites estão apresentadas na Figura 3.2
Figura 3 Tratamento de uretrites
| Condição clínica | Primeira opção | Segunda opção | Observações |
|---|---|---|---|
| Uretrite sem identificação do agente etiológicoa,b | Ceftriaxona 500mg, intramuscular (IM), dose única mais azitromicina 500mg, 2 comprimidos, via oral (VO), dose única | Ceftriaxona 500mg, IM, dose única mais doxiciclina 100mg, 1 comprimido, VO, 2x/dia, por 7 dias | |
| Uretrite gonocócica e demais infecções gonocócicas NÃO complicadas (uretra, colo do útero, reto e faringe)a,b | Ceftriaxona 500mg, IM, dose única mais azitromicina 500mg, 2 comprimidos, VO, dose única | ||
| Uretrite não gonocócicab | Azitromicina 500mg, 2 comprimidos, VO, dose única | Doxiciclina 100mg, 1 comprimido, VO, 2x/dia, por 7 dias | A resolução dos sintomas pode levar até 7 dias após a conclusão da terapia. |
| Uretrite por clamídiab | Azitromicina 500mg, 2 comprimidos, VO, dose única | Doxiciclina 100mg, 1 comprimido, VO, 2x/dia, por 7 dias | A resolução dos sintomas pode levar até 7 dias após a conclusão da terapia. |
| Retratamento de infecções gonocócicasb | Ceftriaxona 500mg, IM, dose única mais azitromicina 500mg, 4 comprimidos, VO, dose única | Gentamicina 240mg, IM mais azitromicina 500mg, 4 comprimidos, VO, dose única | Para casos de falha de tratamento. Possíveis reinfecções devem ser tratadas com as doses habituais. |
| Uretrite por Mycoplasma genitaliumb | Azitromicina 500mg, 2 comprimidos, VO, dose única | ||
| Uretrite por Trichomonas vaginalisb | Metronidazol 250mg, 2 comprimidos VO, 2x/dia, por 7 dias | Clindamicina 300mg, VO, 2x/dia, por 7 dias | |
| Infecção gonocócica disseminada (exceto meningite e endocardite) | Ceftriaxona 1g IM ou IV ao dia, completando ao menos 7 dias de tratamento mais azitromicina 500mg, 2 comprimidos, VO, dose única | ||
| Conjuntivite gonocócica no adulto | Ceftriaxona 1g, IM, dose única |
Fonte: adaptado do Protocolo Clínico e Diretrizes Terapêuticas para Atenção Integral às Pessoas com Infecções Sexualmente Transmissíveis, 2020.13
Notas: a) Se houver alergia grave às cefalosporinas, indicar azitromicina 500mg, quatro comprimidos, via oral, dose única (dose total: 2g); b) Os casos e as parcerias devem se abster de relações sexuais desprotegidas até que o tratamento de ambos esteja completo (ou seja, após o término do tratamento com múltiplas doses ou por sete dias após a terapia com dose única).
Vigilância, prevenção e controle
As IST estão entre os problemas de saúde pública mais comuns no Brasil e no mundo. A atenção primária à saúde constitui o ponto de partida para atendimento às IST, com realização de ações de prevenção, diagnóstico, tratamento oportuno e adequado e encaminhamento dos casos que não competem a esse nível de atenção. Para possibilitar a integralidade do cuidado, é fundamental que os serviços se organizem para promover o acesso a outros níveis de atenção, quando necessário.30
A anamnese, a identificação das diferentes vulnerabilidades e o exame físico são importantes elementos na abordagem das pessoas com IST. Para garantir a qualidade do atendimento, a adesão ao tratamento e a retenção no serviço de saúde, o profissional de saúde necessita estabelecer uma relação de confiança com a pessoa com IST, assegurando a privacidade e confidencialidade das informações.
É importante que o profissional esteja disponível para diálogo e forneça informações sobre educação em saúde, abordando temas como agentes causais das IST, possíveis formas de transmissão, prevenção, diagnóstico e importância da adesão ao tratamento, além da definição de estratégia para seguimento, atenção às parcerias sexuais e acesso aos insumos de prevenção.31
A prevenção e controle das IST que causam uretrites compreendem o uso correto de preservativos durante as relações sexuais; rastreamento e testagem regular de pessoas assintomáticas, realizada nas populações específicas; investigação e manejo dos casos sintomáticos; instituição de tratamento imediato, quando indicado; e tratamento de parcerias sexuais. O tratamento, além de ter função curativa, também visa à interrupção da cadeia de transmissão e à prevenção de complicações decorrentes das uretrites.2 31
O rastreamento de gonococo e clamídia, em pessoas assintomáticas, está indicado nas seguintes situações: gestantes menores de 30 anos, na primeira consulta do pré-natal; pessoas vivendo com HIV, no momento do diagnóstico da infecção pelo HIV; pessoas com indicação de profilaxia pós-exposição ao HIV; pessoas com IST no momento do diagnóstico; pessoas que sofreram violência sexual, no primeiro atendimento e no atendimento quatro a seis semanas após; pessoas com prática sexual anal receptiva (passiva) sem uso de preservativo; e pessoas em uso de profilaxia pré-exposição ao HIV, semestralmente.2
Para que se interrompa a cadeia de transmissão das IST, é fundamental que os contatos sexuais das pessoas infectadas sejam tratados, mesmo quando assintomáticos.3 Portanto, essa informação deve ser repassada à pessoa com IST, ao tempo em que se fornecem instrumentos para comunicação e apoio até o final do atendimento. Deverá ser garantida a confidencialidade, ausência de coerção e proteção contra a discriminação.2
Em homens com sintomas de infecção por gonococo, C. trachomatis ou M. genitalium, todas as parcerias sexuais durante as oito semanas anteriores precisam ser examinadas e tratadas. Em casos assintomáticos, isso se aplica a todas as parcerias sexuais dos últimos seis meses.3
As uretrites não são agravos de notificação compulsória nacional; entretanto, a síndrome do corrimento uretral é de notificação compulsória em alguns estados brasileiros. Ademais, o Ministério da Saúde do Brasil publicou uma portaria32 que instituiu sítios para vigilância sentinela da síndrome do corrimento uretral masculino, os quais devem fornecer informações para a construção de dados epidemiológicos oficiais. Além disso, visa-se fortalecer ações de prevenção de IST que causam corrimento uretral, subsidiar recomendações nacionais para o tratamento da síndrome, monitorar a susceptibilidade de gonococos aos antimicrobianos junto ao Projeto SenGono e pesquisar os agentes causais de úlceras genitais e a resistência de M. genitalium aos antimicrobianos.33
Resistência aos antimicrobianos
Ao longo da história da antibioticoterapia, a N. gonorrhoeae desenvolveu progressiva resistência aos antibióticos, desde as sulfonamidas até as fluorquinolonas. Após a disseminação da resistência ao ciprofloxacino, as cefalosporinas de terceira geração têm sido a base do tratamento, em associação à azitromicina. O surgimento de gonorreia resistente à cefalosporina impactará negativamente na capacidade dos profissionais para tratar a gonorreia de maneira eficaz. Cepas de gonococo consideradas multidroga-resistentes e extensivamente resistentes a medicamentos já são encontradas no continente americano, asiático, em vários países europeus e na Oceania.34-37 É, portanto, fundamental monitorar continuamente a resistência aos antibióticos e incentivar a pesquisa e o desenvolvimento de novos esquemas de tratamento.38 39
A OMS, no “Relatório Global de Vigilância às Infecções Sexualmente Transmitidas de 2018”, prioriza o controle das infecções gonocócicas pela possibilidade iminente de tornarem-se infecções não tratáveis.40 41 O Brasil é um dos países membros do programa para vigilância mundial da susceptibilidade do gonococo aos antimicrobianos (Gonococcal Antimicrobial Surveillance Programme, GASP).42 As atividades do GASP no Brasil acontecem no âmbito do Projeto SenGono, fruto de uma cooperação entre o Ministério da Saúde, o Laboratório de Referência Nacional (Laboratório de Biologia Molecular, Microbiologia e Sorologia da Universidade Federal de Santa Catarina) e os sítios sentinelas distribuídos por todas as regiões do país (Figura 4).33
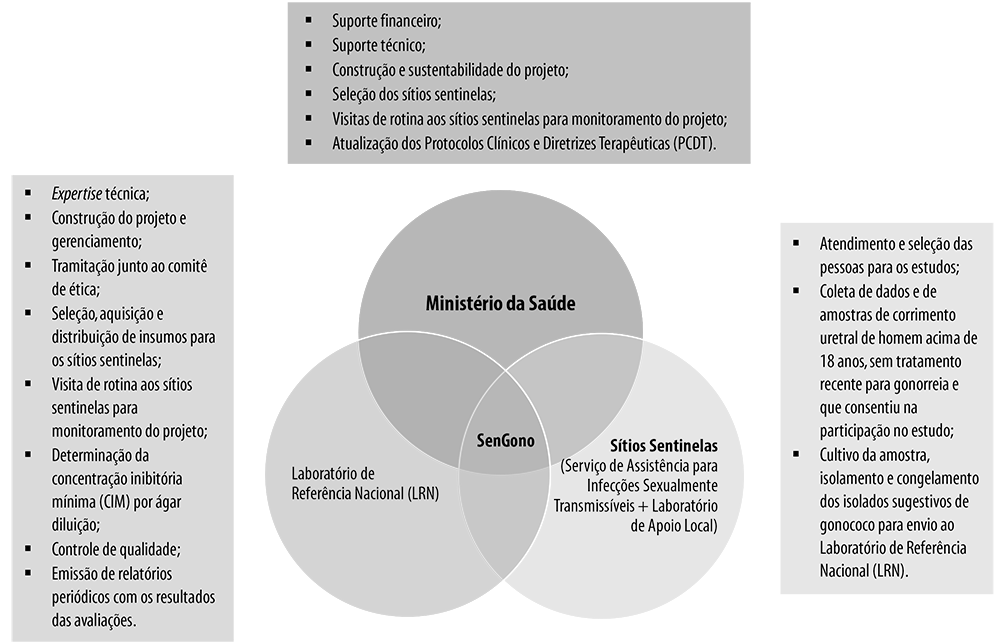
Fonte: adaptado do Boletim Epidemiológico nº 27/2020, do Ministério da Saúde.32
Figura 4 Funções do Ministério da Saúde, do Laboratório de Referência Nacional e dos Sítios Sentinelas no âmbito do Projeto SenGono
Na primeira edição, ocorrida entre 2015 e 2017, constatou-se uma resistência elevada ao ciprofloxacino, com proporções próximas e até superiores a 50% em todas as regiões do país, e altas proporções de susceptibilidade às cefalosporinas de terceira geração (cefixima e ceftriaxona).26
A vigilância realizada no Projeto SenGono integrou o “Plano Nacional de Combate à Resistência aos Antimicrobianos 2019-2023”, e está na sua segunda edição (2018-2020), com a expansão para novos sítios sentinelas e avaliação da suscetibilidade do gonococo a dois novos antimicrobianos (espectinomicina e gentamicina). Além disso, incorporou-se a essa edição a determinação da etiologia do corrimento uretral masculino e a investigação da resistência de M. genitalium aos antimicrobianos.33
O M. genitalium foi identificado pela primeira vez em 1980 e reconhecido como importante causa de uretrites não gonocócicas.25 43-45 Por não apresentar parede celular, antibióticos como os beta-lactâmicos (incluindo penicilinas e cefalosporinas) não são eficazes.29 A introdução da azitromicina, utilizada como terapia de dose única para infecções por clamídia, resultou na depuração do M. genitalium do trato urogenital, ocorrendo eliminação do patógeno sem o desenvolvimento de doença.25 43 46-50 Porém, estudos recentes indicam uma tendência ascendente na prevalência de infecções por M. genitalium resistentes aos macrolídeos (resistência transmitida) e casos de resistência induzida após terapia com azitromicina.3 43 50 Não há evidências de que um regime estendido com azitromicina (1,5g) seja superior ao regime de 1g em dose única.51 O moxifloxacino permanece altamente ativo contra a maioria dos M. genitalium resistentes a macrolídeos. No entanto, foram publicados os primeiros casos clínicos de falha do tratamento com moxifloxacino.3 28 43 44 50-53 Portanto, o M. genitalium é um problema emergente, necessitando de uma vigilância frequente e de estudos com novas opções de diagnóstico e tratamento.27
O aumento da resistência, nas últimas décadas, reforça a importância do diagnóstico etiológico e a escolha de tratamentos adequados. Em 2016, a Assembleia Mundial da Saúde adotou a “Estratégia do setor de saúde global sobre infecções sexualmente transmissíveis, 2016-2021”.38 Essa estratégia inclui a rápida expansão de intervenções e serviços baseados em evidências para eliminar as IST como preocupação de saúde pública até 2030.











 texto em
texto em 


