Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Boletim do Museu Paraense Emílio Goeldi Ciências Naturais
versão impressa ISSN 1981-8114
Bol. Mus. Para. Emilio Goeldi Cienc. Nat. v.1 n.3 Belém dez. 2006
Macrofauna bentônica de zonas entre-marés não vegetadas do estuário do rio Caeté, Bragança, Pará
Macrobenthos from unvegetated intertidal areas in the Caeté river estuary in Bragança, Pará
José Souto Rosa Filho; Debora Vieira Busman; Andréa Pontes Viana; Aderson Manoel Gregório; Diogo Marques Oliveira
Universidade Federal do Pará. Instituto de Geociências. Campus de Belém. Laboratório de Oceanografia Biológica. Belém, Pará, Brasil (jsouto@ufpa.br) (busman_dv@yahoo.com) (vianaap@yahoo.com.br) (aderson.manoel@ufrgs.br) (oliveiradm_oceano@yahoo.com.br)
RESUMO
A estrutura das comunidades macrobentônicas de zonas entre-marés não vegetadas do estuário do rio Caeté, Pará, Brasil foi estudada no período menos chuvoso de 2003. Foram tomadas amostras (n=4) em quatro estações utilizando um corer (0,008 m2, 20 cm de altura). As amostras foram passadas em malha de 0,3 mm e os organismos fixados com formalina salina a 5%. Em cada estação foi coletada uma amostra de sedimento e determinadas a salinidade e temperatura da água. Foram registrados 844 espécimes pertencentes a 17 táxons dos filos Nemertinea, Arthropoda e Annelida. Polychaeta dominou as associações (11 táxons e 87,25% do total de indivíduos). Os táxons mais abundantes foram Mediomastus californienses, Nephtys fluviatilis e oligoquetas Tubificidae. Os valores de abundância e riqueza passaram de 2625 ind.m-2 em P1 para 96625 ind.m-2 em P4 e, respectivamente de 3 para 16 táxons. A análise de agrupamento revelou a formação de três grupos (50% de similaridade). O grupo 1, formado pelas estações P3 e P4, teve alta salinidade (22,6 a 26,5), substrato constituído por areia muito fina, foi o grupo mais rico (13 táxons), diverso (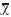 H´= 1,18) e abundante (
H´= 1,18) e abundante (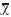 = 12220 ind.m-2), sendo dominado por Sigambra grubii. O grupo 2 reuniu as amostras da estação P1, com salinidade de 5,1, substrato silte-arenoso, e registros dos valores mais baixos de riqueza (3 táxons), diversidade (
= 12220 ind.m-2), sendo dominado por Sigambra grubii. O grupo 2 reuniu as amostras da estação P1, com salinidade de 5,1, substrato silte-arenoso, e registros dos valores mais baixos de riqueza (3 táxons), diversidade (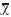 H´ = 0,67) e abundância (
H´ = 0,67) e abundância (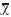 = 665 ind.m-2), cuja espécie mais abundante foi Namalicastys abiuma. O grupo 3, formado pelas amostras da estação P2, teve substrato silte-arenoso e salinidade 3,6. N. abiuma foi a espécie mais abundante nesse grupo, que teve valores intermediários de riqueza (5 táxons), abundância (
= 665 ind.m-2), cuja espécie mais abundante foi Namalicastys abiuma. O grupo 3, formado pelas amostras da estação P2, teve substrato silte-arenoso e salinidade 3,6. N. abiuma foi a espécie mais abundante nesse grupo, que teve valores intermediários de riqueza (5 táxons), abundância (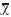 = 2010 ind.m-2) e diversidade (
= 2010 ind.m-2) e diversidade (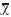 H´ = 0,71). É possível concluir que, no médio litoral não vegetado do rio Caeté, o número de espécies é baixo, Annelida é o grupo dominante, a composição específica reflete o gradiente de salinidade e a riqueza, diversidade e abundância aumentam na medida em que se passa do estuário superior para o inferior.
H´ = 0,71). É possível concluir que, no médio litoral não vegetado do rio Caeté, o número de espécies é baixo, Annelida é o grupo dominante, a composição específica reflete o gradiente de salinidade e a riqueza, diversidade e abundância aumentam na medida em que se passa do estuário superior para o inferior.
Palavras-chave: Amazônia. Zoobentos. Comunidade de fundos moles. Manguezal.
ABSTRACT
The macrobenthic community structure was studied in inter-tidal, non-vegetated areas of the Caeté river estuary, Pará, Brazil, during the dry season of 2003. Four samples were collected at four stations on the downstream direction (P1 to P4) using a corer (0.008 m2 and 20 cm long). Samples were sieved through a 0,3 mm mesh and the organisms preserved in a 5% formaline saline solution stained with Bengal rose. At each station, sediment samples were collected and salinity and water temperature recorded. A total of 105,500 individuals were collected, divided in 17 taxa comprising the fphyla: Nemertea, Arthropoda and Annelida. Polychaeta dominated the assemblages (11 taxa and 87.25% of the individuals). The most abundant taxa were Mediomastuscalifornienses, Nephtys Huviatilisand Oligochaeta (Tubificidae). Density and richness values varied from 2625 ind.m-2 and 3 taxa at station P1 to 96625 ind.m-2 among 16 taxa at station P4. Cluster analysis seperated three groups (50% similarity): Group 1, including samples from stations P3 and P4, was characterized by a relatively high salinity (22.6 to 26.5) and a fine sand substrate. This group, dominated by Sigambra grubii, was the richest (13 taxa), most diverse (χH´ = 1.18) and abundant (χ= 12220 ind.m-2); Group 2, including samples from station P1, was characterized by a salinity of 5,1 and a silt-sandy substrate. This group presented the lowest richness (3 taxa), diversity (χH´ = 0.67) and abundance (χ= 665 ind.m-2) values, and was dominated by the species Namalicastysabiuma; and Group 3, including samples from station P2, was characterized by a salinity of 3.6 and a silt-sandy substrate. N. abiuma was the most abundant species of this group that was characterized by intermediate richness (5 taxa), abundance (χ= 2010 ind.m-2) and diversity (χH´ = 0.71) values. Thus, it is concluded that in the inter-tidal area of the non-vegetated Caeté river the species number is low; Annelida is the most abundant group; the species composition reflects the estuary salinity gradient; and richness, diversity and abundance increase from the upper to the lower estuary.
Keywords: Amazon. Zoobenthos. Soft bottom community. Mangrove.
INTRODUÇÃO
Os manguezais, importantes sistemas costeiros tropicais, são áreas de preservação permanente em decorrência de sua alta produtividade primária, possuem funções de reserva ecológica (centro de multiplicação de numerosas espécies animais), berçário, meio nutritivo e, sobretudo, fonte importante de recursos para as comunidades tradicionais (MPEG, 1999).
Dentre os componentes biológicos dos ambientes de manguezal, a fauna bentônica, composta por protozoários e metazoários que vivem em íntima relação com o substrato (LALLI; PARSONS, 1997), apresenta a maior diversidade e importância numérica (LITTLE, 2000). A macrofauna bentônica, por sua vez, compreende os organismos que são retidos em malha de 0,5 mm de abertura, sendo representada em manguezais por quase todos os filos de invertebrados maiores (LEVINTON, 2001).
Em manguezais, os principais fatores determinantes da estrutura e dinâmica das associações de macroinvertebrados bentônicos são as características ambientais (salinidade, temperatura, hidrodinâmica, composição e textura dos sedimentos e disponibilidade de substrato), a dinâmica das populações (recrutamento, natalidade e mortalidade) e as interações biológicas (competição, predação, parasitismo) (KINNE, 1971; ROSEMBERG, 1995; WIJSMAN; HERMAN; GOMOIU, 1999; HOGARTH, 1999).
Manino e Montagna (1997) citam que, nesses ambientes, a distribuição da salinidade e dos diferentes tipos de sedimento são importantes devido ao seu efeito na ecologia das espécies. Estudos sobre a distribuição da fauna estuarina ao longo de gradientes salinos apotam que os diferentes valores de salinidade atuam como uma barreira fisiológica para espécies estenohalinas marinhas (que não penetram nas áreas com baixa salinidade) e de água doce (incapazes de colonizar zonas com água salobra ou marinha) (WOLFF, 1983; KENISH 1986). Barnes (1980, 1994) registrou que, em estuários, de uma forma geral, a diversidade tende a crescer quando se passa da água doce para a água salgada.
Diversos autores, estudando as relações organismos-sedimentos em ambientes marinhos e estuarinos (RHOADS, 1974; DAUER; EWIG; RODI JR., 1987; FORBES; LOPEZ, 1990; SNELGLOVE; BUTTMAN, 1994), concluem que os macroinvertebrados bentônicos estão estreitamente relacionados com os sedimentos que habitam, sendo um pré-requisito para o entendimento da estrutura e dinâmica das associações macrobentônicas, uma descrição das relações entre os organismos e os sedimentos.
No Brasil, os manguezais estendem-se desde o Oiapoque, Amapá, até Laguna, Santa Catarina, ocupando uma área de aproximadamente 13.000 km2, com cerca de 50% dessas áreas localizadas na costa da região norte, nos estados do Maranhão, Fará e Amapá (KJEFVE et al., 2003). Nessas áreas, apesar de sua importância ecológica e econômica, a estrutura e o funcionamento das comunidades bentônicas são praticamente desconhecidos (LANA et al., 1996; CAPOB1ANCO et al., 2001), revelando a premente necessidade de estudos que venham preencher essas lacunas.
O presente estudo objetiva caracterizar a estrutura das associações macrobentônicas de fundos moles não vegetados do médio-litoral no estuário do rio Caeté, Pará, utilizando como descritores: composição específica, abundância, diversidade e equitatividade e verificando suas variações ao longo do gradiente salino, bem como suas relações com as características do substrato.
MATERIAL E MÉTODO
Área de estudo
O estuário do rio Caeté está localizado na planície costeira Bragantina, entre as latitudes 9884436 e 9893688 S e longitudes 304856 e 314305 W, no município de Bragança, nordeste do Pará. O regime de marés na região é do tipo macromaré semi-diurna, com variações de 4 m e máximas de 6 m durante os solistícios e equinócios. No estuário do rio Caeté, a temperatura do ar varia entre 25o e 27oC e a umidade relativa entre 80% e 91% (MARTORANO et al., 1993).
No período mais chuvoso (entre dezembro e maio), a precipitação pluviométrica no nordeste do Pará pode alcançar 22 mm.dia-1 e, no período menos chuvoso (junho a novembro), as taxas de precipitação variam entre 0,5 a 2 mm.dia-1. Durante os meses de maior precipitação, o rio Caeté apresenta os níveis de cota mais elevados e os maiores valores de vazão (aproximadamente 1400 m3.s-1), sendo o inverso registrado no período mais seco (valores aproximados de 750 m3.s-1) (SILVA, 2001).
As margens do estuário são colonizadas por bosques de mangue compostos por Rhizophora mangle, Avicennia germinans e Laguncularia racemosa. Em geral, os bosques de R. mangle ocorrem associados a baixas salinidades, enquanto que para o desenvolvimento de bosques de A. germinans é necessária uma alta salinidade (MATNI; MENEZES; BATISTA, 2002).
Procedimentos de campo
As coletas foram realizadas no período menos chuvoso, nos dias 11 e 12 de novembro de 2003, sendo tomadas amostras em quatro estações (P1, P2, P3 e P4) ao longo de um gradiente crescente de salinidade, da cidade de Bragança até o estuário inferior (Figura 1).
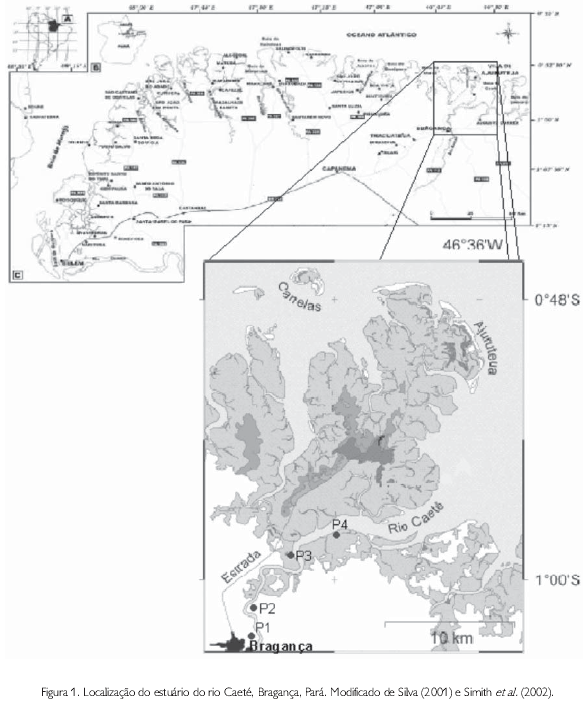
As estações de coleta localizam-se na região de médio-litoral não vegetado. Em cada estação foram tomadas quatro amostras utilizando um cilindro de PVC de 10 cm de diâmetro (0,008 m-2) enterrado 20 cm no substrato. Ainda em campo, as amostras foram passadas em malha de 0,3 mm de abertura, cujo material retido foi fixado com formalina salina a 5 % corada com Rosa de Bengala. Paralela à coleta de material biológico, foi determinada a salinidade da água com refratômetro manual (marca ATAGO) e coletadas amostras de sedimento para análise granulométrica (uma por estação).
Procedimentos de laboratório
Em laboratório, as amostras de material biológico foram triadas, os organismos identificados ao menor nível taxonômico possível e contados. Após esta etapa, o material foi conservado em álcool etílico a 70%. Calculou-se, então, para cada amostra, densidade (ind.m-2), riqueza (pela contagem do número de espécies), diversidade (índice H' de Shannon-Wiener), utilizando log e equitatividade (índice J de Pielou).
As amostras de sedimento foram inicialmente lavadas para a retirada do sal e, posteriormente, secas em estufa a 50oC. Para a determinação das frações granulométricas e separação dos finos (1000 rpm por um minuto para o silte e 1000 rpm por 10 min para a argila foi utilizado o método de centrifugação; enquanto para os grosseiros usou-se o peneiramento. Para a determinação dos parâmetros granulométricos de Folk e Ward (1957) foi utilizado o programa Sysgran® 2.4.
Aplicou-se análise de classificação para a identificação de padrões espaciais de distribuição da comunidade macrobentônica. Utilizou-se o método de amalgamação UPGMA, a partir de uma matriz de similaridade (similaridade de Bray Curtis) calculada com os valores de densidade por amostra, transformados por log (x+1). Para cada grupo identificado, foram calculados a densidade média e o número de espécies. Com o objetivo de determinar a contribuição de cada espécie para a formação dos grupos, o procedimento SIMPER (CLARKE; WARWICK, 1994) foi empregado com base na densidade por amostra, transformada por log (x + 1). Para a realização dessas análises foi utilizado o aplicativo PRIMER® 5.0.
RESULTADOS
A salinidade cresceu do estuário inferior (próximo à cidade de Bragança) para o superior (próximo ao mar), sendo mínima nas estações P1 e P2 e máxima em P4 e P5 (Tabela 1). As análises sedimentológicas mostraram que, no estuário do rio Caeté, a região entre-marés é silto-arenosa a areno-siltosa. A proporção de finos foi diminuindo em direção à foz, seguindo uma distribuição sedimentológica grano-cescente, característica de ambiente estuarinos. O grau de seleção dos sedimentos variou de pobre a moderadamente selecionado (Tabela 1).

Foram coletados e identificados 844 indivíduos distribuídos em 17 táxons pertencentes aos filos Nemertea, Arthropoda e Annelida (Tabela 2), com dominância deste último, representativo de 98,6% do total de indivíduos (Figura 2).
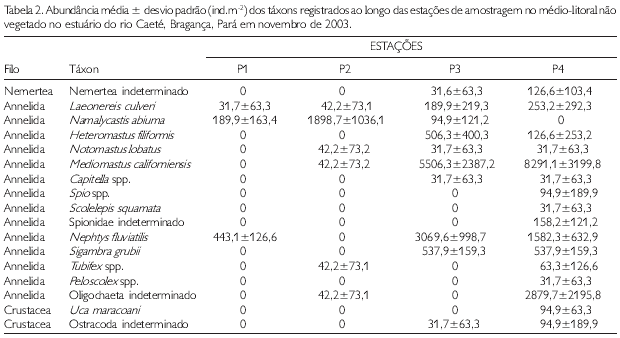
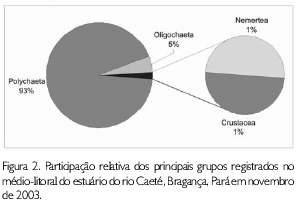
Entre os anelídeos, Polychaeta foi o grupo mais abundante em número de táxons (11) e indivíduos (87,25% do total). Os táxons mais abundantes, em ordem decrescente, foram Mediomastus californienses (52% do total), Nephtys iluviatilis (19% do total), oligoquetas da família Tubificidae (11% do total), Namalycastis abiuma (7% do total), Sigambra grubii (4% do total) e Heteromastus fililformis (2% do total). Os demais táxons ocorreram esporadicamente e foram pouco abundantes, representando sempre menos que 1% do total (Tabela 2).
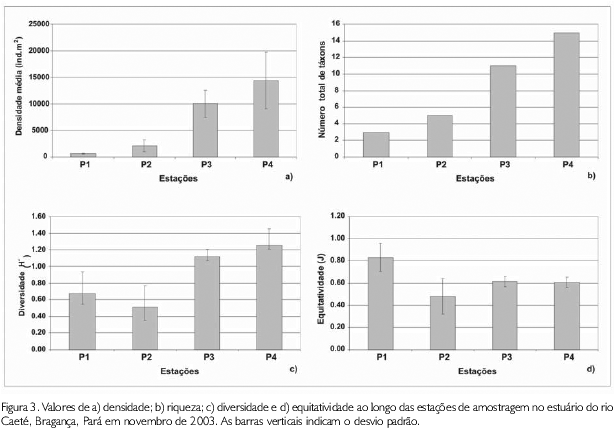
O número de espécies e de indivíduos aumentou gradativamente com a salinidade. Na região de baixa salinidade (5,1) foram registrados 664,6±63,3 ind.m-2 e, na zona de salinidade elevada (26,5), 14430,4±5333,9 ind.m-2 ; por sua vez, o número total de táxons passou de 3 para 16 na mesma direção (Figuras 3a e b). Observa-se, ainda, nas Figuras 3c e 3d, que a diversidade e a equitatividade apresentaram comportamento inverso, com o primeiro parâmetro máximo em P3 e P4 e o segundo em P1. Na estação P2, foram registrados os menores valores de diversidade e equitativadade (Figuras 3c e d).
A análise de agrupamento revelou a formação de três grupos a um nível de 50% de similaridade (Figura 4). O grupo A foi formado pelas estações P3 e P4, localizadas próximo a foz do estuário. Este grupo esteve caracterizado por altas salinidades (22,6 a 26,5) e substrato constituído por silte grosso e areia muito fina (Tabela 1). Nesse grupo foram registrados os valores mais elevados de riqueza (16 táxons), densidade média (12215,2±3941,6 ind.m-2) e diversidade (1,2±0,1). As espécies com maior contribuição para a formação desse grupo foram S. grubii, N. fluviatilis e M. californiensis (Tabela 3).
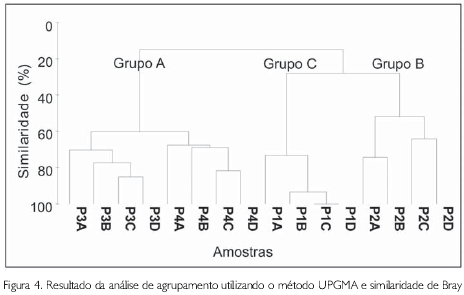
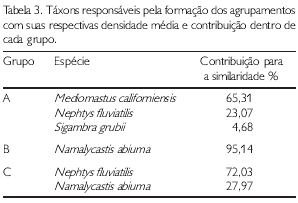
As amostras da estação P2, localizadas no estuário médio, reuniram-se para formar o grupo B, onde se registrou o menor valor de salinidade (3,6) e substrato areno-siltoso. A densidade média (2109,7±1105,9) e riqueza (6 táxons) tiveram valores intermediários quando comparado com os dois outros grupos. N. abiuma foi a principal responsável pela formação deste grupo (Tabela 3), representando 90% do total de indivíduos. A elevada dominância de N. abiuma nesse grupo determinou que nesse grupo fossem registrados os mais baixos valores de diversidade e equitatividade (Figuras 3c e d).
O grupo C, formado pelas amostras coletadas no estuário superior com salinidade 5,1 (estação P1), teve substrato siltoso. Nesse grupo foram registrados os menores valores de riqueza (3 táxons) e densidade média (664,6 ± 63,3 ind.m-2). Os Polychaeta N. abiuma e N. fluviatilis tiveram a maior contribuição para a formação desse grupo (Tabela. 3).
DISCUSSÃO
A fauna bentônica de áreas entre-marés não vegetadas no estuário do rio Caeté esteve composta por 17 táxons pertencentes a três filos, com dominância de Annelida. A densidade média e a riqueza aumentaram em direção à desembocadura, sendo máxima na estação mais próxima ao mar. A salinidade e as características dos sedimentos foram os principais fatores abióticos responsáveis pelas modificações na fauna, que pode ser dividida em três grupos de estações, sendo o primeiro com estações localizadas no estuário superior e mais pobre em abundância, riqueza e diversidade. Por outro lado, o grupo formado pelas amostras coletadas próximo à desembocadura foi o mias rico, abundante e diverso.
Em estuários tropicais, tradicionalmente, a macrofauna bentônica é composta principalmente por crustáceos e poliquetos (GAMBI; CONTI; BREMES, 1997). A classe Polychaeta não raro constitui o grupo dominante e mais importante em fundos moles estuarinos (OLIVEIRA; MOCHEL 1999; TENÓRIO; COELITO-SANTOS; SANTOS, 2000; DITTMAN, 2000). No rio Caeté, concordando com os resultados obtidos em outros estuários, Annelida foi o grupo mais rico e abundante, representando 65% dos táxons e 87,25% do total de indivíduos presentes.
Essa elevada ocorrência de anelídeos no estuário estudado foi fortemente determinada pelo tipo de substrato dominante na área, composto predominantemente por sedimentos ricos em silte e argila, rico em matéria orgânica (MANINO; MONTAGNA, 1997). A elevada oferta de alimento, por sua vez, favoreceu a colonização por espécies comedoras de depósito, como Mediomastus californiensis e oligoquetas da família Tubificidae, que representaram mais de 60% dos indivíduos coletados.
O número de táxons registrados no presente trabalho (17) é mais baixo que os registrados em outras áreas estuarinas, como no Golfo de Nicoya (Costa Rica), onde Maurer e Vargas (1984) citam a ocorrência de 205 espécies; no nordeste da Austrália, onde Dittman (1995) registrou a presença de 227 espécies em planos de lama na zona entre-marés; e no Golfo do México, onde Hernandez Alcantara e Solisweiss (1995) observaram 87 espécies. Mesmo numa área muito próxima, na ilha Canela (nordeste do Pará), Acheapong (2001) registrou maior valor de riqueza que a observada no estuário do rio Caeté.
A baixa riqueza da macrofauna registrada no presente trabalho pode ser explicada pelo elevado estresse a que essas comunidades estão submetidas, decorrentes de dois fatores principais: a costa paraense está situada numa área de macromarés semi-diurnas, com amplitude máxima de maré de 6 m, o que faz com que o substrato fique exposto ao ar por dois períodos de tempo de até seis horas ao longo do dia, provocando bruscas variações nas características físico-químicas do substrato; e, devido à sua posição geográfica na zona equatorial, a possibilidade da salinidade da água oscila entre 0 a 5 no período chuvoso (dezembro a maio) e 32 a 35 nos demais meses do ano (período menos chuvoso).
Respondendo ao gradiente de salinidade, no estuário do rio Curuçá, observa-se um incremento na densidade e na diversidade. Essa tendência ao aumento da riqueza, biomassa e diversidade é também observada em outros estudos como os feitos por Elliott e Kingston (1987), quando observaram, na baia Nuece (França), o incremento no número de espécies com o aumento da salinidade e diferenças na abundância e diversidade da macrofauna, dirigidas por flutuações da salinidade e variáveis hidrodinámicas. Barnes (1980, 1994) cita que a diversidade em estuários tende, em geral, a aumentar em direção a foz, uma vez que o número de espécies é maior no mar que em rios e estuários. Rosa Filho e Bemvenuti (1998) registraram valores mais elevados de abundância e riqueza em áreas próximas à desembocadura dos estuários no Rio Grande do Sul.
O aumento na diversidade em direção às zonas mais salinas dos estuários é explicada por diversos autores pela intolerância fisiológica da maioria das espécies estuarinas a baixos valores de salinidade (KINNE, 1971). Bulger (1993) cita que a salinidade é um fator determinante na distribuição da fauna e flora estuarina, dado que muitas espécies bentônicas apresentam intolerância fisiológica às variações na salinidade. No mesmo sentido, Wolff (1983) afirma que os gradientes de salinidade atuam como uma barreira natural às espécies estenohalinas.
O gradiente de salinidade no Caeté é ainda mais evidenciado quando considerado o índice de diversidade de Shannon, que foi o mais baixo no estuário superior, aumentando progressivamente com o incremento na salinidade e chegando ao máximo nas estações mais próximas à foz. A grande amplitude de salinidade observada é mais característica no período seco, que compreendeu os dias de coleta, quando a baixa pluviosidade e elevada evaporação reduzem a descarga fluvial e, em conseqüência, há uma maior penetração da cunha salina.
A granulometria pode ser considerada um agente controlador secundário da distribuição das espécies bentônicas do estuário do rio Caeté, pois o substrato predominantemente silte-arenoso é propício para a colonização de espécies escavadoras, como Nephtys fluviatilis e Heteromastus filiformis, resultando no adensamento da primeira espécie. Na estação P2 foram observados os maiores teores de areia. Neste ponto observou-se, em campo, erosão acentuada na margem oposta à área de coleta, prova de que a região está sujeita a forte hidrodinâmica, favorecendo a deposição de sedimentos mais grosseiros. Isto pode ter condicionado a não ocorrência da espécie N. fluviatilis nesta estação.
A diversidade também aumentou com o incremento do teor de areia nos sedimentos, o que já foi verificado em outros estuários. No setor polihalino na baía de Paranaguá, a riqueza de espécies, particularmente das formas infaunais, aumentou como reflexo das características dos sedimentos, dominados por areia muito fina (NETTO; LANA, 1995). Manino e Montagna (1997) correlacionaram a abundância bentônica na baia Nueces com as características sedimentares, registrando acréscimo da diversidade em sedimentos arenosos.
A formação de três grupos de estações refletiu a heterogeneidade ambiental no estuário do rio Caeté. A salinidade e a granulometria agruparam as estações P3 e P4 (grupo A) e afastaram-nas das demais. Cerca de 91% dos indivíduos e 94% das espécies foram registradas nesse grupo e 10 espécies (59%) ocorreram exclusivamente nele, muitas das quais são marinhas, como Sigambra grubii. Este grupo apresentou também as maiores densidade e diversidade, provavelmente em virtude da proximidade da foz resultar em maiores salinidades.
A granulometria foi responsável por separar os grupos B (estação P2) e C (estação P1). O grupo C apresentou baixa riqueza de espécies, provavelmente devido à maior influência fluvial, que resultou em salinidade baixa, condicionando que, nesse grupo, estivessem presentes apenas espécies tipicamente estuarinas, mais adaptadas. No grupo B, observou-se, ainda. um reduzido número de espécies, possivelmente devido à instabilidade físico-química e hidrodinâmica, permitindo sobrevivência somente de espécies tolerantes, como Namalycastis abiuma e Laeonereis culveri.
A dominância de um pequeno número de espécies e uma baixa diversidade são características comuns de comunidades estuarinas, formadas principalmente por espécies resistentes e que se reajustam às situações de estresse, sendo favorecidas e se aproveitando de todo espaço e recurso disponível (HOGARTH, 1999). Por essa razão, as espécies tipicamente estuarinas foram as que estiveram mais amplamente distribuídas. Por outro lado, espécies estenohalinas marinhas, como S. grubii, somente foram observadas nas estações localizadas no estuário inferior.
As espécies detritívoras L. culveri e N. fluviatilis são de ampla distribuição e tipicamente estuarinas (BEMVENUTI; CAPITOLO; GIANUCA, 1978; BEMVENUTI, 1997). Laeonereis ocorre predominantemente em substrato arenoso na região oligohalina de estuários (SANTOS; LANA, 2001). Esta espécie é comedora de depósitos de subsuperfície, sendo reconhecida por sua abundância em ambientes de baixa salinidade (SANTOS; LANA, 2001), talvez a razão pela qual ela tenha sido coletada em todas as áreas do estuário do Caeté.
Namalycastis abiuma é comumente encontrada na região entre-marés de banco lodosos, associada a troncos caídos de árvores de manguezais e mesmo em raízes de Rhizophora mangle (SANTOS; LANA, 2001). A espécie é típica de estuários tropicais e subtropicais, porém, exclusiva de águas quentes (SANTOS; LANA, 2001). Seu hábito alimentar é ingestão de depósito de superfície, já havendo sido encontrada por Santos e Lana (2000) sob o córtex do mangue vermelho R. mangle,em locais com salinidade em torno de 28.
Em conclusão, pôde-se observar que, no estuário do rio Caeté, as associações macrobentônicas são ricas em indivíduos mas pobres em espécies, refletindo a rigidez ambiental a que estão submetidos os organismos; e a salinidade é o principal fator estruturador dessas associações, estando fortemente correlacionada com as variações espaciais observadas nos descritores diversidade, distribuição e abundância. Mais estudos são requeridos para que haja melhor compreensão da estrutura e funcionamento dessas associações.
REFERÊNCIAS
ACHEAPONG, E. 2001. Distribution of macrozoobenthos abundance and biomass in intertidal soft sediments of North-east Brazil. 69f. Thesis (M.Sc.) - University of Bremen, Bremen.
BARNES, R. S. K. 1980. Coastal lagoons. Cambridge: Cambridge University Press. 106 p.
BARNES, R. S. K. 1994. Macrofaunal community structure and life histories in coastal lagoons. In: KJEFVE, B. Coastal Lagoon Process. New York: Elsevier. p. 311-362.
BEMVENUTI, C. E. 1997. Benthic invertebrates. In: SEELIGER, U.; ODEBRECHT, C.; CASTELLO, J. P. (Ed.). Subtropical convergence marine ecosystem: the coast and the sea in the warm temperate southwestern atlantic. New York: Springer Verlag. p. 43-46.
BEMVENUTI, C. E.; CAPITOLI, R. R.; GIANUCA, N. M. 1978. Estudos de ecologia bentônica na região estuarial da Lagoa dos Fatos: distribuição quantitativa do macrobentos infralitoral. Atlântica, v. 3, n. 2, p. 23-32.
BULGER, A. J. 1993. Biologically-based estuarine salinity zones derived from a multivariate analysis. Estuaries, v. 16, n. 2, p. 311-322.
CAPOBIANCO, J. P. R. et al. 2001. Biodiversidade na Amazônia brasileira: avaliação e ações prioritárias para a conservação, uso sustentável e repartição de benefícios. São Paulo: Instituto Socioambiental, Estação Liberdade. 540 p.
CLARKE, K. R.; WARWICK, R. M. 1994. Change in marine communities: an approach to statistical analysis and interpretation. Plymouth: Plymouth Marine Laboratory. 144 p.
DAUER, D. M.; EWIG, R. M.; RODI JR., A. J. 1987. Macrobenthic distribution within the sediment along an estuarine salinity gradient. Int. Revue ges Hydrobiol., v. 72, p. 529-538.
DITTMAN, S. 1995. Benthos structure on tropical tidal flats of Australia. Helgoländer Meeresunters, v. 49, p. 539-551.
DITTMAN, S. 2000. Zonation of benthic communities in a tropical tidal flat of north-east Australia. Journal of Sea Research, v. 43, p. 33-51.
ELLIOTT, M.; KINGSTON, P. F. 1987. The sublittoral benthic fauna of the estuary and Firth of Forth, Scotland. Proceeding of the Royal Society of Edinburgh, v. 93, p. 449-465.
FOLK, R.; WARD, W. C. 1957. Brazos River bar: a study in the significance of grain size parameters. Jour. Sed. Petrology, v. 27, p. 3-26.
FORBES, V. E.; LOPEZ, G. R. 1990. The role of sediment type in growth and fecundity of mud snails (Hydrobiidae). Oecologia, v. 83, p. 53-61.
GAMBI, M. C.; CONTI, G.; BREMEC, C. S. 1997. Polychaete distribution, diversity and seasonality related to seagrass cover in shallow soft-bottoms of the Tyrrenian Sea (Italy). Scientia Marina, v. 26, n. 1/2, p. 1-17.
HERNANDEZ ALCANTARA, P.; SOLISWEISS, V. 1995. Some macrobenthos communities associated with mangroves in the Terminos Lake (Gulf of Mexico). Revista de Biologia Tropical, v. 43, n. 1-2, p. 117-129.
HOGARTH, P. J. 1999. The biology of mangroves. Oxford: Oxford University Press. 228 p.
KENISH, M. J. 1986. Ecology of estuaries: biological aspects. Boca Raton: CRC Press Inc. 279 p. v. 2.
KINNE, O. 1971. Salinity. In: KINNE, O. Marine ecology: a comprehensive, integrated treatise on life in oceans and coastal waters. London: John Wiley & Sons. v. 1. n. 2. p. 683-995.
KJERFVE, B. et al. 2002. Morphodynamics of muddy environments along the Atlantic coasts of North and South America. In: HEALY, T.; WANG, Y.; HEALY, J. A. (Ed.). Muddy coasts of the world: processes, deposits and function. New York: Elsevier. p. 479-532.
LALLI, C. N.; PARSONS, T. R. 1997. Biological oceanography: an introduction. London: Butterworth Heinemann. 314 p.
LANA, P. C. et al. 1996. O bentos da costa brasileira: avaliação crítica e levantamento bibliográfico (1858-1996). Brasília, DF: MMA. 431 p.
LEVINTON, J. S. 2001. Marine biology: function, biodiversity ecology. Oxford: Oxford University Press. 420 p.
LITTLE, C. 2000. The biology of soft shores and estuaries. Oxford: Oxford University Press. 252 p.
MANINO, A.; MONTAGNA, P. A. 1997. Small-scale spatial variation of macrobenthic community structure. Estuaries, v. 20, p. 159-173.
MARTORANO, L. G. et al. 1993. Estudos climáticos do estado do Pará, classificação climática (Köppen) e deficiência hídrica (THORNTHWHITE, MATHER). Belém: SUDAM, EMBRAPA. 53 p.
MATNI, A. S.; MENEZES, M. P. M.; BATISTA, B. S. 2002. Comparação da estrutura florestal entre bosques de mangue salino e salobro da península Bragantina, Pará, Brasil. In: WORKSHOP ECOLAB, 3., Belém. Anais... [S.l.:s.n.]. 1 CD ROM.
MAURER, D.; VARGAS, J. A. 1984. Diversity of soft-bottom benthos in a tropical estuary: gulf of Nicoya, Costa Rica. Marine Biology, v. 81, p. 97-106.
PROST, Maria Thereza. (Coord.). 1999. Manguezais do litoral paraense: recursos naturais, uso social e indicadores para sustentabilidade. Belém: Museu Paraense Emílio Goeldi. 91 p. Relatório Técnico-Científico Parcial.
NETTO, S.; LANA, P. C. 1995. Zonação e estratificação da macrofauna bêntica em um banco areno-lodoso do setor euhalino de alta energia da Baía de Paranaguá (Paraná, Brasil). Iheringia, v. 79, p. 27-37.
OLIVEIRA, M.; MOCHEL, F. R. 1999. Macroendofauna bêntica de substratos móveis de um manguezal sob impacto das atividades humanas no sudoeste da Ilha de São Luís, Maranhão, Brasil. Boletim do Labohidro, v. 12, p. 75-93.
RHOADS, D. 1974. Organism-sediment relations on the muddy sea floor. Oceanogr. Mar. Biol. Ann. Rer., v. 12, p. 263-300.
ROSA-FILHO, J. S.; BEMVENUTI, C. E. 1998. Caracterización de las comunidades macrobentónicas de fondos blandos en regiones estuarinas de Rio Grande do Sul (Brasil). Thalassas, v. 14, p. 45-56.
ROSENBERG, R. 1995. Benthic marine fauna structured by hidrodynamic processes and food availability. Neth. J. Sea Res., v. 34, p. 303-317.
SANTOS, C. S. G.; LANA, P. C. 2000. Nereididae (Annelida; Polychaeta) da costa nordeste do Brasil. I. Padrões regionais e zoogeográficos de distribuição. Iheringia, Sér. Zool. v. 88, p. 181-189.
SANTOS, C. S. G.; LANA, P. C. 2001. Nereididae (Annelida, Polychaeta) da costa nordeste do Brasil. Gêneros Namalycastis, Ceratocephale, Laeonereis e Rutillienereis. Iheringia, Ser. Zool., v. 91, p. 137-149.
SILVA, M. G. L. 2001. Avaliação multitemporal da dinâmica costeira da praia do Pescador - Bragança (Norte do Brasil). 128 f. Dissertação (Mestrado) - Universidade Federal do Pará, Belém.
SIMITH, D. J. B. et al. 2002. Composição florística e abundância do fitoplâncton da baía do estuário do rio Caeté (Bragança - PA - Brasil). In: WORKSHOP ECOLAB, 6., Belém. Anais... [S.l.:s.n.]. 1 CD Rom.
SNELGROVE, P. V. R.; BUTTMAN, C. A. 1994. Animal-sediment relationship revisited: cause versus effect. Oceanogr. Mar. Biol. Ann. Rev., v. 32, p. 111-177.
WIJSMAN, J. W. M.; HERMAN, P. M. J.; GOMOIU, M. 1999. Spatial distribution in sediment characteristics and benthic activity on the northwestern Black Sea shelf. Mar. Ecol. Prog. Ser., v. 181, p. 25-39.
WOLFF, W. J. 1983. Estuarine benthos. In: KETCHUM, B. H. (Ed.). Ecosystems of the world: estuaries and enclosed seas. New York: Elsevier. p. 151-182.
TENÓRIO, D. O.; COELHO-SANTOS, M. A.; SANTOS, W. S. 2000. Biodiversidade bêntica do Canal de Santa Cruz, Itamaracá, Pernambuco, Brasil. In: MANGROVE. Recife: [s.n.]. p. 46.
 Endereço para correspondência:
Endereço para correspondência:
Editora do Museu Paraense Emílio Goeldi
Av. Magalhães Barata, 376
São Braz – CEP 66040-170
Caixa Postal 399
Telefone/fax: 55-91-3219-3317
E-mail: boletim@museu-goeldi.br
Recebido: 10/03/2005
Aprovado: 18/10/2006













