Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.1 n.1 Ananindeua mar. 2010
http://dx.doi.org/10.5123/S2176-62232010000100015
La caracterización fenotípica y genotípica de Serratia marcescens proveniente de la Unidad de Neonatología de Referencia de Belém, Pará, Brasil
Raimundo Gladson Corrêa CarvalhoI; Irna Carla do Rosário Souza CarneiroII; Marcelo Sena PinheiroIII; Surama da Costa PinheiroIV; Paulo Sérgio Roffe AzevedoIV; Schirley Dias dos SantosV; Ana Roberta Fusco da CostaVI; Francisco Lúzio de Paula RamosVI; Karla Valéria Batista LimaVI
ICurso de Pós-graduação
em Análises Clínicas, Centro Universitário do Pará,
Belém, Pará, Brasil. Laboratório de Patologia Clínica
e Laboratorial Dr. Paulo Azevedo, Belém, Pará, Brasil
IIDepartamento de Medicina, Universidade Federal do Pará,
Belém, Pará, Brasil
IIICurso de Pós-graduação em Análises
Clínicas, Centro Universitário do Pará, Belém,
Pará, Brasil
IVLaboratório de Patologia Clínica e Laboratorial
Dr. Paulo Azevedo, Belém, Pará, Brasil
VCurso de Pós-graduação em Análises
Clínicas, Centro Universitário do Pará, Belém,
Pará, Brasil. Seção de Bacteriologia e Micologia, Instituto
Evandro Chagas/SVS/MS, Ananindeua, Pará, Brasil
VISeção de Bacteriologia e Micologia, Instituto
Evandro Chagas/SVS/MS, Ananindeua, Pará, Brasil
Dirección para correspondencia
Endereço para correspondência
Correspondence
RESUMEN
La Serratia marcescens ha sido considerada como un agente importante de las infecciones relacionadas con la salud (IRAS, por sus siglas en portugués), y se ha destacado su alto nivel de resistencia intrínseca a los antimicrobianos utilizados en neonatología, además de persistir durante largos períodos de tiempo en el ambiente hospitalario. En este trabajo fueron evaluados a través de métodos fenotípicos y moleculares S. marcescens recuperados a partir de la colonización del tracto gastrointestinal o sepsis de aparición tardía en recién nacidos hospitalizados en la Unidad de Neonatología (UN) de Belém. La identificación de S. marcescens y las pruebas de sensibilidad se realizaron mediante el sistema automatizado Vitek (Biomerieux); la susceptibilidad al ertapenem se evaluó mediante la prueba de epsilometría (Oxoid). El genotipado se hizo mediante ERIC-PCR, utilizando partidores ERIC1 (5'-TGAATCCCCAGGAGCTTACAT-3') y ERIC2 (5'- AAGTAAGTGACTGGGGTGAGCG-3'). Se obtuvieron 22 cepas de S. marcescens, 15 recuperadas de hemocultivos y 7 de seguimiento (hisopado rectal); todas presentan resistencia a la ampicilina, ampicilina-sulbactam, gentamicina y cefazolina. No se presentó resistencia a la ciprofloxacina, imipenem, meropenem y ertapenem. En cuanto a los demás antibióticos evaluados, el perfil de susceptibilidad fue variable. Se obtubieron 11 patrones de amplificación por ERICPCR, dos de ellos compartidos por 14 aislamientos. Fue posible observar un patrón característico de las cepas polimórficas de la colonización gastrointestinal, excepto en dos casos que presentaron patrones de genotipos relacionados con los casos de sepsis. Los datos de este estudio confirman el alto nivel de resistencia de S. marcescens a los antibióticos, aunque todas las cepas fueron sensibles a ciprofloxacina y carbapenémicos. El tipaje a través de antibiograma y ERIC-PCR sugieren la dispersión de clones asociados con la colonización o la sepsis entre las salas de la Unidad de Neonatología del hospital estudiado.
Palabras clave: Serratia marcescens; Técnica de Tipificación Bacteriana; Reacción en Cadena de la Polimerasa; Farmacorresistencia Bacteriana.
INTRODUCCIÓN
La Serratia marcescens, perteneciente a la familia Enterobacteriaceae, ha sido relatada como importante agente de infecciones relacionadas a la salud (IRAS), destacándose por el potencial de diseminación y con el agravante de presentar elevado nivel de resistencia intrínseca a las drogas usadas en neonatología, y a los agentes antisépticos. Por colonizar la piel y el trato gastrointestinal de individuos adultos y neonatos, este patógeno persiste por largos períodos en el ambiente hospitalario11,2,6. Por eso, en seguida al relato de infecciones, es necesario investigar el origen del patógeno y mantener la vigilancia, por medio de tipado, para el efectivo control y/o erradicación de los casos.
Varios métodos han sido usados para tipado de cepas epidémicas de S. marcescens. Involucran tanto caracterización fenotípica como genotípica, y están basados en el presupuesto de que organismos relacionados poseen características únicas, que los distinguen de los no relacionados. Las características fenotípicas (bioquímica, resistencia a los antimicrobianos, serotipado, fagotipado, etc.) pueden no ser tan discriminatorias, siendo necesario el uso de métodos moleculares para la confirmación de la clonalidad. Las técnicas que utilizan electroforesis en gel de campo pulsado (PFGE) y ribotipado presentan buena discriminación, pero tienen la desventaja de que dan bastante trabajo, y necesitan de un largo período para la ejecución, además de equipos y reactivos caros9.
Técnicas moleculares basadas en la amplificación de ácidos nucleicos, como el Enterobacterial Repetitive Intergenic Consensus (ERIC), han sido utilizadas por la facilidad de ejecución y reproductibilidad, además de su concordancia con los resultados obtenidos por ribotipad5,2,12.
En este trabajo son evaluadas cepas de S. marcescens, en lo referido al perfil de resistencia a los antimicrobianos y a la caracterización genética, provenientes de colonización o sepsis tardías ocurridas en unidad neonatal (UN) de referencia en Belém.
MATERIALES Y MÉTODOS
CARACTERIZACIÓN DE LA INSTITUCIÓN Y LAS MUESTRAS
El estudio fue desarrollado en una UN con capacidad para 103 camas, en hospital de alta complejidad localizado en la ciudad de Belém, Pará. La unidad está constituida por nursery interna (para nacidos en el mismo hospital); unidad de tratamiento intensivo (UTI) neonatal; y nursery externa (BE). La nursery interna, por su vez, está dividida en cinco alas: Cuidados especiales (CE), Cuidados Intermedios (CI), Semi-intensiva (SI) y Sala de Transición (ST). La principal demanda de recién nacidos, atendida por la unidad, es de prematuros de bajo peso.
En los meses del estudio se realizaron 675 hemocultivos y 75 cultivos de vigilancia, para evaluar la colonización del trato intestinal por cepas de S. marcescens.
COLECTA Y SELECCIÓN DE LAS MUESTRAS
Los hemocultivos se realizaron a partir de 3 ml de sangre venosa de cada recién nacido utilizando el sistema automatizado BACTEC 9120 (Becton Dickinson). El control con relación a la colonización del agente en los neonatos, se realizó por cultivo de hisopado rectal, obtenido a partir del séptimo día de internación de los neonatos, y repetido semanalmente hasta el alta hospitalaria. Los cultivos primarios positivos fueron repicados en Agar sangre (Difco), Agar Cled (Difco) y Agar Mac-Conckey (Difco) e incubados en estufa bacteriológica (Fanen) a 37o C por 24 h. Para las colonias resultantes de bacilos Gram negativos no productores de oxidasa, se realizó una suspensión en solución salina 0,45% estandarizada en colorímetro (BioMerieux) hasta la concentración equivalente al tubo 0,5 de la escala de Mac-Farland (1,5 106 UFC/ mL) la que fue colocada en tarjetas GN para identificación en sistema automatizado VITEK (BioMérieux). Para este estudio se seleccionaron las especies S. marcescens.
La cepa de S. marcescens ATCC 8100 se usó como control en el genotipado, junto a una muestra no relacionada al brote.
ANÁLISIS DE SENSIBILIDAD
El perfil de susceptibilidad fue evaluado en sistema automatizado VITEC (BioMérieux) siguiendo la recomendación del fabricante. Fue evaluada la susceptibilidad de la S. marcescens a: ampicilina (AMP), ampicilina-sulbactam (SAM), amikacina (AN), aztreonan (ATM), cefepima (FEP), cefotaxima (CTX), cefoxitina (FOX), ceftazidima (CAZ), cefalotina (KF), gentamicina (GEN), piperacilina-tazobactam (PTZ), trimetoprim-sulfametoxazol (STX), imipenem (IPM), meropenem (MEM). La sensibilidad al ertapenem fue evaluada con auxilio de disco conteniendo 10 µg de la droga (Oxoid). La lectura de los halos de inhibición se hizo con el auxilio de una regla milimétrica.
GENOTIPADO DE LAS CEPAS POR ERIC-PCR
El DNA bacteriano se extrajo utilizando el método de hervido y congelación (15 min cada) y luego sometido a amplificación por medio de la técnica de reacción en cadena de la polimerasa (PCR), empleando los primers ERIC1 (5'-TGAATCCCCAGGAGCTTACAT-3') y ERIC2 (5'-AAGTAAGTGACTGGGGTGAGCG-3'), según el protocolo inicialmente descrito por Liu et al5. El análisis del polimorfismo de los fragmentos de restricción se hizo luego de electroforesis en gel de agarosa a 2%, seguido de la visualización en transiluminador de UV.
El desarrollo de este trabajo fue aprobado por el Comité de Ética en Investigación del Instituto Evandro Chagas, protocolo CEP/IEC no 003/07, el 14 de junio de 2007.
RESULTADOS
Se obtuvieron 22 cultivos de S. marcescens, recuperados a partir de episodios de sepsis y colonizaciones neonatales tardías, siendo 15 provenientes de hemocultivos de neonatos y siete de cultivo de control. Todas las muestras presentaron resistencia a: ampicilina, ampicilina-sulbactam, gentamicina y cefalotina. No se observó resistencia a: ciprofloxacina, imipenem, ertapenem, meropenem. Con relación a los demás antibióticos evaluados, el perfil de susceptibilidad fue variable (Cuadro 1).
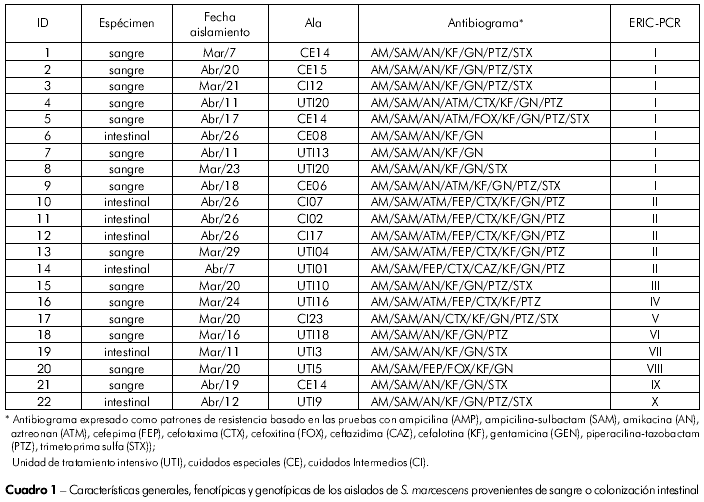
Se obtuvieron 11 patrones de amplificación por ERIC-PCR; ocho presentaron patrones con cinco o más amplificaciones en el rango de 100 a 3.000 pb (Figura 1); mientras que cuatro muestras presentaron menos de cinco amplificaciones (patrones 17, 19, 21). Dos patrones polimórficos fueron compartidos por 14 aislados (Cuadro 1, Figura 1).
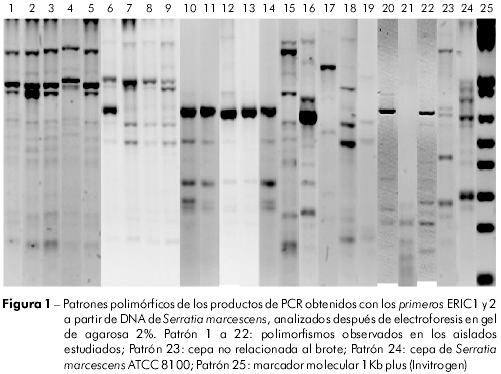
En el grupo I, ocho cepas fueron provenientes de hemocultivos de neonatos internados en diferentes alas de la UN, mientras la cepa de S. marcescens designada por el número 6 fue recuperada de colonización intestinal. En el grupo II, las cepas 10, 11, 12 y 14 fueron provenientes de hisopado rectal (vigilancia), mientras la cepa 13 fue de hemocultivo.
DISCUSIÓN
La Serratia marcescens puede estar asociada a infecciones esporádicas o epidémicas con el agravante de presentar elevado nivel de resistencia a los antimicrobianos recomendados en la terapéutica en neonatología11,6 y a los agentes antisépticos utilizados, lo que asegura la persistencia de este patógeno por largos períodos en el ambiente hospitalario. Una importante característica de este agente es la habilidad en producir β-lactamasas, que le otorgan resistencia a los antimicrobianos β-lactámicos de espectro extendido, complicando la terapia.
El esquema empírico de tratamiento de IRAS en UN depende del tiempo de aparecimiento de la infección (precoz: la evidenciada en las primeras 48 h de vida del recién nacido; o tardía: evidencia clínica y laboratorial de infección luego de las 48 h de vida del neonato); de la realización previa de procedimientos invasivos; del conocimiento de la microbiota local; y de los perfiles de resistencia bacteriana en cada hospital1. Los protocolos pueden ser definidos como formas estructuradas de apoyo al manejo técnico, las que incluyen definición de objetivos terapéuticos, secuencia temporal de cuidados, y estrategias diagnósticas y terapéuticas.
En el presente estudio, todas las muestras de S. marcescens se presentaron resistentes a la ampicilina y a la asociación ampicilina/sulbactam. El índice de resistencia a los aminoglicósidos gentamicina y amikacina también fue elevado (Cuadro 1). Martinez et al7, al evaluar 90 muestras de S. marcescens aisladas en 1994, en el Hospital de Clínicas de la Facultad de Medicina de Ribeirão Preto, observaron un 99% con resistencia a la ampicilina, un, 41% a la gentamicina y un 21% a la amikacina.
En este estudio, más del 70% (16) de las cepas de S. marcescens evaluadas presentaron resistencia al β-lactámico piperacilina asociado al inhibidor de β-lactamasa tazobactam. La asociación tazobactam-piperacilina ha sido una alternativa terapéutica para las IRAS causadas por bacilos Gram negativos y anaerobios productores de β-lactamasas en UTI, y más recientemente en UTIN cuando esos microorganismos son aislados en infecciones tardías. En la UN evaluada, la asociación tazobactam-piperacilina no deberá ser considerada para tratamiento de infecciones por S. marcescens.
Los agrupamientos observados luego del análisis del polimorfismo obtenido por ERIC-PCR para las cepas provenientes de pacientes internados en diferentes alas, configuran la diseminación entre las salas de CE, CI y UTI. De manera general, fue posible observar un patrón polimórfico característico para las cepas provenientes de colonización gastrointestinal; sin embargo, en dos casos, cepas provenientes de colonización estaban también relacionadas a casos de sepsis (Cuadro 1). No se evaluaron factores de riesgo asociados a la septicemia.
Levando en consideración que no hubo evolución del cuadro infeccioso en los neonatos portadores de las cepas 10, 11, 12 y 14, se confirma la necesidad de una asociación de factores de riesgo para el desarrollo de sepsis, ya que un 80% de los neonatos no presentó cuadro de septicemia.
El genotipado basado en la amplificación de elementos repetidos, semejante al ERIC-PCR, ha sido usado con suceso para caracterización de varios organismos, como el Mycobacterium tuberculosis10, Campylobacters8, Vibrio cholerae3, entre otros.
Evaluaron 22 muestras de S. marcescens, siendo siete recuperadas a partir del esputo de pacientes sometidos a ventilación mecánica durante brote de neumonía, y 15 no relacionadas al brote5. Los datos de tipado por ERIC-PCR evidenciaron dos agrupamientos entre las cepas relacionadas al brote y distintos perfiles entre las cepas no-relacionadas. Tales datos se confirmaron por ribotipado y perfil de resistencia a los antibióticos.
En este estudio se observaron diferencias entre los datos de tipado por ERIC-PCR y patrón de resistencia a los antimicrobianos. Hubo concordancia entre los métodos de tipado para las cepas 1, 2 y 3 (Grupo I); 6 y 7 (Grupo I); 10, 11, 12 y 13 (Grupo II), o sea, en 64,29% de las muestras evaluadas. Varios factores pueden justificar tal resultado. Primero: el patrón de susceptibilidad no se determinó siguiendo el método de disco difusión, estandarizado y recomendado actualmente por el Clinicai and Laboratory Standards Institute (CLSI)4; tal técnica es importante por ser la más completamente descrita, para la cual se desarrollaron patrones de interpretación apoyados por muchos datos laboratoriales y clínicos, cuyas dificultades y mejorías son constantemente debatidas. Segundo: el perfil de susceptibilidad bacteriana puede presentar alteraciones en espacio de tiempo inferior a los cambios en los patrones de ERIC-PCR. Los patrones polimórficos presentados en este estudio mantuvieron excelente reproductibilidad, evidenciando buena discriminación entre cepas relacionadas al brote y a las no-relacionadas.
En todos los agrupamientos generados por ERIC-PCR, el perfil de sensibilidad permitió la subdivisión de las cepas, con mayor variación de susceptibilidad a los antibióticos aztreonam, cefotaxima y cefoxitima; no obstante, tal hallazgo queda restricto a las cepas con alto índice de resistencia.
Las cepas de S. marcescens 8, 19 y 21 presentaron el mismo patrón de resistencia, diferenciándose con relación al polimorfismo obtenido por ERIC-PCR. La baja resolución fenotípica puede ser resultante del bajo índice de resistencia encontrado para estas muestras, ya que el 100% de las cepas presentaron resistencia a los antimicrobianos AM, SAM, NA, KF, GN. Las cepas 8, 19 y 21 presentaron también resistencia a STX, lo que se observó en 50% del muestreo evaluado. O sea, el tipado por caracterización del perfil de resistencia puede ser un indicativo de transmisión; sin embargo, otros métodos deben ser evaluados para la confirmación.
Se observa la necesidad de aumentar el muestreo del estudio para una mejor evaluación del tipado por análisis de antibiograma y ERIC-PCR, además de desarrollar genotipado secundario de las muestras por PFGE, actualmente considerado "patrón oro".
En el caso del agrupamiento de las cepas provenientes de control, la S. marcescens actúa apenas como un indicador de transmisión. Bien como la S. marcescens, es posible que otros patógenos sean transmitidos horizontal y concomitantemente, los que pueden haber pasado desapercibidos por no constituir el foco de la investigación.
Los datos obtenidos en este trabajo confirman el elevado índice de resistencia de las cepas de S. marcescens; sin embargo, todas las cepas evaluadas presentaron sensibilidad a los carbapenémicos y a la ciprofloxacina. El tipado por medio de ERIC-PCR permitió el agrupamiento de cepas, sugiriendo diseminación de clones asociados a la colonización o sepsis entre alas en la UN del hospital estudiado.
REFERENCIAS
1 Agência Nacional de Vigilância Sanitária (BR). Prevenção e controle de infecção hospitalar. Brasília: Ministério da Saúde; 2005.
2 Assadian O, Berger A, Aspöck C, Mustafa S, Kohlhauser C, Hirschl AM. Nosocomial outbreak of Serratia marcescens in a neonatal intensive care unit. Infect Control Hosp Epidemiol. 2002 Aug;23(8):457-6. DOI: 10.1086/502085 [ Links ]
3 Chokesajjawatee N, Zo YG, Colwell RR. Determination of clonality and relatedness of Vibrio cholerae isolates by genomic fingerprinting, using long-range repetitive element sequence-based PCR. Appl Environ Microbiol. 2008 Sep;74(17):5392-401. doi:10.1128/AEM.00151-08 [ Links ]
4 Clinical and Laboratory Standards Institute (USA). Performance standards for antimicrobial disk susceptibility tests; approved standard. 8th ed. Wayne, Pennsylvania; 2003. [ Links ]
5 Liu PYF, Lau YJ, Hu BS, Shir JM, Cheung MH, Shi ZY, et al. Use of PCR to study epidemiology of Serratia marcescens isolates in nosocomial infection. J Clin Microbiol. 1994;32(8):1935-8. [ Links ]
6 Maragakis LL, Winkler A, Tucker MG, Cosgrove SE, Ross T, Lawson E, et al. Outbreak of multidrug-resistant Serratia marcescens infection in a neonatal intensive care unit. Infect Control Hosp Epidemiol. 2008;29(5):418-23. DOI: 10.1086/587969 [ Links ]
7 Martinez R, Gironi RHAR, Santos VR. Sensibilidade bacteriana a antimicrobianos, usados na prática médica - Ribeirão Preto-SP - 1994. Medicina (Ribeirão Preto). 1996 abr-set;29(2-3):278-84. [ Links ]
8 Mouwen DJM, Weijtens MJBM, Capita R, Alonso-Calleja C, Prieto M. Discrimination of enterobacterial repetitive intergenic consensus PCR types of Campylobacter coli and Campylobacter jejuni by Fourier transform infrared spectroscopy. Appl Environ Microbiol. 2005 Aug;71(8):4318-24. DOI:10.1128/AEM.71.8.4318-4324.2005 [ Links ]
9 Parvaz P, Tille D, Meugnier H, Perraud M, Chevallier P, Ritter J, et al. A rapid and easy PCR-RFLP method for genotyping Serratia marcescens strains isolated in different hospital outbreaks and patient environments in the Lyon area, France. J Hosp Infect. 2002 Jun;51(2):96-105. [ Links ]
10 Sechi LA, Zanetti S, Dupré I, Delogu G, Fadda G. Enterobacterial repetitive intergenic consensus sequences as molecular targets for typing of Mycobacterium tuberculosis strains. J Clin Microbiol. 1998 Jan;36(1):128-32. [ Links ]
11 Villari P, Crispino M, Salvadori A, Scarcella A. Molecular epidemiology of an outbreak of Serratia marcescens in a neonatal intensive care unit. Infect Control Hosp Epidemiol. 2001 Oct;22(10):630-4. DOI: 10.1086/501834 [ Links ]
12 Vries JJ, Baas WH, Van der Ploeg K, Heesink A, Degener JE, Arends JP. Outbreak of Serratia marcescens colonization and infection traced to a healthcare worker with long-term carriage on the hands. Infect Control Hosp Epidemiol. 2006 Nov;27(11):1153-8. DOI: 10.1086/508818 [ Links ]
 Correspondência
/ Correspondence / Correspondencia:
Correspondência
/ Correspondence / Correspondencia:
Karla Valéria Batista Lima
Instituto Evandro Chagas,
Seção de Bacteriologia e Micologia
Rodovida BR 316, km 7, s/no,
Levilândia
CEP: 67030-000
Ananindeua-Pará-Brasil
Recebido em / Received / Recibido en: 30/07/2009
Aceito em / Accepted / Aceito en: 01/10/2009











 texto em
texto em 

