Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.1 n.2 Ananindeua jun. 2010
http://dx.doi.org/10.5123/S2176-62232010000200002
ARTIGO HISTÓRICO
Espécies neotropicais de Leishmania: uma breve revisão histórica sobre sua descoberta, ecologia e taxonomia
Ralph Lainson
Seção de Parasitologia, Instituto Evandro Chagas/SVS/MS, Belém, Pará, Brasil
Endereço
para correspondência
Correspondence
Dirección para correspondencia
Título original: The Neotropical Leishmania species: a brief historical review of their discovery, ecology and taxonomy. Traduzido por: André Monteiro Diniz.
RESUMO
Este artigo apresenta uma revisão dos mais importantes eventos históricos que levaram à atual classificação das espécies neotropicais de Leishmania e indica as doenças básicas causadas em seres humanos por estes diferentes parasitos, sem discutir os aspectos clínicos e epidemiológicos das leishmanioses. Para cada uma das espécies descritas, são fornecidas informações a respeito de sua conhecida distribuição geográfica, dos flebotomíneos hospedeiros registrados e de seus reservatórios mamíferos secundários, selvagens ou domésticos. Os dados apresentados levam à conclusão de que o parasito Leishmania (L.) infantum chagasi, agente causador da leishmaniose visceral americana, é provavelmente autóctone da região neotropical, e não importado durante a colonização ibérica.
Palavras-chave: Leishmania; Neotrópico; Ecologia; Taxonomia.
INTRODUÇÃO
A leishmaniose cutânea americana (LCA) parece ser uma doença antiga, que afligia humanos em áreas tropicais e subtropicais do Novo Mundo, como sugerido em antigas peças de cerâmica originárias do Peru e Equador (huacos). Essas peças geralmente retratavam rostos humanos com deformações graves bastante similares às causadas pela leishmaniose mucocutânea. Ademais, historiadores da época da colonização ibérica relatavam com frequência a ocorrência de lesões cutâneas nos habitantes nativos. Em 1571, Pedro Pizarro83 descreveu a desfiguração de narizes e lábios de plantadores de coca que trabalhavam na base das encostas orientais das Cordilheiras dos Andes. Como atualmente a leishmaniose mucocutânea é reconhecidamente endêmica nesta área, é bastante provável que aquele historiador se referisse a esta doença.
Aos poucos foi ficando evidente que as lesões cutâneas chamadas de uta pelos índios peruanos e a doença mucocutânea conhecida como espundia eram disseminadas pela maior parte do continente latinoamericano, onde receberam diversas denominações. As lesões menos destrutivas eram chamadas de uta seco, úlcera de Velez, ulcer de los chicleros, buba, úlcera de Baurú, ferida brava, botão do oriente, forest yaws, Bay-sore, pian-bois e bosch-yaws; já as mais destrutivas receberam as seguintes denominações: espundia, llaga corrosiva, cancro espúndico, nariz de tapir, tiacarana, gangosa, ferida esponjosa, e cancro fagendênico. No entanto, a etiologia destas lesões permaneceu desconhecida por muito tempo.
A leishmaniose visceral americana (LVA) pode ser tão antiga quanto a LCA na América Latina, porém oferece menor quantidade de evidências visuais externas de sua existência. Entretanto, a enfermidade conhecida no Brasil como barriga d'água (caracterizada por uma dilatação anormal do abdome), associada a episódios de febre e mal estar, era bastante conhecida, e boa parte de suas ocorrências foram provavelmente casos de LVA não diagnosticados.
Eventos importantes do histórico da LCA e da LVA na região neotropical, particularmente no Brasil, são descritos abaixo em ordem cronológica. Eles poderão ajudar a compreender como foi desenvolvida a classificação atual de seus agentes causadores.
INÍCIO
Por muitos anos, a uta peruana e outras lesões cutâneas semelhantes ocorridas em outros países da América Latina eram consideradas idênticas à denominada "botão do oriente", observada em países da região do Mediterrâneo e do continente asiático, cuja etiologia ainda suscitava dúvidas à época.
1909-1911
O agente causador do botão do oriente do Velho Mundo foi descoberto em 1903115 e denominado Leishmania tropica em 190662. Lesões cutâneas semelhantes encontradas na região neotropical só foram associadas a um parasita do gênero Leishmania em 1909, quando Lindenberg60 e Carini e Paranhos6, em estudos independentes, demonstraram "corpúsculos de Leishman-Donovan" (formas amastigotas) em lesões cutâneas de indivíduos acometidos de "úlcera de Baurú" no Estado de São Paulo, Brasil. Curiosamente, Lindenberg (Figura 1) publicou sua descoberta em um jornal, O Estado de São Paulo, em 30 de março de 1909, e Carini e Paranhos divulgaram seus achados no dia seguinte - no mesmo jornal! Finalmente, em 1911, Splendore105 demonstrou a presença do parasita em lesões mucocutâneas de espundia.

Inicialmente, acreditava-se que o parasita causador deveria ser denominado Leishmania tropica (Wright, 1903) Lühe, 1906, porém Gaspar Vianna111(Figura 2), clínico e parasitologista brasileiro, investigou formas amastigotas em lesões cutâneas de um paciente de Além Paraíba, Estado de Minas Gerais, Brasil, e concluiu (equivocadamente, como foi demonstrado posteriormente) que sua morfologia diferia da das formas amastigotas de L. tropica. Ele então denominou o parasita Leishmania brazilienses, posteriormente corrigido para L. braziliensis por Matta69, em 1916.

1913
Por muitos anos, houve um entendimento geral de que todas as leishmanioses cutâneas e mucocutâneas americanas seriam causadas por um único parasita, o L. braziliensis. No entanto, Velez110, talvez por motivações patrióticas, decidiu que o parasita causador da uta peruana não era nem o L. tropica nem o L. braziliensis e chamou-o de Leishmania peruviana.
O primeiro relato de LVA nas Américas foi provavelmente o de Migone74, em 1913. Ele observou o que considerou serem formas amastigotas no sangue de um paciente no Paraguai. Os sintomas reportados eram altamente indicativos de LVA. O paciente não respondeu satisfatoriamente ao tratamento contra a malária e morreu. Antes de adoecer, ele havia trabalhado na construção da notória ferrovia São Paulo-Corumbá, no Brasil, onde, acredita-se, teria sido infectado.
1934-1937
Mesmo com casos esporádicos de LVA surgindo em diversos países das Américas do Sul e Central, demorou certo tempo até que evidências definitivas da existência da doença fossem obtidas no Brasil. Em 1934, porém, 41 casos foram diagnosticados após análise de tecidos de fígado removidos por viscerotomia80 (Figura 3). Três deles eram originários do Estado do Pará, e representaram o primeiro registro da LVA na Amazônia.

Sabia-se que tanto a L. donovani quanto a L. infantum, agentes causadores da leishmaniose visceral do Velho Mundo, facilmente infectavam animais de laboratório. Em 1937, após Cunha e Chagas12 não conseguirem infectar hospedeiros semelhantes com o parasita extraído de casos de LVA no Brasil, denominaram o parasita Leishmania chagasi.
1945-1948
No Brasil, merece destaque a descoberta, por Medina71, de um misterioso parasita que causava lesões na pele do porquinho-da-índia doméstico (Cavia porcellus), em 1946; este parasita foi posteriormente denominado Leishmania enriettii Muniz & Medina, 1948. Este achado foi um claro indicativo da presença de outras espécies dermotrópicas de Leishmania, além da L. braziliensis, e que poderiam infectar o ser humano no país. Até a década de 1960, ainda se acreditava que todos os casos de LCA humano no país eram causados por L. braziliensis. Este entendimento geral persistiu apesar de o agente causador da doença na floresta confluente, localizada no país vizinho da Guiana Francesa, ter sido denominado L. guyanensis Floch, 1954.
Em 1946, Convit e Lapenta9 descreveram uma forma estranha de leishmaniose cutânea em pacientes na Venezuela. Esta forma caracterizava-se por um grande número de lesões nodulares espalhadas pelo corpo e que continham uma enorme quantidade de amastigotas grandes. Os pacientes apresentaram resultado negativo para o teste de Montenegro e não apresentaram resposta ao tratamento usual com antimoniais. A enfermidade foi então denominada leishmaniose cutânea difusa (LCD) e seu agente causador na Venezuela foi posteriormente chamado de Leishmania pifanoi73.
1953-1961
No Panamá, em 1957, pesquisadores107,106demonstraram a presença de uma espécie de Leishmania no roedor silvestre Proechimys semispinosus. Outras infecções também foram registradas por Forattini20 em roedores silvestres no Estado de São Paulo, Brasil, em 1960. Em nenhum dos casos, entretanto, foi demonstrado conclusivamente que o organismo era idêntico ao parasita que infectava humanos dentro daquela mesma localidade.
Naquele momento estava ficando claro que diferentes parasitas dermotrópicos do gênero Leishmania eram provavelmente responsáveis pela ocorrência de leishmaniose cutânea em diferentes partes da região neotropical. O parasita causador da úlcera dos chicleros em Yucatán, Guatemala e Belize, foi denominado Leishmania tropica mexicana por Biagi3, em 1953. Na Guiana Francesa, Floch19 adotou a mesma nomenclatura trinomial, referindo-se à causa de "pian-bois" por L. tropica guyanensis em 1954. Do mesmo modo, em outras localidades da América do Sul, o mesmo autor considerou ser a leishmaniose cutânea causada por L. tropica braziliensis. No entanto, em 1959, Medina e Romero73, juntamente com vários outros pesquisadores, corretamente desaprovaram o nome específico "tropica" para os parasitas associados à LCD na Venezuela. Em 1961, o parasitalogista brasileiro Pessôa81, seguindo a mesma corrente, listou as espécies conhecidas de Leishmania nas Américas como L. braziliensis braziliensis, L. b. guyanensis, L. b. peruviana, L. b. pifanoi e L. b. mexicana.
1962-1965
Em 1962, Garnham23 elevou o parasita causador da úlcera dos chicleros em Belize, América Central, a um nível específico, como Leishmania mexicana. Além disso, em 1962 e 1964, durante investigações acerca da epidemiológica desta doença, Lainson e Strangways-Dixon56,57 afirmaram que roedores selvagens eram os reservatórios deste parasita, e que eles frequentemente apresentavam lesões visíveis e ricas em formas amastigotas em suas caudas. Um voluntário foi infectado com sucesso por um parasita proveniente de roedor, e uma análise comparativa biológica e bioquímica do organismo com os de casos de LCA demonstrou que eles eram idênticos. Esta foi a primeira associação conclusiva de um parasita neotropical de Leishmania que reconhecidamente infectava humanos com um reservatório silvestre em animais selvagens.
Naturalmente, foi levantada a suspeita de que um reservatório roedor de L. braziliensis semelhante existisse nas florestas do Brasil. Em uma visita ao Instituto Evandro Chagas (IEC) em 1963, este autor discutiu com o Dr. Orlando Costa, diretor do IEC, e com o Dr. Otis Causey, chefe de seu programa de arbovírus, a possibilidade de se implementar um programa de colaboração a respeito da eco-epidemiologia da LCA na Amazônia.
Causey ficou impressionado com a semelhança das lesões em caudas causadas pela L. mexicana e as observadas em roedores capturados na floresta do Utinga, em Belém, Brasil. Ele havia considerado que elas teriam sido causadas por infecções bacterianas em caudas lesionadas e comprometeu-se em examiná-las em mais detalhes no futuro. Algumas semanas depois, ele presenteou este autor com um esfregaço corado pelo método de Giemsa de uma lesão na cauda de um espécime de Oryzomys capito, um roedor selvagem comum na área em que foi capturado. Essa amostra era rica em formas amastigotas de Leishmania. Esta descoberta, surpreendentemente rápida, deu ensejo a uma negociação com a Fundação Wellcome Trust, de Londres, que concordou em implantar uma Unidade de parasitologia (Wellcome Parasitalogy Unit -WPU) na Seção de Parasitologia do IEC, por um período de três anos, com a promessa de maior apoio caso os resultados das pesquisas realizadas o justificassem. A cooperação IEC/WPU durou até o ano de 1992.
1965-1967
O parasita encontrado em Oryzomys foi primeiramente definido como sendo L. braziliensis por Nery-Guimarães e Costa77 em 1964. No entanto, esta conclusão não foi corroborada pela comparação daquele parasita com os extraídos de casos de leishmanioses cutâneas e mucocutâneas humanas, realizada pela WPU. Inicialmente, as formas amastigotas do parasita do roedor eram claramente maiores que as de L. braziliensis e, quando inoculadas na pele de camundongos e hamsters de laboratório, produziam rapidamente grandes lesões, semelhantes a tumores, com altas concentrações de formas amastigotas. Por outro lado, L. braziliensis produzia um pequeno nódulo que normalmente levava vários meses até se tornar visível e que continha um baixo número de formas amastigotas relativamente pequenas. Além disso, o parasita - que hoje, sabe-se, infecta muitos roedores e marsupiais silvestres (Figura 4) - cresceu de forma exuberante em meio de cultura ágar sangue (NNN) convencional; já L. braziliensis apresentou dificuldade para sobreviver naquele meio, e suas cepas isoladas geralmente morriam após várias subculturas. Em 1969 e 1970, Lainson e Shaw49,45 referiram-se a essas diferenças como um comportamento característico de "cepas rápidas e lentas" de Leishmania.
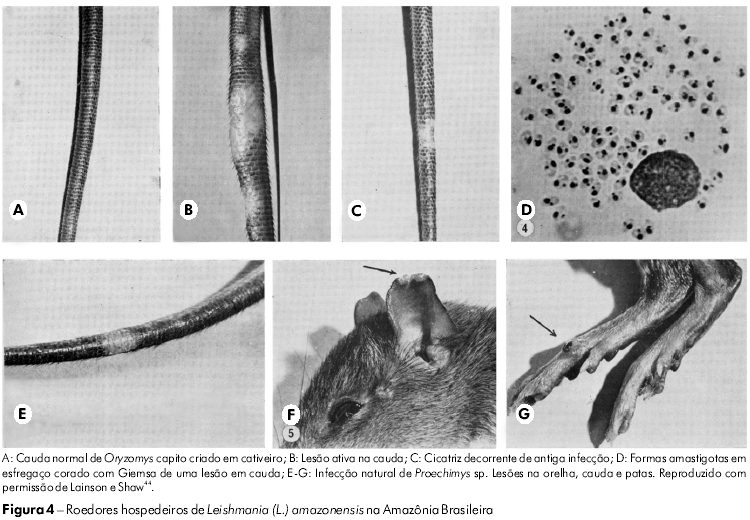
A análise contínua de isolados de Leishmania coletados de pacientes direcionados ao IEC logo demonstrou que um pequeno número de parasitas eram iguais aos extraídos de Oryzomys e outros roedores. Foi demonstrado, também, que o parasita era responsável pela enfermidade conhecida como LCD ou, mais especificamente, da leishmaniose cutânea anérgica difusa (LCAD), uma infecção altamente desfigurante, que acomete indivíduos imunologicamente incompetentes e que resiste ao tratamento usual com drogas antileishmania. Devido à grande semelhança entre os aspectos biológicos do parasita e os apresentados pela L. mexicana encontrada na América Central, ele foi denominado L. mexicana amazonensis Lainson e Shaw, 1972.
1968
Neste ano a raposa Cerdocyon thous foi incriminada pela primeira vez como um importante reservatório do parasita responsável pelas leishmanioses viscerais canina e humana na Amazônia, àquela época descritas por alguns como L. chagasi e por outros como L. donovani. Três raposas infectadas52,54 foram encontradas perto da floresta do Utinga, na periferia de Belém. Posteriormente, foram encontrados dez animais infectados entre 25 examinados (40%) na Ilha do Marajó, Pará54, o que constitui um número surpreendentemente alto. Nenhum desses animais demonstrava qualquer sinal externo da doença.
1977
Esfregaços do tecido de fígado e baço extraídos de um porco-espinho da espécie Coendou prehensilis, capturado em uma área de floresta no Estado do Pará, revelaram a presença de formas amastigotas medindo até 6,8 x 4,5 µm43, um tamanho surpreendentemente grande, mesmo quando comparado a amastigotas de L. m. amazonensis. Em 1971, Herrer27 deu o nome Leishmania hertigi a um parasita encontrado em porcos-espinhos no Panamá; consequentemente, para o parasita encontrado no Coendou brasileiro foi dado o nome subespecífico de Leishmania hertigi deanei em homenagem a Leonidas Deane. Deane encontrou o que seria provavelmente o mesmo parasita em porcos-espinhos originários do Estado do Piauí, Brasil, porém, incerto de sua natureza, absteve-se de nomeá-lo. O caráter semelhante à leishmania deste estranho parasita foi indicado pela produção (ainda que temporária) de formas amastigotas na pele de hamsters inoculados experimentalmente, bem como pela formação de estágios típicos de promastigotas em meio de cultura de ágar-sangue. Em 1980, Miles et al76 distinguiram os parasitas de L. (L.) hertigi hertigi e L. mexicana amazonensis por meio da comparação de seus perfis isoenzimáticos.
1979
Uma espécie de Leishmania foi isolada do fígado e baço de um tatu-galinha, Dasypus novemcinctus, da área de Monte Dourado (Jari), no norte do Pará, Brasil51.
Suas características biológicas, bem como o desenvolvimento de técnicas imunológicas e bioquímicas, aos poucos serviram de base para tentativas preliminares de classificar o crescente número de espécies identificadas e aceitas como pertencentes ao gênero Leishmania46,50,42,117,51. As observações acerca do modo de desenvolvimento dessas espécies em seus vetores flebotomíneos foram particularmente importantes, e deram ensejo à divisão dos parasitas em três grupos distintos, denominados Seções (Figura 5).
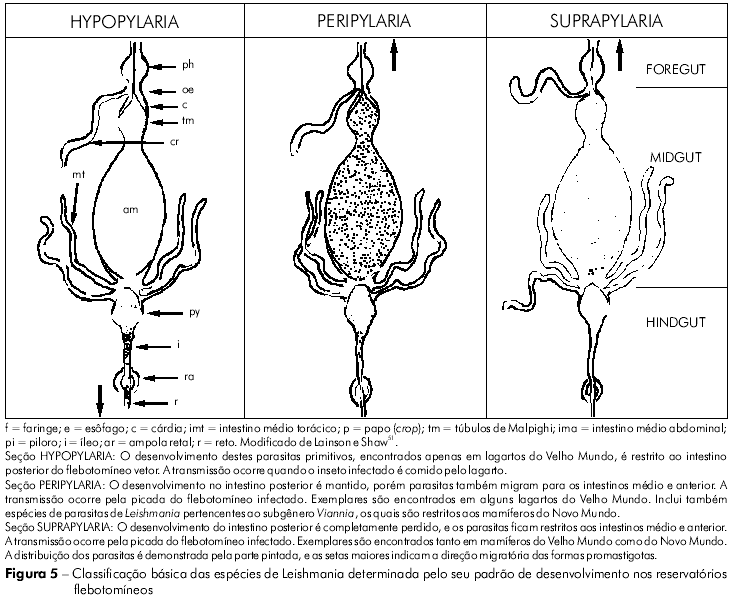
CLASSIFICAÇÃO INICIAL DAS ESPÉCIES DO GÊNERO LEISHMANIA51
SEÇÃO HYPOPYLARIA (de hypo = sob, e pyl = portão)
Os parasitas pertencentes a este grupo foram considerados as espécies mais primitivas, e seu desenvolvimento é restringido a uma posição posterior no piloro, íleo e reto do intestino do flebotomíneo. Os reservatórios são aparentemente restritos a alguns lagartos do Velho Mundo, em cujas vísceras ou sangue o parasita pode tomar as formas amastigota e/ou promastigota. As espécies listadas incluem Leishmania agamae David, 1929, e L. ceramodactyli Adler & Theodor, 1928. Sua transmissão geralmente segue-se à ingestão, pelo lagarto, do flebotomíneo infectado. Alguns estudiosos35, dentre eles este autor, entendem que estes parasitas deveriam ser classificados sob o gênero Sauroleishmania Ranque, 1973.
SEÇÃO PERIPYLARIA (de peri = por todos os lados, e pyl = portão)
Essas espécies de Leishmania se desenvolvem obrigatoriamente no intestino posterior do flebotomíneo. No entanto, além disso, têm também migrado para o intestino anterior. Neste grupo estão incluídos os seguintes parasitas encontrados em lagartos do Velho Mundo: Leishmania adleri Heisch, 1958, e Leishmania tarentolae Wenyon, 1921. O parasita pode então ser transmitido por meio da picada de um flebotomíneo infectado ou quando este é ingerido. Esta Seção foi dominada pelo que Lainson e Shaw chamaram de complexo L. braziliensis51 do Novo Mundo. Naquele momento, este complexo incluía os seguintes parasitas: L. braziliensis Vianna, 1911; L. peruviana Velez, 1913; L. guyanensis Floch, 1954; e L. panamensis Lainson & Shaw, 1972. Todos eles infectam humanos.
SEÇÃO SUPRAPYLARIA (de supra = sobre, e pyl = portão)
Considerava-se que essas espécies de Leishmania haviam perdido o seu desenvolvimento no intestino posterior do flebotomíneo, e que os parasitas encontravam-se restritos agora aos intestinos médio e anterior. Eles são encontrados na pele, nas vísceras e no sangue de mamíferos do Velho Mundo e da região neotropical; sua transmissão ocorre por meio da picada do flebotomíneo vetor infectado. Esta Seção foi dividida em quarto complexos:
Complexo L. donovani
Leishmania donovani (Laveran & Mesnil, 1902) Ross, 1903 (Velho Mundo); Leishmania infantum Nicolle, 1908 (Velho Mundo); Leishmania chagasi Cunha & Chagas, 1937 (Novo Mundo).
Complexo L. mexicana
L. mexicana mexicana (Biagi, 1953) Lainson & Shaw, 1979; L. mexicana amazonensis Lainson & Shaw, 1972; L. mexicana pifanoi (Medina & Romero 1959) Medina & Romero, 1962; L. mexicana aristidesi Lainson & Shaw, 1979; L. mexicana enriettii Muniz & Medina, 1948 (todos do Novo Mundo).
Complexo L. hertigi
L. hertigi hertigi Herrer, 1971; L. hertigi deanei Lainson & Shaw, 1977 (Novo Mundo).
Complexo L. tropica
Leishmania tropica (Wright, 1903) Lühe, 1906; Leishmania major Yakimov & Schockov, 1914; Leishmania aethiopica Bray, Ashford & Bray, 1973 (todos do Velho Mundo).
Em 1982, a pesquisadora russa Saf'janova91 distinguiu as chamadas leishmanias de lagartos das verdadeiras espécies de Leishmania em mamíferos por meio da utilização dos subgêneros Sauroleishmania Ranque, 1973, e Leishmania Ross, 1903, respectivamente. Dentro do subgênero Leishmania, ela considerou que o complexo L. donovani era constituído por Leishmania (L.) donovani, L. (L.) infantum (Velho Mundo) e L. (L.) chagasi (Novo Mundo). No entanto, ela não levou em consideração o desenvolvimento de L. braziliensis e leishmânias neotropicais relacionadas no intestino posterior de flebotomíneos (membros da Seção Peripylaria51) como sendo de importância taxonômica, e agrupou todos os parasitas neotropicais como sendo L. (L.) amazonensis, L. (L.) mexicana, L. (L.) braziliensis e L. (L.) panamensis (leishmanioses tegumentares), e L. (L.) chagasi (leishmaniose visceral). Além disso, Saf'janova considerava não haver critérios taxonômicos suficientes para incluir L. braziliensis peruviana e L. braziliensis guyanensis em sua classificação. A exclusão destes dois últimos parasitas deveu-se provavelmente à falta de acesso à literatura mais recente, cujos estudos já haviam indicado de forma clara uma caracterização específica baseada em evidências biológicas, bioquímicas e sorológicas40,70,75.
1987 UMA CLASSFICAÇÃO REVISADA DAS ESPÉCIES NEOTROPICAIS DE LEISHMANIA
Estudos abrangentes sobre a ecologia e epidemiologia da leishmaniose cutânea na Amazônia Brasileira revelaram um aumento constante no número de espécies de Leishmania, caracterizadas de forma mais adequada por meio de seus perfis enzimáticos76. Este fato deu azo à realização de uma revisão taxonômica41.
Em 1977, Lainson et al58 ressaltaram a importância de se levar em consideração a ocorrência ou ausência de desenvolvimento no intestino posterior do flebotomíneo para distinguir os parasitas do complexo L. braziliensis (com desenvolvimento no intestino posterior) dos parasitas do complexo L. mexicana (sem desenvolvimento no intestino posterior)58. Nesse diapasão, a classificação revisada incluiu todas as espécies que apresentaram desenvolvimento no intestino posterior no novo subgênero Viannia, nome este dado em homenagem a Gaspar Vianna, que descrevera L. (V.) braziliensis, agora a espécie-tipo do subgênero em questão. Todas as espécies que não apresentaram desenvolvimento do intestino posterior foram então incluídas no subgênero Leishmania Ross, 1903, utilizado por Saf'janova91 em 1982. Ademais, ao comentarem a "extensa combinação de dados geográficos nas denominações dos parasitas, o que por vezes criava um conflito absurdo entre elas" (por exemplo, L. braziliensis guyanensis e L. mexicana venezuelensis), propuseram a elevação das subespécies a um patamar específico. Com essas modificações, foi dada às espécies de Leishmania na região neotropical a classificação exposta a seguir41.
SUBGÊNERO LEISHMANIA ROSS, 1903
Definição: Apresenta as características do gênero Leishmania. O ciclo de vida no inseto hospedeiro era limitado aos intestinos médio e anterior. Espécie-tipo: Leishmania (Leishmania) donovani (Laveran & Mesnil, 1903) Ross, 1903. Incluía os seguintes parasitas neotropicais: Leishmania (L.) chagasi Cunha & Chagas, 1937; L. (L.) enriettii Muniz & Medina, 1948; L. (L.) mexicana Biagi, 1953 emend. Garnham, 1962; L. (L.) amazonensis Lainson & Shaw, 1972; L. (L.) aristidesi Lainson & Shaw, 1979; L. (L.) venezuelensis Bonfante-Garrido, 1980; L. (L.) garnhami Scorza et al, 1979; L. (L.) pifanoi (Medina & Romero, 1959) Medina & Romero, 1962; L. (L.) hertigi Herrer, 1971; L. (L.) deanei Lainson & Shaw, 1977.
SUBGÊNERO VIANNIA LAINSON & SHAW, 1987
Definição: Apresenta as características do gênero Leishmania. O ciclo de vida no inseto hospedeiro incluía uma fase de desenvolvimento prolífera em que apresentava formas paramastigotas arredondadas e ovoides, bem como algumas formas promastigotas coladas à parede do intestino posterior (piloro e/ou íleo) por meio de hemidesmossomos flagelares. Porém, ocorre uma migração dos parasitas para os intestinos médio e anterior. Espécie-tipo: Leishmania (Viannia) braziliensis.
As espécies deste subgênero são conhecidas apenas no Novo Mundo e são as seguintes: L. (V.) braziliensis Vianna, 1911, emend Matta, 1916; L. (V.) peruviana Velez, 1913; L. (V.) guyanensis Floch, 1954; L. (V.) panamensis Lainson & Shaw, 1972.
CONTINUAÇÃO DAS PESQUISAS SOBRE AS ESPÉCIES NEOTROPICAIS DE LEISHMANIA
1987
O uso de anticorpos monoclonais tornou-se um método consolidado para a identificação da Leishmania (Viannia) braziliensis em flebotomíneos infectados97.
1988-1989
Uma nova espécie pertencente ao subgênero Viannia foi isolada de uma preguiça, de um procionídeo e de duas espécies de macacos de uma floresta de planície ao pé da Serra dos Carajás, Estado do Pará, Brasil38. Este parasita foi denominado Leishmania (Viannia) shawi Lainson et al, 1989.
O parasita que havia sido isolado de um tatu-galinha (Dasypus novemcinctus) em 1979 foi caracterizado e finalmente denominado Leishmania (Viannia) naiffi Lainson & Shaw, 1989.
1991
Kreutzer et al36 descreveram uma nova espécie de Leishmania que infectava humanos na Colômbia e no Panamá, e nomeou-a L. (Viannia) colombiensis.
1992
Grimaldi et al26 isolaram outro parasita ainda não descrito da preguiça Choloepus hoffmanni e do esquilo Sciurus granatensis no Equador e deram a ele o nome de L. (V.) equatorensis.
2002
Foi descoberto que um parasita isolado de casos de LCA em soldados envolvidos em missões realizadas em florestas degradadas na Cidade de Belém, Estado do Pará, Brasil, diferia de todas as espécies de Leishmania encontradas na região amazônica99. Foi então denominado Leishmania (Viannia) lindenbergi Silveira et al, 2002.
2003
Em 1977, foi isolada uma espécie de Leishmania, do subgênero Viannia, de um único espécime do flebotomíneo Lutzomyia tuberculata, extraído do tronco de uma grande árvore da floresta do Utinga. Ela permaneceu no criobanco do IEC por um longo tempo, até ser caracterizada e denominada Leishmania (Viannia) utingensis Braga et al, 20034.
1998/2005
A consolidação do subgênero Viannia e a caracterização de outros parasitas de Leishmania isolados de flebotomíneos, mamíferos selvagens e pacientes com LCA deram ensejo a duas outras publicações, que acabaram por modificar e atualizar a classificação vigente48,47.
Uma mudança importante na classificação anterior dos parasitas do subgênero Leishmania foi a proposta pelos autores Lainson e Shaw47, em 2005, de dividir Leishmania (L.) infantum em duas subespécies: L. (L.) infantum infantum (Velho Mundo) e L. (L.) infantum chagasi (Novo Mundo). Além disso, a nova classificação incluía a Leishmania (L.) forattinii Yoshida et al, 1993, um parasita encontrado no Brasil, em um gambá, o Didelphis marsupialis aurita, e em um roedor, o Proechimys iheringi denigratus.
Todas as espécies neotropicais de Leishmania reconhecidas até o presente momento, sua distribuição geográfica, seus hospedeiros flebotomíneos suspeitos e comprovados, seus hospedeiros mamíferos e os dados clínicos relacionados àquelas que infectam humanos estão apresentados a seguir.
CLASSIFICAÇÃO ATUAL DAS ESPÉCIES NEOTROPICAIS DE LEISHMANIA
Adaptado de Cox11 e Lainson e Shaw47.
Reino: Protozoa Goldfuss, 1818
Filo: Euglenozoa Cavalier-Smith, 1998
Classe: Kinetoplastea: Honigberg, 1963
Ordem: Trypanosomatida Kent, 1880
Família: Trypanosomatidae Doflein, 1901
Gênero: Leishmania Ross, 1903
Subgênero: Leishmania Ross, 1903
Subgênero: Viannia Lainson & Shaw, 1987
SUBGÊNERO LEISHMANIA
LEISHMANIA (LEISHMANIA) INFANTUM CHAGASI (CUNHA & CHAGAS, 1937) SHAW, 2002
Distribuição geográfica conhecida
Maior parte do continente latino-americano, incluindo Argentina, Bolívia, Brasil, Colômbia, Equador, El Salvador, Guadalupe, Guatemala, Honduras, Martinica, México, Nicarágua, Paraguai, Suriname e Venezuela.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Lutzomyia) longipalpis é o seu principal vetor em toda a área de ocorrência da LVA14,37, porém, Lu. evansi também foi incriminada na Colômbia e na Venezuela109,17. Lu. (Lu.) cruzi tornou-se fortemente suspeita de ser um vetor alternativo no Estado do Mato Grosso do Sul, Brasil, após o isolamento de L. (L.) infantum chagasi de 14 espécimes93. No entanto, as fêmeas de Lu. cruzi e de Lu. longipalpis são indistinguíveis, e mesmo os machos das duas espécies só podem ser diferenciados com base em pequenas diferenças. Os autores concluíram que as fêmeas infectadas eram de Lu. cruzi, haja vista que os machos de Lu. longipalpis estavam aparentemente ausentes no período estudado. Apesar de a presença de Lu. longipalpis na mesma área já ter sido confirmada94, parece haver poucas dúvidas atualmente acerca da possibilidade de Lu. (Lu.) cruzi ser considerado um vetor alternativo da Leishmania (L.) infantum chagasi no Estado do Mato Grosso do Sul.
Hospedeiros mamíferos registrados
Os canídeos selvagens Cerdocyon thous ("raposa caranguejeira")52,54 e Speothos venaticus ("cachorro vinagre")18, os felídeos Panthera onca (onça pintada) e Felis concolor (suçuarana)13, os gambás Didelphis marsupialis10,108 e D. albiventris98, o cachorro doméstico e humanos.
Infecção em humanos
L. (L.) chagasi causa predominantemente a leishmaniose visceral, que é geralmente fatal quando não tratada adequadamente, porém sua infecção pode ser assintomática em alguns indivíduos. Na Costa Rica, a infecção ocorre majoritariamente na forma de lesões cutâneas não ulcerativas116, e em Honduras e Nicarágua, a infecção é tanto visceral como cutânea84,2.
Há opiniões divergentes sobre o fato de o parasita L. (L.) chagasi ser autóctone dos trópicos americanos ou se a ocorrência da doença no Novo Mundo é causada por L. (L.) infantum, a qual foi introduzida por imigrantes ibéricos, ou por seus cachorros, há cerca de 500 anos. Alguns argumentos em defesa da hipótese de o parasita ser indígena estão expostos a seguir37,54,48,47:
1. Em termos geológicos, 500 anos é um período muito curto para que o parasita tenha atingido uma distribuição tão vasta por toda a América Latina, do México à Argentina.
2. A especificidade de hospedeiro das espécies de Leishmania na natureza é mais pronunciada nos flebotomíneos, que são normalmente considerados os hospedeiros primários das espécies de Leishmania. Portanto, parece ser improvável que L. (L.) infantum introduzida pudesse ter dado um salto repentino do gênero Phlebotomus, no Velho Mundo, para o gênero Lutzomyia, nas Américas. Lutzomyia (Lutzomyia) longipalpis é o principal vetor de L. (L.) infantum chagasi por toda a sua distribuição geográfica14,37, e não há informações sobre o vetor transmitir nenhuma outra espécie de Leishmania.
3. Com base em dados moleculares, é frequente a menção de que os parasitas denominados L. (L.) infantum e L. (L.) chagasi são idênticos. Já há, entretanto, algumas publicações (convenientemente ignoradas) que afirmam haver diferenças entre esses dois organismos. Essas distinções têm sido demonstradas por meio da digestão com endonuclease de restrição, por hibridização de DNA de cinetoplasto33,32 e nos perfis de radiorrespirometria dos dois parasitas16,15; por fim, as diferenças antigênicas têm sido defendidas devido a suas respectivas formas promastigotas92. Consequentemente, estes achados, salvo se comprovadamente refutados, deveriam ser levados em consideração em qualquer discussão acerca da taxonomia destes dois organismos.
4. No ciclo de transmissão de L. (L.) infantum chagasi pela população nativa de Lutzomyia longipalpis entre os animais selvagens, verifica-se uma alta taxa de prevalência da infecção na raposa Cerdocyon thous, nativa do Brasil54 e no gambá Didelphis marsupialis na Colômbia10,108. Já foram documentadas também infecções esporádicas em outros animais selvagens, incluindo o gambá Didelphis albiventris98, o "cachorro vinagre" Speothos venaticus18, a onça Panthera onca e a suçuarana Felis concolor13. Todas as infecções registradas nestes animais eram de natureza inaparente e benigna, o que seria mais sugestiva a existência de uma antiga relação hospedeiro-parasita do que a infecção com um parasita estranho e recentemente introduzido.
A grande diversidade de espécies de Leishmania no Novo Mundo fez com que surgisse a hipótese de que seus parasitas teria se originado nos trópicos americanos78,79, e que o gênero Leishmania foi introduzido no Velho Mundo via ponte terrestre de Bering. Outros autores63, mesmo concordando com esta hipótese, têm afirmado que, após a introdução deste parasita ancestral no Velho Mundo e a evolução de Leishmania donovani e Leishmania infantum (há estimados 14-24 milhões de anos), este último foi introduzido no Novo Mundo por meio dos colonizadores ibéricos.
Para este autor, parece igualmente razoável sugerir que, enquanto a evolução deste antigo parasita ocorria no Velho Mundo, levando ao surgimento não só dos parasitas viscerotrópicos L. (L.) donovani e L. (L.) infantum, mas também dos membros dermotrópicos do complexo L. (L.) tropica, outro processo de evolução deste mesmo parasita ocorria no Novo Mundo, produzindo o parasita viscerotrópico L. chagasi e os parasitas dermotrópicos do subgênero Leishmania (por exemplo, os parasitas pertencentes aos complexos L. mexicana e L. hertigi). Ao mesmo tempo, outra vertente em termos evolucionários divergiu, formando o subgênero Viannia, cujos membros mantiveram as características primitivas de desenvolvimento no intestino posterior nos flebotomíneos. Este grupo de parasitas é desconhecido no Velho Mundo, possivelmente devido ao fato de que sua forma ancestral nunca tenha sido introduzida via ponte terrestre de Bering, uma vez que seus hospedeiros mamíferos apresentavam uma limitada capacidade de locomoção.
A denominação L. (L.) infantum Nicolle, 1908 tem claramente prioridade cronológica sobre L. (L.) chagasi Cunha & Chagas, 1937, e sentimo-nos obrigados a aceitar a denominação específica infantum para o parasita em ambos os hemisférios. A separação geográfica prolongada pode explicar as já mencionadas diferenças registradas entre as duas populações, sugerindo que seria melhor considerá-las como sendo as subespécies L. (L.) infantum chagasi e L. (L.) infantum infantum95,39,47,11.
Tem havido uma certa controvérsia acerca da autoria desta proposta. Inicialmente, foi sugerida por Lainson e Shaw47, em capítulo de sua autoria, denominado "New World Leishmaniasis", que fora submetido para publicação da 10a edição da obra "Topley & Wilson's Microbiology and Microbial Infections". No entanto, houve um atraso incomum até que esta edição da obra tenha sido publicada, o que ocorreu somente em 2005. Durante este ínterim, tanto Shaw95, em 2002, como Lainson e Rangel39, em 2003, utilizaram os novos nomes subespecíficos em outras publicações. Portanto, cronologicamente falando, os nomes subespecíficos corretos da L. infantum devem ser grafados L. (L.) infantum infantum (Nicolle, 1908) Shaw, 2002 e L. (L.) infantum chagasi (Cunha & Chagas, 1937) Shaw, 2002.
LEISHMANIA (L.) ENRIETTII MUNIZ & MEDINA, 1948
Distribuição geográfica conhecida
Apenas nos Estados do Paraná71 e São Paulo65, Brasil.
Hospedeiros flebotomíneos conhecidos
Lu. monticola e Lu. correalimai são suspeitos: o primeiro já foi infectado experimentalmente quando alimentado em lesões de porquinhos-da-índia64.
Hospedeiros mamíferos registrados
Há registros de infecções naturais apenas em porquinhos-da-índia domésticos (Cavia porcellus).
Infecção em humanos
Ainda não há registros; todas as tentativas de infectar voluntários falharam.
LEISHMANIA (L.) MEXICANA (BIAGI, 1953) GARNHAM, 1962
Distribuição geográfica conhecida
Belize, Guatemala, Honduras, Costa Rica, sul dos EUA. Registros de ocorrências em países sul-americanos muito distantes geograficamente devem ser analisados com cautela.
Hospedeiros flebotomíneos conhecidos
Lutzomyia olmeca olmeca é um vetor comprovado. Lu. diabolica é suspeito no norte do México e no sul do Estado do Texas, e Lu. anthophora é suspeita no Estado do Arizona.
Hospedeiros mamíferos registrados
Os roedores silvestres Ototylomys phyllotis, Nyctomys sumichrasti, Heteromys desmarestianus, Sigmodon hispidus; Neotoma albigula, no sul dos EUA (Arizona); humano.
Infecção em humanos
Leishmaniose cutânea, com uma tendência forte a causar lesões no ouvido externo (chiclero's ear). Casos ocasionais de LCAD.
LEISHMANIA (L.) PIFANOI (MEDINA & ROMERO, 1959) MEDINA & ROMERO, 1962
Distribuição geográfica conhecida
Aparentemente limitada à Venezuela, particularmente nos Estados de Yaracuy, Lara e Miranda.
Hospedeiros flebotomíneos conhecidos
Incertos, mas possivelmente Lutzomyia flaviscutellata.
Hospedeiros mamíferos registrados
Humanos. Apesar de os reservatórios animais selvagens de L. (L.) pifanoi serem ainda desconhecidos, Lima et al59 sugeriram que os roedores Sigmodon hispidus e Rattus rattus poderiam ser hospedeiros de várias Leishmania spp., incluindo, presumivelmente, a L. (L.) pifanoi.
Infecção em humanos
Até o presente momento, todos os casos registrados foram de LCAD.
LEISHMANIA (LEISHMANIA) AMAZONENSIS LAINSON & SHAW, 1972
Distribuição geográfica conhecida
Bolívia, Brasil, Colômbia, Guiana Francesa e Paraguai. Ocorre provavelmente em outros países neotropicais onde exista o vetor flebotomíneo.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Nyssomyia) flaviscutellata é o seu mais44,96,113,112, importante vetor , com registros de infecções ocasionais em flebotomíneos taxonomicamente próximos a ele, Lu. (N.) olmeca olmeca and Lu. (N.) reducta. Um parasita, identificado como L. (L.) amazonensis, foi isolado de 16 dentre 1.715 espécimes de Lu. nuneztovari68 na Bolívia.
Hospedeiros mamíferos registrados
Os roedores selvagens terrestres Proechimys spp., Oryzomys spp., Nectomys, Neacomys, e Dasyprocta; os marsupiais Marmosa, Metachirus, Didelphis e Philander; a raposa Cerdocyon thous; humanos.
Infecção em humanos
Leishmaniose cutânea com lesão única, localizada, e, em pacientes com um sistema imunológico mediado por células deficientes, LCAD. Alguns raros casos de leishmaniose visceral têm sido atribuídos a este parasita exclusivamente no Estado da Bahia, Brasil1. O espectro clínico e imunopatológico da leishmianiose cutânea americana já foram descritos, com particular referência a sua forma disseminada, causada por L. (L.) amazonensis e L. (V.) braziliensis, o que ilustra a sua extrema patogenicidade nos extremos de LCAD e da leishmaniose mucocutânea100.
LEISHMANIA (LEISHMANIA) ARISTIDESI (LAINSON & SHAW, 1979) EMEND LAINSON & SHAW, 1987
Distribuição geográfica conhecida
Floresta de Sasardi, na região de San Blas, leste do Panamá.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Nyssomyia) olmeca bicolor é um vetor putativo, baseado em sua predominância em armadilhas modelo Disney com isca de roedor e marsupial em áreas onde animais infectados também foram coletados7.
Hospedeiros mamíferos registrados
O gambá Marmosa robinsoni e os roedores Proechimys semispinosus e Dasyprocta punctata29,30.
Infecção em humanos
Desconhecida, apesar de haver registros ocasionais de que Lu. olmeca bicolor se alimente de humanos.
LEISHMANIA (LEISHMANIA) GARNHAMI SCORZA ET AL, 1979
Distribuição geográfica conhecida
Andes venezuelanos.
Hospedeiros flebotomíneos conhecidos
Lu. youngi é o seu vetor mais suspeito. Um parasita encontrado em um espécime infectado produziu formas amastigotas na pele de um hamster inoculado. Suspeitou-se que essas formas fossem L. (L.) garnhami, mas o parasita não foi identificado definitivamente66.
Hospedeiros mamíferos registrados
O gambá Didelphis marsupialis e humanos.
Infecção em humanos
LCA da forma localizada simples.
LEISHMANIA (LEISHMANIA) VENEZUELENSIS BONFANTE-GARRIDO, 1980
Distribuição geográfica conhecida
Venezuela, nos Estados de Lara e Yaracuy.
Hospedeiros flebotomíneos conhecidos
Ainda não foi identificado um vetor definitivo, mas há suspeitas de envolvimento de Lu. olmeca bicolor e Lu. rangeliana.
Hospedeiros mamíferos registrados
Seus hospedeiros mamíferos selvagens permanecem incertos, mas o parasita já foi registrado no gato doméstico e em humanos. Foi sugerido que os roedores Sigmodon hispidus e Rattus rattus são potenciais reservatórios de várias Leishmania spp.59, inclusive, presumivelmente, L. (L.) venezuelensis.
Infecção em humanos
Lesões cutâneas únicas ou múltiplas. Em alguns casos, nódulos espalhados podem ser confundidos com LCAD, porém a infecção responde bem ao tratamento antimonial.
LEISHMANIA (LEISHMANIA) FORATTINII YOSHIDA ET AL, 1993
Distribuição geográfica conhecida
Brasil, nos Estados de São Paulo, Bahia e Espírito Santo.
Hospedeiros flebotomíneos conhecidos
Ainda não identificados, porém Lu. (Psychodopygus) ayrozai e Lu. yuilli já foram infectados experimentalmente.
Hospedeiros mamíferos registrados
O roedor Proechimys iheringi e o marsupial Didelphis marsupialis, no Estado de São Paulo.
Infecção em humanos
Ainda não há registro, mas como os vetores suspeitos alimentam-se de sangue humano, infecções em humanos devem ser reportadas no futuro.
LEISHMANIA (LEISHMANIA) HERTIGI HERRER, 1971
Distribuição geográfica conhecida
Panamá e Costa Rica.
Hospedeiros flebotomíneos conhecidos
Seu vetor flebotomíneo ainda não foi descoberto. As altas taxas de infecção em seu reservatório mamífero sugerem que ele habite áreas próximas ao[s] vetor[es], possivelmente em árvores ocas.
Hospedeiros mamíferos registrados
O porco-espinho tropical Coendou rothschildi. Foram conduzidos estudos exaustivos em outros animais selvagens, que não revelaram nenhum outro hospedeiro mamífero.
Infecção em humanos
Não há registros, possivelmente devido à incapacidade de este parasita sobreviver em tecidos humanos ou porque seu vetor nunca pica humanos.
LEISHMANIA (LEISHMANIA) DEANEI LAINSON & SHAW, 1977
Distribuição geográfica conhecida
Até o presente momento, registrada apenas na Amazônia Brasileira.
Hospedeiros flebotomíneos conhecidos
Seu hospedeiro invertebrado permanece desconhecido. Flebotomíneos da espécie Lutzomyia (Viannamyia) furcata, que habitam árvores, foram coletados de uma árvore oca habitada por um porco-espinho infectado na floresta do Utinga, Belém, Pará, Brasil. Foram observadas formas promastigotas em seu repasto sanguíneo ainda não digerido. No entanto, não houve qualquer evidência de que os parasitas tinham migrado para o intestino anterior, e eles desapareceram após a digestão completa do sangue41.
Hospedeiros mamíferos registrados
O porco-espinho arborícola Coendou p. prehensilis. L. (L.) deanei, como L. (L.) hertigi, apresenta uma alta taxa de infecção neste porco-espinho. Extensas análises em outros mamíferos selvagens sugerem que este seja o único reservatório mamífero do parasita.
Infecção em humanos
Não há registros. Como no caso de L. (L.) hertigi, esta falta de registro pode ser explicada pelo fato de seu organismo não sobreviver em tecidos humanos ou simplesmente porque o seu vetor nunca picar humanos.
Na classificação de 200547, esses dois misteriosos parasitas foram agrupados sob o título "Leishmania-like parasitas of uncertain taxonomic position" (parasitas com características semelhantes às de Leishmania, de taxonomia incerta), principalmente porque estudos moleculares79 haviam sugerido que eles seriam mais diretamente relacionados a Endotrypanum (um flagelado endoeritrocítico encontrado em preguiças) do que a Leishmania. Entretanto, seus nomes atuais foram mantidos47 até que mais dados sejam coletados, e, por esta razão, este autor os agrupa juntamente com membros do subgênero Leishmania. Com base na ausência de formas de L. (L.) deanei aderidas ao intestino posterior de Lutzomyia furcata, ainda que em infecções transitórias, este parasita certamente não parece ser um membro do subgênero Viannia. Espera-se que o conhecimento a respeito dos ciclos de vida completos destes dois organismos em seus hospedeiros invertebrados naturais venha a indicar o seu exato status taxonômico.
Apesar de os dois membros do complexo L. hertigi parecerem ser característicos aos porcos-espinhos, eles são facilmente distinguíveis pela análise de seus perfis isoenzimáticos e por uma diferença marcante na morfologia de suas formas amastigotas: as de L. (L.) hertigi são estranhamente alongadas e medem apenas de 3,5 x 1,2 a 4,8 x 2,5 μm, enquanto as de L. (L.) deanei são arredondadas e, com 5,1 x 3,1 a 6,8 x 3,7 μm, são as maiores entre todas as espécies de Leishmania de que se tem registro.
O SUBGÊNERO VIANNIA
LEISHMANIA (VIANNIA) BRAZILIENSIS (VIANNA, 1911) EMEND MATTA, 1916
Distribuição geográfica conhecida
Apesar de parasitas denominados alternativamente de L. braziliensis ou L. braziliensis lato sensu terem sido relatados em quase todos os países da América Latina, da Argentina ao México, ainda restam dúvidas acerca da verdadeira natureza de vários registros, devido ao uso de métodos inadequados de identificação no passado. Alguns podem ter sido simples zimodemos de L. (V.) braziliensis e outros podem vir a ser descobertos como espécies diferentes e não identificadas do subgênero Viannia.
Hospedeiros flebotomíneos conhecidos
As incertezas referentes à exata distribuição geográfica do L. (V.) braziliensis dificultam a identificação de todos os seus vetores. Porém, pelo menos no Brasil, onde o parasita já foi registrado em todos os estados, resta claro que há várias espécies de flebotomíneos envolvidas em sua transmissão, incluindo Lutzomyia (Nyssomyia) intermedia, Lu. (N.) whitmani strictu sensu, Lu. (Psychodopygus) wellcomei, Lu. migonei85 e Lu. (N.) neivae (Pinto, 1926) (para referência, veja as "Considerações Finais" abaixo).
Em um estudo recente na área do Projeto Salobo, na Serra dos Carajás, Pará, Brasil, formas promastigotas de quatro espécimes de Lu. (Psychodopygus) davisi foram identificadas como sendo L. (V.) braziliensis, enquanto outras extraídas de espécimes de Lu. (Psychodopygus) hirsuta (3 infectadas), Lu. (Nyssomyia) umbratilis (3), Lu. (N.) richardwardi (2), Lu. (Trichophoromyia) brachipyga (2), Lu. (T.) ubiquitalis (2), Lu. trinidadensis (1) e Lu. migonei (1) ainda não foram identificadas104. Lu. (P.) davisi já foi apontado como um importante vetor da leishmaniose cutânea zoonótica no Estado de Rondônia25.
No Estado do Pará, perto da Cidade de Paragominas, um parasita identificado como sendo L. (V.) braziliensis foi isolado de um flebotomíneo com a morfologia dúbia de fêmeas de Lu. (P.) complexa e Lu. (P.) wellcomei103. As fêmeas dessas duas espécies são morfologicamente indistinguíveis. No entanto, concluiu-se que o espécime infectado era Lu. (P.) complexa devido à ausência aparente de machos de Lu. (P.) wellcomei.
Hospedeiros mamíferos registrados
O voo baixo do flebotomíneo Lu. (Psychodopygus) wellcomei, vetor importante de L. (V.) braziliensis na Serra dos Carajás, Pará55, e a forte atração exercida pelas armadilhas com isca de roedor levaram a suspeitas iniciais de que roedores terrestres e alguns marsupiais pudessem ser os reservatórios deste parasita114,55.
Antes do desenvolvimento de técnicas bioquímicas, sorológicas e moleculares para a caracterização e identificação de isolados de Leishmania, só era possível basear-se em características biológicas ("extrínsecas") dos parasitas, tais como o tamanho das formas amastigotas e seu comportamento em meio de cultura convencional e inoculados em animais de laboratório. Tomando por base estas características juntamente com o padrão de desenvolvimento dos parasitas em flebotomíneos infectados experimentalmente (para indicar os membros do subgênero Viannia), os primeiros pesquisadores podiam ao menos dizer que os isolados de animais selvagens em áreas altamente endêmicas de LCA humana causada por L. (V.) braziliensis eram provavelmente este parasita. Esses registros incluem os seguintes animais:
Oryzomys concolor, O. capito, O. nigripes, Akodon arviculoides, Proechimys spp., Rattus rattus, Rhipidomys leucodactylus (Rodentia) e Didelphis marsupialis (Marsupialia)21,22,45,51,53,88, todos no Brasil; na Venezuela, Rattus rattus e Sigmodon hispidus (Rodentia)59. Finalmente, parasitas dos roedores brasileiros Bolomys lasiurus e Rattus rattus foram classificados conclusivamente como L. (V.) braziliensis por meio de eletroforese enzimática multilocus5.
Foram identificadas lesões cutâneas causadas por L. (V.) braziliensis em animais domésticos, incluindo equinos, cachorros e gatos, em áreas que sugerem um ciclo de transmissão peridoméstico. Esses relatos têm origem principalmente da Argentina, Bolívia, Brasil, Colômbia e Venezuela. Humanos são comumente infectados.
Infecção em humanos
Leishmaniose cutânea, geralmente com uma ou poucas lesões. A infecção frequentemente leva à leishmaniose mucocutânea. O espectro clínico e imunopatológico da leishmaniose cutânea americana já foi descrita em outros estudos100, com particular referência às espécies disseminada e mucocutânea.
LEISHMANIA (VIANNIA) PERUVIANA VELEZ, 1913
Distribuição geográfica conhecida
Peru, na região a oeste dos Andes, em áreas com vegetação escassa e uma população restrita de animais selvagens. Essa área pode se estender às áreas montanhosas da Argentina e outros países andinos.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Helcocyrtomyia) peruensis e Lutzomyia verrucarum são fortemente suspeitos, sendo que um parasita com características biológicas semelhantes às dos coletados de humanos e cachorros já foi isolado do primeiro28.
Hospedeiros mamíferos registrados
Cachorros e humanos. Um estudo recente descreveu o isolamento deste parasita extraído do roedor Phyllotis andinum e do gambá Didelphismarsupialis61.
Infecção em humanos
Leishmaniose cutânea simples, com uma ou poucas lesões. Não há registros de que o parasita cause a leishmaniose mucocutânea.
LEISHMANIA (VIANNIA) GUYANENSIS FLOCH, 1954
Distribuição geográfica conhecida
Esta espécie silvestre frequentemente infecta humanos no Brasil, particularmente na área ao norte do rio Amazonas e nos países vizinhos da Guiana Francesa e Suriname. Também há registros de infecção na Colômbia, Equador, Venezuela e em florestas de planície no Peru.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Nyssomyia) umbratilis é o seu vetor principal. Há registros de infecções relativamente esporádicas em Lu. (N.) anduzei (Revisões47,85). Alguns registros iniciais de infecção em Lu. (N.) whitmani s.l. podem ter sido, na verdade, de Leishmania (Viannia) shawi.
Hospedeiros mamíferos registrados
Os hospedeiros selvagens mais importantes são a preguiça real Choloepus didactylus e o tamanduá-mirim Tamandua tetradactyla53,24. Há registros ocasionais da infecção em roedores e gambás. A infecção em animais selvagens é benigna e inaparente.
Infecção em humanos
Leishmaniose cutânea, apresentando uma ou várias lesões, as quais podem ser causadas por múltiplas picadas de flebotomíneos infectados ou por disseminação linfática metastática. Casos raros de envolvimento mucocutâneo já foram reportados.
LEISHMANIA (VIANNIA) PANAMENSIS LAINSON & SHAW, 1972
Distribuição geográfica conhecida
Área do Canal do Panamá, Panamá; também registrado na Colômbia, Costa Rica, Equador, Honduras, Nicarágua e Venezuela.
Hospedeiros flebotomíneos conhecidos
O Lutzomyia (N.) trapidoi é considerado o seu vetor mais importante. Várias outras espécies são consideradas vetores secundários, incluindo Lu. (N.) ylephiletor, Lu. (Lu.) gomez e Lu. (Psychodopygus) panamensis34,8.
Hospedeiros mamíferos registrados
A preguiça Choloepus hoffmanni é o seu reservatório mais importante, porém há relatos de infecções ocasionais nas preguiças Bradypus infuscatus e B. griseus. Este parasita também já foi relatado em vários outros animais arborícolas, incluindo Bassaricyon gabbi, Nasua nasua e Potos flavus (Procyonidae), os macacos Aotus trivirgatus e Saguinus geoffroyi e o roedor terrestre Heteromys sp.29,30. Cães de caça, assim como os humanos, geralmente tornam-se "hospedeiros vítimas", apresentando lesões cutâneas visíveis.
Infecção em humanos
Leishmaniose cutânea, apresentando de uma a várias lesões; raros casos da doença do tipo mucocutânea foram registrados.
LEISHMANIA (VIANNIA) LAINSONI SILVEIRA ET AL, 1987
Distribuição geográfica conhecida
Áreas de floresta do Brasil, Peru e Bolívia.
Hospedeiros flebotomíneos conhecidos
Até o presente momento, Lutzomyia (Trichophoromyia) ubiquitalis102 é o seu único vetor conhecido. Este inseto é o primeiro representante do subgênero Trichophoromyia a ser incriminado como vetor de uma espécie de Leishmania. Lu. (T.) velascoi é altamente suspeito de ser vetor na Bolívia67.
Hospedeiros mamíferos registrados
Até o presente momento, apenas o grande roedor Agouti paca101 e humanos foram identificados como hospedeiros.
Infecção em humanos
A infecção por este parasita geralmente apresenta uma única lesão; nenhum caso de leishmaniose mucocutânea foi registrado até o presente momento.
LEISHMANIA (VIANNIA) NAIFFI LAINSON & SHAW, 1989
Distribuição geográfica conhecida
Esta espécie foi isolada nos Estados do Pará e Amazonas, Brasil, e na Guiana Francesa. No entanto, será provavelmente registrada em outras partes da América Latina, onde o reservatório mamífero e os vetores flebotomíneos coexistem.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Psychodopygus) ayrozai parece ser o principal vetor de infecções em tatus hospedeiros. Contudo, este flebotomíneo não é altamente antropofílico, fato este que é provavelmente responsável por sua baixa taxa de infecção em humanos. Raras infecções foram registradas em Lu. (P.) paraensis e Lu. (P.) squamiventris, os quais são altamente antropofílicos e, portanto, provavelmente vetores deste parasita.
Hospedeiros mamíferos registrados
O único animal selvagem hospedeiro conhecido até o momento é o tatu-galinha Dasypus novemcinctus Sua infecção geralmente ocorre em sua pele e vísceras aparentemente normais.
Infecção em humanos
Leishmaniose cutânea, geralmente sob a forma de uma lesão única. Diferentemente da maioria das espécies neotropicais de Leishmania, L. (V.) naiffi raramente produz uma lesão visível na pele de hamsters de laboratório. Caso este parasita também produza infecções ocultas na pele de humanos, é possível que a sua transmissão para o homem seja muito mais frequente do que normalmente considerado.
LEISHMANIA (VIANNIA) SHAWI LAINSON ET AL, 1989
Distribuição geográfica conhecida
Diversas áreas da Amazônia Brasileira.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (N.) whitmani sensu lato. Há registros de diferenças morfométricas entre Lu. (N.) whitmani strictu sensu, encontrado no Estado da Bahia, Nordeste do Brasil, e o vetor de L. (V.) shawi encontrado no Estado do Pará, Amazônia Brasileira86. Essas diferenças, consideradas juntamente com a distinção entre as duas populações por meio de sondas de DNA87, sugerem que o vetor de L. (V.) shawi seria uma "espécie críptica" de um complexo Lu. (N.) whitmani. No entanto, esta teoria tem sido questionada com base na análise filogenética de haplótipos mitocondriais (citocromo b) de Lu. (N.) whitmani, que levou à conclusão de que existem clades de haplótipos e a interprocriação destes flebotomíneos nas florestas do Brasil31. Contudo, os comportamentos das espécies de flebotomíneos, no Estado da Bahia, e do Lu. (N.) whitmani s.l. , no Estado do Pará, são bem diferentes. Na Bahia, o inseto é altamente antropofílico, é normalmente encontrado em casas e é um vetor de L. (V.) braziliensis; em florestas primárias do Pará, no entanto, o flebotomíneo raramente pica humanos, não há registros de que entre em casas mesmo quando elas se encontram nas proximidades das florestas e é um vetor de L. (V.) shawi.
Hospedeiros mamíferos registrados
Os macacos Cebus apella e Chiropotes satanas (Cebidae), as preguiças Choloepus didactylus e Bradypus tridactylus (Xenarthra), o coati Nasua nasua (Procyonidae) e humanos.
Infecção em humanos
O parasita é responsável pela leishmaniose cutânea, normalmente do tipo que apresenta uma lesão única, porém são ocasionalmente observados casos de múltiplas lesões, certamente devido à ocorrência de metástase. Ainda não há relatos da ocorrência de leishmaniose mucocutânea causada pela L. (V.) shawi.
LEISHMANIA (VIANNIA) COLOMBIENSIS KREUTZER ET AL, 1991
Distribuição geográfica conhecida
Este parasita foi primeiramente documentado na Colômbia e no Panamá; posteriormente foi encontrado na Venezuela. Sua distribuição se estende provavelmente pelas florestas do Brasil e das planícies peruanas, bem como por outros países latino-americanos onde mamíferos e flebotomíneos reservatórios coexistem em ambiente selvagem.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (Helcocyrtomyia) hartmanni na Colômbia; Lu. (Lu.) gomezi e Lu. (Psychodopygus) panamensis no Panamá.
Hospedeiros mamíferos registrados
A preguiça Choloepus hoffmanni e humanos (Panamá).
Infecção em humanos
Lesões cutâneas únicas ou múltiplas. Não há registro de casos de doença mucocutânea causada por este parasita.
LEISHMANIA (VIANNIA) EQUATORENSIS GRIMALDI ET AL, 1992
Distribuição geográfica conhecida
Até o presente momento, este parasita parece estar limitado à costa equatoriana, no Oceano Pacífico.
Hospedeiros flebotomíneos conhecidos
Lutzomyia (N.) hartmanni.
Hospedeiros mamíferos registrados
A preguiça Choloepus hoffmanni e o esquilo Sciurus granatensis.
Infecção em humanos
Ainda não registrada.
LEISHMANIA (VIANNIA) LINDENBERGI SILVEIRA ET AL, 2002
Distribuição geográfica conhecida
Este parasita foi encontrado apenas em floresta secundária em Belém, Pará, Brasil.
Hospedeiros flebotomíneos conhecidos
Seu vetor é desconhecido atualmente, mas Lutzomyia (N.) antunesi é fortemente suspeito. Este inseto já demonstrou ser o flebotomíneo antropofílico predominante em uma área em que muitos soldados foram infectados com L. (V.) lindenbergi ao efetuar manobras militares na floresta. Além disso, o voo baixo do Lu. (N.) antunesi poderia explicar o porquê das lesões desses homens terem sido observadas em sua maioria nas faces e braços. Como os homens passavam a maior parte do tempo em trincheiras, aquelas partes do corpo seriam as mais expostas às picadas de um flebotomíneo em voo baixo. Uma espécie não identificada de Leishmania foi encontrada em espécimes de Lu. (N.) antunesi, na Ilha de Marajó, Pará90, porém o seu desenvolvimento no flebotomíneo foi suprapilariano. Em contraste, em flebotomíneos infectados experimentalmente, o desenvolvimento de L. lindenbergi é peripilariano, o que é típico de parasitas do subgênero Viannia.
Hospedeiros mamíferos registrados
Até o presente momento, os humanos são os seus únicos hospedeiros. Suspeita-se que os reservatórios animais selvagens sejam provavelmente terrestres.
Infecção em humanos
Lesões cutâneas localizadas: até o presente momento, nenhum caso de doença mucocutânea foi relatado.
LEISHMANIA (VIANNIA) UTINGENSIS BRAGA ET AL, 2003
Distribuição geográfica conhecida
Belém, Pará, Brasil.
Hospedeiros flebotomíneos conhecidos
Há um único registro de uma espécie do flebotomíneo Lutzomyia (Viannamyia) tuberculata coletado em extraído do tronco de uma grande árvore na floresta do Utinga, Belém, Pará, Brasil.
Hospedeiros mamíferos registrados
Atualmente desconhecidos.
Infecção em humanos
O parasita ainda não foi registrado em humanos.
"HYBRIDS" OF LEISHMANIA SPECIES WITHIN THE SUBGENUS VIANNIA
Estes "híbridos" incluem L. (V.) braziliensis / L. (V.) panamensis; L. (V.) braziliensis / L. (V.) guyanensis; e L. (V.) braziliensis / L. (V.) peruviana. Todos eles foram isolados apenas de casos de LCA humana. Apenas o último "híbrido" citado foi associado à leishmaniose mucocutânea. Foi sugerido que esses "híbridos" seriam resultantes de uma troca genética. Para maiores detalhes e referência, veja Lainson e Shaw47.
CONSIDERAÇÕES FINAIS
Fui informado pelo revisor deste artigo da descoberta da infecção natural do flebotomíneo Lutzomyia (Nyssomyia) neivae (Pinto, 1926) com Leishmania (V.) braziliensis no sul do Brasil82. Agradeço a ele pela inclusão deste dado no artigo.
A obtenção de provas irrefutáveis da participação de Lutzomyia cruzi na transmissão de Leishmania (L.) infantum chagasi, devido ao fato de as fêmeas deste flebotomíneo não poderem ser distinguidas das fêmeas de Lu. (Lu.) longipalpis, enfrentou tantas dificuldades quanto a busca pelo(s) vetor(es) de Leishmania (V.) braziliensis na Serra dos Carajás, Pará, Brasil. Neste caso, as duas espécies de flebotomíneos antropofílicos predominantes na área eram Lutzomyia (Psychodopygus) wellcomei e Lu. (P.) complexa, cujas fêmeas são também morfologicamente indistinguíveis. Descobriu-se que várias fêmeas foram infectadas por L. (V.) braziliensis, e o problema consistiu em decidir a qual espécie elas pertenciam. Este dilema foi finalmente elucidado pela criação de espécimes adultos a partir de ovos de fêmeas infectadas; esta estratégia forneceu os machos essenciais para a identificação, e demonstrou que os flebotomíneos infectados eram da espécie Lu. (P.) welcomef89. Este método poderia também ser utilizado para identificar espécimes infectados de Lu. cruzi / Lu. longipalpis no Estado do Mato Grosso do Sul.
Se considerarmos o impressionante número de espécies de Leishmania que foram registradas até o presente momento na região neotropical , e, particularmente, na região amazônica, esta área poderia muito bem ser tida como o local de origem deste gênero. Esta hipótese é corroborada pela observação de que muitos destes parasitas (espécies do subgênero Viannia) mantiveram o seu desenvolvimento no intestino posterior no hospedeiro flebotomíneo, o que seria remanescente do ciclo de vida de flagelados monóxenos de insetos dos quais as espécies de Leishmania teriam evoluído.
A existência de espécies de Leishmania conhecidas apenas em seu flebotomíneo hospedeiro (por exemplo, L. (V.) utingensis em Lutzomyia tuberculata) sugere a ocorrência de outras ainda não detectadas entre as várias espécies de flebotomíneos não antropofílicos. A busca continuada por estes parasitas e seus reservatórios mamíferos selvagens será fundamental para a geração de um quadro mais completo da ecologia deste fascinante grupo de parasitas.
AGRADECIMENTOS
O autor agradece ao Wellcome Trust, London, por seu apoio contínuo à Wellcome Parasitalogy Unit por cerca de 30 anos, e a todos os respectivos diretores do Instituto Evandro Chagas, Secretaria de Vigilância em Saúde, Ministério da Saúde, Brasil, onde este estudo foi executado. Não há espaço aqui para listar todos os participantes destas pesquisas ao longo de todo este período, porém alguns agradecimentos devem ser direcionados aos seguintes colaboradores: Prof. Jeffrey J. Shaw, velho amigo e colega, que trabalhou com o autor do dia da criação da WPU, em 1965, até o seu fechamento, em 1992; àqueles que foram pioneiros em técnicas moleculares, sorológicas e bioquímicas para a identificação de espécies de Leishmania e que deram condições para que o programa de Leishmaniose IEC/WPU fosse implementado, incluindo os Drs. M. L. Chance, P J. Gardener, Prof. M. A. Miles, Prof. D. C. Barker, Dr. Diane McMahon-Pratt e Dr. J. David; e às Dras. Marinete M. Póvoa, Roseli R. Braga e Edna A. Y. Ishikawa, que as utilizaram de forma extremamente competente; a nosso grupo de entomólogos, tão produtivos: Dr. Habib Fraiha, Prof. Richard Ward, Drs. Paul Ready, Adelson A. A. Souza, e Lee Ryan, e ao clínico e parasitologista Fernando T. Silveira, que, como chefe atual do Programa de Leishmaniose do IEC, tem usado sua longa experiência em campo e laboratório com membros anteriores da WPU para fazer com que este continue a dar frutos; finalmente, a todo o corpo técnico atual e passado, em particular a Maria das Graças S. da Silva, Sued Freitas Silva, Manoel C. de Souza, Roberto D. Naiff e Maricleide Naiff, Antonio Julio Monteiro, Deocleciano G. Primo, José Aprígio N. de Lima, João B. P. da Luz, António F. P. Martins, Nonato B. Pires, lorlando da Rocha Barata e João A. Brandão.
REFERÊNCIAS
1 Barrai A, Badaró R, Barral-Netto M, Grimaldi Jr G, Momen H, Carvalho EM. Isolation of Leishmania mexicana amazonensis from the bone marrow in a case of American visceral leishmaniasis. Am J Trop Med Hyg. 1986 Jul;35(4):732-4. [ Links ]
2 Belli A, Garcia D, Palacios X, Rodriguez B, Valle S, Videa E, et al. Widespread atypical cutaneous leishmaniasis caused by Leishmania (L.) chagasi in Nicaragua. Am J Trop Med Hyg. 1999 Sep;61(3): 380-5. [ Links ]
3 Biagi FF. Algunos comentarios sobra las leishmaniasis y sus agentes etiológicos, Leishmania tropica mexicana, nueva subspecie. Medicina, Mexico. 1953;33:401-6.
4 Braga RR, Lainson R, Ishikawa EAY, Shaw JJ. Leishmania utingensis n.sp., a parasite from the sand fly Lutzomyia (Viannamyia) tuberculata in Amazonian Brazil. Parasite. 2003;10:111-8.
5 Brandão Filho SP, Brito ME, Carvalho FG, Ishikawa EA, Cupolillo E, Floeter-Winter L, et al. Wild and synanthropic hosts of Leishmania (Viannia) braziliensis in the endemic cutaneous leishmaniasis locality of Amaraji, Pernambuco State, Brazil. Trans R Soc Trop Med Hyg. 2003 May-Jun;97(3):291-6.
6 Carini A, Paranhos U. Identification de l'ulcera de Baurú avec le bouton d'Orient. Bull Soc Path Exot. 1909;2:225-6.
7 Christensen HA, Herrer A, Telford SR. Enzootic cutaneous leishmaniasis in eastern Panama. II. Entomological investigations. Ann Trop Med Parasitol. 1972 Mar;66(1):55-66.
8 Christensen HA, Herrer A, Telford SR. Leishmania braziliensis from Lutzomyia panamensis in Panama. J Parasitol. 1969;55:1090-1.
9 Convit J, Lapenta P. Sobre un caso de leishmaniose tegumentaria de forma diseminada. Rev Policlin Caracas. 1946;18:153-8.
10 Corredor A, Gallego JF, Tesh RB, Morales A, Carrasquilla CF, Young DG, et al. Didelphis marsupialis, an apparent wild reservoir of Leishmania donovani chagasi in Colombia, South America. Am J Trop Med Hyg. 1989;40(5):480-6.
11 Cox FE. Classification and introduction to the parasitic protozoa. In: Cox FE, Wakelin D, Gillespie SH, Despommier DD, editors. Topley & Wilson's Microbiology and Microbial Infections, Parasitology. 10th ed. London: Hodder Arnold Press; 2005. p.186-99.
12 Cunha AM, Chagas E. Nova espécie de protozoário do género Leishmania pathogenico para o homem. Leishmania chagasi n.sp. Nota Prévia. O Hospital, Rio de Janeiro. 1937;11:3-9.
13 Dahroug MA, Almeida AB, Sousa VR, Dutra V, Turbino NC, Nakazato L, et al. Leishmania (Leishmania) chagasi in captive wild felids in Brazil. Trans R Soc Trop Med Hyg. 2010 Jan;104(1):73-4. [ Links ]
14 Deane LM, Grimaldi G. Leishmaniasis in Brazil. In: Chang KP, Bray RS, editors. Leishmaniasis. New York: Elsevier; 1985. p. 247-75.
15 Decker-Jackson JE, Schrot JR, Levin GV. Identification of Leishmania spp by radiorespirometry. J Protozool.1977;24(3):463-70. [ Links ]
16 Decker-Jackson JE, Tang DB. Identification of Leishmania spp by radiorespirometry. II. A statistical method of data analysis to evaluate the reproductibility and sensitivity of the technique. In: Chance ML, Walton BC, editors. Biochemical Characterization of Leishmania. Proccedings of a Workshop Pan Am Health Organization; 1980 Dec 19; Washington (DC): Switzerland.UNDP/World Bank/WHO Special Programme for Research. Training in Tropical Diseases; 1980. p. 205-45.
17 Feliciangeli MD, Rodriguez N, De Guglielmo Z, Rodriguez A. The re-emergence of American visceral leishmaniasis in an old focus in Venezuela. II. Vectors and parasites. Parasite. 1999 Jun;6(2):113-20.
18 Figueiredo FB, Gremião ID, Pereira SA, Fedulo LP, Menezes RC, Balthazar DA, et al. First report of natural infection of a bush dog (Speothos venaticus) with Leishmania (Leishmania) chagasi in Brazil. Trans R Soc Trop Med Hyg. 2008 Feb; 102(2):200-1. [ Links ]
19 Floch H. Leishmania tropica guyanensis n.sp. agent de la leishmaniose tégumentaire des Guyanes et l'Amérique Centrale. Arch Inst Pasteur Guyane Franc Terit Inini. 1954;328:1-4.
20 Forattini OP. Sobre os reservatórios naturais da leishmaniose tegumentar americana. Rev Inst Med Trop Sao Paulo. 1960;2:195-203. [ Links ]
21 Forattini OP, Pattoli DB, Rabello EX, Ferreira OA. Infecções naturais de mamíferos silvestres em área endémica de leishmaniose tegumentar do Estado de São Paulo, Brasil. Rev Saude Publica. 1972;6(3):255-61. [ Links ]
22 Forattini OP, Pattoli DB, Rabello EX, Ferreira OA. Nota sobre infecção natural de Oryzomys capito laticeps em foco enzoótico de leishmaniose tegumentar no Estado de São Paulo, Brasil. Rev Saude Publica.1973;7:181-4.
23 Garnham PCC. Cutaneous leishmaniasis in the New World, with special reference to Leishmania mexicana. Sci Rep Inst Sup Sanit. 1962;2:76-82.
24 Gentile BF, Le Pont F, Pajot FX, Besnard R. Dermal leishmaniasis in French Guiana: the sloth (Choloepus didactylus) as a reservoir host. Trans R Soc Trop Med Hyg. 1981;75(4):612-3. [ Links ]
25 Gil LH, Basano SA, Souza AA, Silva MG, Barata I, Ishikawa EA, et al. Recent observations on the sand fly (Diptera: Psychodidae) fauna of the State of Rondônia, western Amazónia, Brazil: the importance of Psychodopygus davisi as a vector of zoonotic cutaneous leishmaniasis. Mem Inst Oswaldo Cruz. 2003 Sep;98(6):751-5. [ Links ]
26 Grimaldi G, Kreutzer RD, Hashiguchi Y, Gomez EA, Mimory T, Tesh RB. Description of Leishmania equatorensis sp.n (Kinetoplastida: Trypanosomatidae), a new parasite infecting arboreal mammals in Ecuador. Mem Inst Oswaldo Cruz. 1992;87(2):221-8. [ Links ]
27 Herrer A. Leishmania hertigi sp.n., from the tropical porcupine, Coendou rothschildi Thomas. J Parasitol. 1971 Jun;57(3):626-9. [ Links ]
28 Herrer A. Lutzomyia peruensis (Shannon, 1929), posible vector natural de la uta (leishmaniose tegumentaria). Rev Inst Trop Sao Paulo. 1982;24:168-72.
29 Herrer A, Christensen HA, Beumer RJ. Reservoir hosts of cutaneous leishmaniasis among Panamanian forest mammals. Am J Trop Med Hyg. 1973 Sep;22(5):585-91. [ Links ]
30 Herrer A, Telford SR, Christensen HA. Enzootic cutaneous leishmaniasis in eastern Panama. I. Investigation of the infection among forest mammals. Ann Trop Med Parasitol. 1971 Sep;65(3):349-58. [ Links ]
31 Ishikawa EA, Ready PD, Souza AA, Day JC, Rangel EF, Davies CR, et al. A mitochondrial DNA phylogeny indicates close relationships between populations of Lutzomyia whitmani (Diptera: Psychodidae: Phlebotominae) from the rain-forest regions of Amazonia and northeast Brazil. Mem Inst Oswaldo Cruz. 1999 May-Jun;94(3):339-45. [ Links ]
32 Jackson PD, Stiteler JM, Wohlhieter JA, Reed SG, Badaro R, Inverso J, et al. Characterization of Leishmania responsible for visceral disease in Brazil by restriction endonuclease digestion and hybridization of kinetoplastic DNA. In: 11th International Congress of Tropical Medicine and Malaria; 2004 Sep 16-22; Calgary, Canada. 1984. p. 68.
33 Jackson PD, Wohlhieter JA, Hockmeyer WT. Leishmania characterization by restriction endonuclease digestion of kinetoplastic DNA [abstracts]. In: 5th International Congress of Parasitology; 1982 Aug 7-14; Toronto, Canada, 1982. p. 342.
34 Johnson PT, McConnell E, Hertig M. Natural infections of leptomonad flagellates in Panamanian phlebotomus sandflies. Exp Parasitol. 1963 Aug;14:107-22. [ Links ]
35 Killick-Kendrick R, Lainson R, Rioux J-A, Saf'janova VM. The taxonomy of Leishmania-like parasites of reptiles. In: Rioux J-A, editor. Leishmania, Taxonomie et phylogenese: applications eco-epidemiologiques. Colloque International CNRS/INSERM; 1984 Jul 2-6; Montpellier, Montpellie:IMEE 1984; France. p. 143-148.
36 Kreutzer RD, Corredor A, Grimaldi Jr G, Grogl M, Rowton ED, Young DG, et al. Characterization of Leishmania colombiensis (Kinetoplastida:Trypanosomatidae), a new parasite infecting humans, animals and phlebotomine sand flies in Colombia and Panama. Am J Trop Med Hyg. 1991 Jun;44(6):662-75. [ Links ]
37 Lainson R. Demographic changes and their influence on the epidemiology of the American leishmaniases. In: Service MW, editors. Demography and Vector-Borne Diseases. Florida: CRC Press Inc; 1989. p. 85-106.
38 Lainson R, Braga RR, Souza AA, Povoa MM, Ishikawa EA, Silveira FT. Leishmania (Viannia) shawi sp.n., a parasite of monkeys, sloths and procyonids in Amazonian Brazil. Ann Parasitol Hum Comp. 1989;64(3):200-7. [ Links ]
39 Lainson R, Rangel EF. Ecologia das leishmanioses: Lutzomyia longipalpis e a eco-epidemiologia da leishmaniose visceral americana (LVA) no Brasil. In: Rangel EF, Lainson R, editors. Flebotomineos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 311-36. [ Links ]
40 Lainson R, Ready PD, Shaw JJ. Leishmania in phlebotomid sandflies. VII. On the taxonomic status of Leishmania peruviana, causative agent of Peruvian 'uta', as indicated by its development in the sandfly, Lutzomyia longipalpis. Proc R Soc Lond B Biol Sci. 1979 Dec;206(1164):307-18. [ Links ]
41 Lainson R, Shaw JJ. Evolution, classification and geographical distribution. In: Peters W, Killick-Kendrick R, editors. The leishmaniases in biology and medicine. London: Academic Press; 1987. p. 12-120. [ Links ]
42 Lainson R, Shaw JJ. Leishmanias and leishmaniasis of the New World, with particular reference to Brazil. Bull Pan Am Health Org. 1973;7(4):1-19.
43 Lainson R, Shaw JJ. Leishmanias of neotropical porcupines: Leishmania hertigi deanei nov. subsp. Acta Amaz. 1977;7(1):51-7.
44 Lainson R, Shaw JJ. Leishmaniasis in Brazil. I. Observations on enzootic rodent leishmaniasis-incrimination of Lutzomyia flaviscutellata (Mangabeira) as the vector in the lower Amazonian basin. Trans R Soc Trop Med Hyg. 1968;62(3):385-95. [ Links ]
45 Lainson R, Shaw JJ. Leishmaniasis in Brazil. V. Studies on the epidemiology of cutaneous leishmaniasis in Mato Grosso State, and observations on two distinct strains of Leishmania isolated form man and forest animals. Trans R Soc Trop Med Hyg. 1970;64(5):654-67. [ Links ]
46 Lainson R, Shaw JJ. Leishmaniasis of the New World: taxonomic problems. Brit Med Bull. 1972 Jan;28(1):44-8. [ Links ]
47 Lainson R, Shaw JJ. New World Leishmaniasis. In: Cox FEG, Wakelin D, Gillespie SH, Despommier DD, editors. Topley & Wilson's Microbiology and Microbial Infections: parasitology. 10th ed. London: Hodder Arnold ASM Press; 2005. p. 313-49. [ Links ]
48 Lainson R, Shaw JJ. New World leishmaniasis - the Neotropical Leishmania species. In: Cox FE, Kreier JP, Wakelin D, editors. Topley & Wilson's Microbiology and Microbial Infections. 9th ed. London: Hodder Headline Group; 1998. p. 241-66. [ Links ]
49 Lainson R, Shaw JJ. Some reservoir-hosts of Leishmania in wild animals of Mato Grosso State, Brazil. Two distinct strains of parasites isolated from man and rodents. Trans R Soc Trop Med Hyg. 1969;63(3):408-9. [ Links ]
50 Lainson R, Shaw JJ. Taxonomy of the New World Leishmania species. Trans R Soc Trop Med Hyg. 1972;66(6):943-4.
51 Lainson R, Shaw JJ. The role of animals in the epidemiology of South American leishmaniasis. In: Lumsden WHR, Evans DA, editors. Biology of the Kinetoplastida. London: Academic Press; 1979. p. 1-116. [ Links ]
52 Lainson R, Shaw JJ, Lins ZC. Leishmaniasis in Brazil: IV The fox, Cerdocyon thous (L) as a reservoir of Leishmania donovani in Para State, Brazil. Trans R Soc Trop Med Hyg. 1969;63(6):741-5. [ Links ]
53 Lainson R, Shaw JJ, Póvoa M. The importance of edentates (sloths and anteaters) as primary reservoirs of Leishmania braziliensis guyanensis, causative agent of "pian-bois" in North Brazil. Trans R Soc Trop Med Hyg. 1981;75(4):611-2.
54 Lainson R, Shaw JJ, Silveira FT, Braga RR. American visceral leishmaniasis: on the origin of Leishmania (Leishmania) chagasi. Trans R Soc Trop Med Hyg. 1987;81(3):517.
55 Lainson R, Shaw JJ, Ward RD, Fraiha H. Leishmaniasis in Brazil. IX. Considerations on the Leishmania braziliensis complex: importance of sandflies of the genus Psychodopygus (Mangabeira) in the transmission of L. braziliensis in north Brazil. Trans R Soc Trop Med Hyg. 1973;67(2):184-96. [ Links ]
56 Lainson R, Strangways-Dixon J. Dermal leishmaniasis in British Honduras: some host-reservoirs of Leishmania braziliensis mexicana. A preliminary note. Brit Med J. 1962;1:1596-8. [ Links ]
57 Lainson R, Strangways-Dixon J. The epidemiology of dermal leishmaniasis in British Honduras. Part II. Reservoir-hosts of Leishmania mexicana among the forest rodents. Trans R Soc Trop Med Hyg. 1964;58:136-53. [ Links ]
58 Lainson R, Ward RD, Shaw JJ. Leishmania in phlebotomid sandflies: VI. Importance of hindgut development in distinguishing between parasites of the Leishmania mexicana and L. braziliensis complexes. Proc R Soc Lond B Biol Sci. 1977;199:309-20. [ Links ]
59 Lima H, de Gugielmo Z, Rodríguez A, Convit J, Rodriguez N. Cotton rats (Sigmodon hispidus) and black rats (Rattus rattus) as possible reservoirs of Leishmania spp. in Lara State, Venezuela. Mem Inst Oswaldo Cruz. 2002 Mar;97(2):169-74. [ Links ]
60 Lindenberg A. L'ulcere de Bauru ou le bouton d'orient au Brésil. Bull Soc Path Exot. 1909;2:252-4.
61 Llanos-Cuentas EA, Roncal N, Villaseca P, Paz L, Ogusuku E, Perez JE, et al. Natural infections of Leishmania peruviana in animals in the Peruvian Andes. Trans R Soc Trop Med Hyg. 1999 Jan-Feb;93(1):15-20. [ Links ]
62 Lühe M. Die im Blute schmarotzenden Protozoen und ihre nachsten Verwandren. In: Mense C, Barth IA, editors. Hanbuch der Tropenkrankheiten; 1906. p.203.
63 Lukes J, Maurico IL, Schönian G, Dujardin JC, Soteriadon K, Dedet J-P, et al. Evolutionary and geographical history of the Leishmania donovani complex, with a revision of current taxonomy. Proc Natl Acad Sci USA. 2007 May;104(22):9375-80. [ Links ]
64 Luz E, Giovannoni M, Borba AM. Infecção de Lutzomyia monticola por Leishmania enriettii. Ann Fac Med Univers Fed Parana. 1967;9-10:121-B.
65 Machado MI, Milder RV, Pacheco RS, Silva M, Braga RR, Lainson R. Naturally acquired infections with Leishmania enriettii Muniz and Medina 194B in guinea-pigs from São Paulo, Brazil. Parasitology. 1994;109(Pt2):135-8.
66 Márquez M, Scorza JV. Criterios de nuliparidad y de paridad en Lutzomyia townsendi (Ortiz, 1959) del occidente de Venezuela. Mem Inst Oswaldo Cruz 1982;77(3):229-46. [ Links ]
67 Martinez E, Le Pont F, Mollinedo S, Cupolillo E. A first case of cutaneous leishmaniasis due to Leishmania (Viannia) lainsoni in Bolivia. Trans R Soc Trop Med Hyg 2001 Jul;95(4):375-7. [ Links ]
68 Martinez E, Le Pont F, Torrez M, Telleria J, Vargas F, Dujardin JC, et al. Lutzomyia nuneztovari anglesi (Le Pont and Desjeux, 19B4) as a vector of Leishmania amazonensis in a sub-Andean leishmaniasis focus of Bolivia. Am J Trop Med Hyg. 1999 Nov;61(5): B46-9.
69 Matta AA. Sur les leishmanioses tégumentaires. Classification générale des leishmanioses. Bull Soc Path Exot. 1916;9:494-503.
70 McMahon-Pratt D, Bennett E, David JR. Monoclonal antibodies that distingu ish su bspecies of Leishmania braziliensis. Am J Immunol. 1982 Sep;129(3):926-7. [ Links ]
71 Medina HSG. Estudos sôbre leishmaniose. I. Primeiros casos de leishmaniose espontânea observados em cobaios. Arq Bioi Tec. 1946;1:39-74. [ Links ]
72 Medina R, Romero J. Estudio clínico y parasitológico de una nueva cepa de leishmania. Arch Venez Med Trop Parasitol Med. 1959 Jul;3:298-326.
73 Medina R, Romero J. Leishmania pifanoi n.sp. El agente causal de la leishmaniasis tegumentaria difusa. Arch Venez Pat Trop Parasitol Med. 1962;4:349-53.
74 Migone LE. Un caso de kala-azar a Asunción (Paraguay). Bull Soc Path Exot. 1913;6:118-20.
75 Miles MA, Lainson R, Shaw JJ, Póvoa M, Souza AA. Leishmaniasis in Brazil: XV. Biochemical distinction of Leishmania mexicana amazonensis, L. braziliensis braziliensis and L. braziliensis guyanensis - aetiological agents of cutaneous leishmaniasis in the Amazon Basin of Brazil. Trans R Soc Trop Med Hyg. 1981;75(4):524-9. [ Links ]
76 Miies MA, Póvoa MM, Souza AA, Lainson R, Shaw JJ. Some methods for the enzymic characterization of Latin-American Leishmania with particular reference to Leishmania mexicana amazonensis and subspecies of Leishmania hertigi. Trans R Soc Trop Med Hyg. 1980;74(2):243-52. [ Links ]
77 Nery-Guimarães F, Costa O. Observações sôbre o comportamento da "Leishmania" produtora de infecção natural em "Oryzomys goeldi" na Amazônia. (Segunda nota). O Hospital, Rio de Janeiro. 1964;66:287-92.
78 Noyes HA. Implications of a Neotropical origin of the genus Leishmania. Mem Inst Oswaldo Cruz. 1998 Sep;93(5):657-62. [ Links ]
79 Noyes HA, Arana BA, Chance ML, Maignon R. The Leishmania hertigi (Kinetoplastida; Trypanosomatidae) complex and the lizard Leishmania: their classification and evidence for a neotropical origin of the Leishmania-Endotrypanum clade. J Eukaryot Microbiol. 1997 Sep-Oct;44(5):511-7. [ Links ]
80 Penna HA. Leishmaniose visceral no Brasil. Brasil Med. 1934;48:949-50.
81 Pessôa SB. Classificação das leishmanioses e das espécies do gênero Leishmania. Arq Hig Saude Pub. 1961;26:41-50.
82 Pita-Pereira D, Souza GD, Zwetsch A, Alves CR, Britto C, Rangel EF. First report of Lutzomyia (Nyssomyia) neivai (Diptera: Psychodidae: Phlebotominae) naturally infected by Leishmania (Viannia) braziliensis in a periurban area of South Brazil using a multiplex polymerase chain reaction assay. Am J Trop Med Hyg. 2009 Apr;80(4):593-5. [ Links ]
83 Pizarro P. Relación de la conquista del Perú. Colección de libros y documentos referentes a la historia del Perú. Lima: Collection Urteaga-Romero; 1571. (1st Series) [ Links ]
84 Ponce C, Ponce E, Morrison A, Cruz A, Kreutzer R, McMahon-Pratt D, et al. Leishmania donovani chagasi: a new clinical variant of cutaneous leishmaniasis in Honduras. Lancet. 1991 Jan;337(8733):67-70. [ Links ]
85 Rangel EF, Lainson R. Proven and putative vectors of American cutaneous leishmaniasis in Brazil: aspects of their biology and vectorial competence. Mem Inst Oswaldo Cruz. 2009 Nov;104(7):937-54. [ Links ]
86 Rangel EF, Lainson R, Souza AA, Ready P, Azevedo ACR. Variation between geographical populations of Lutzomyia (Nyssomyia) whitmani (Antunes & Coutinho, 1939) sensu lato (Diptera: Psychodidae: Phlebotominae) in Brazil. Mem Inst Oswaldo Cruz. 1996 Jan-Feb;91(1):43-50. [ Links ]
87 Ready PD, Day JC, Souza AA, Rangel EF, Davies CR. Mitochondrial DNA characterization of populations of Lutzomyia whitmani (Diptera: Psychodidae) incriminated in the peri-domestic and silvatic transmission of Leishmania species in Brazil. Bull Entomol Res. 1997 Apr;87(2):187-95. [ Links ]
88 Rocha NM, Melo MN, Babá EH, Dias M, Michalick MS, Costa CA, et al. Leishmania braziliensis braziliensis isolated from Akodon arviculoides captured in Caratinga, Minas Gerais, Brazil. Trans R Soc Trop Med Hyg. 1988 Jan;82(1):68. [ Links ]
89 Ryan L, Lainson R, Shaw JJ. Leishmaniasis in Brazil. XXIV. Natural flagellate infections of sandflies (Diptera: Psychodidae) in Pará State, with particular reference to the rôle of Psychodopygus wellcomei as the vector of Leishmania braziliensis braziliensis in the Serra dos Carajás. Trans R Soc Trop Med Hyg. 1987 May-Jun;81(3):353-9. [ Links ]
90 Ryan L, Silveira FT, Lainson R, Shaw JJ. Leishmanial infections in Lutzomyia longipalpis and Lu. antunesi (Diptera: Psychodidae) on the island of Marajó, Pará State, Brazil. Trans R Soc Trop Med Hyg. 1984;78(4):547-8. [ Links ]
91 Saf'janova VM. Classification of the genus Leishmania Ross. In: The Leishmanias, Protozoology. Leningrad: Academy of Sciences; All Union Society of Protozoologists; 1982. p. 95-101.
92 Santoro F, Lemesre JL, Rizvi FS, Afchain D, Sadogirsky M. Spécificité au niveau de proteins de surface des promastigotas de Leishmania donovani (Laveran et Mesnil, 1903), Leishmania infantum Nicolle, 1908 et Leishmania chagasi Cunha et Chagas, 1937. In: Rioux JA, editor. Leishmania. Taxonomie et Phylogenese. Applications Éco-Épidémiologiques. Colloque Internat; 1984 July 2-6; Montpellier: L'Institut Méditerranéen d'Études Épidémiologiques et Écologiques; 1986. p. 71-6.
93 Santos SO, Arias J, Ribeiro AA, Paiva Hoffmann M, Freitas RA, Malacco MA. Incrimination of Lutzomyia cruzi as a vector of American visceral leishmaniasis. Med Vet Entomol. 1998 Jul;12(3):315-7. [ Links ]
94 Santos SO, Arias JR, Hoffmann MP, Fulan MB, Ferreira WF, Pereira C, et al. The presence of Lutzomyia longipalpis in a focus of American visceral leishmaniasis where the only proven vector is Lutzomyia cruzi, Corumbá. Mato Grosso do Sul State. Rev Soc Bras Med Trop. 2003 Sep-Oct;36(5):633-4. [ Links ]
95 Shaw JJ. New World leishmaniasis: the ecology of leishmaniasis and the diversity of leishmanial species in Central and South America. In: J Farrell, editors. World Class Parasites: Leishmania. London: Kluwer Academic Publishers Boston; 2002. p. 11-31.
96 Shaw JJ, Lainson R. Leishmaniasis in Brazil: II. Observations on enzootic rodent leishmaniasis in the lower Amazon Region the feeding habits of the vector, Lutzomyia flaviscutellata in reference to man, rodents and other animals. Trans R Soc Trop Med Hyg. 1968;62(3):396-405. [ Links ]
97 Shaw JJ, Lainson R, Ryan L, Braga RR, McMahon-Pratt D, David JR. Leishmaniasis in Brazil: XXIII. The identification of Leishmania braziliensis braziliensis in wild-caught neotropical sandflies using monoclonal antibodies. Trans R Soc Trop Med Hyg. 1987;81(1):69-72. [ Links ]
98 Sherlock IA, Miranda JC, Sadigursky M, Grimaldi G. Natural infection of the opossum Didelphis albiventris (Marsupialia, Didelphidae) with Leishmania donovani in Brazil. Mem Inst Oswaldo Cruz. 1984 Oct-Dec;79(4):511. [ Links ]
99 Silveira FT, Ishikawa EA, Souza AA, Lainson R. An outbreak of cutaneous leishmaniasis among soldiers in Belém, Pará State, Brazil, caused by Leishmania (Viannia) lindenbergi n.sp. A new leishmanial parasite of man in the Amazon Region. Parasite. 2002 Mar;9(1):43-50. [ Links ]
100 Silveira FT, Lainson R, Corbett CEP. Clinical and immunopathological spectrum of American cutaneous leishmaniasis with special reference to the disease in Amazonian Brazil a review. Mem Inst Oswaldo Cruz. 2004 May;99(3):239-51. [ Links ]
101 Silveira FT, Lainson R, Shaw JJ, Braga RR, Ishikawa EAY, Souza AAA. Leishmaniose cutânea na Amazônia: isolamento de Leishmania (Viannia) lainsoni do roedor Agouti paca (Rodentia: Dasyproctidae) no Estado do Pará, Brasil. Rev Inst Med Trop Sao Paulo. 1991 Jan-Feb;33(1):18-22. [ Links ]
102 Silveira FT, Souza AAA, Lainson R, Shaw JJ, Braga RR, Ishikawa EAY. Cutaneous leishmaniasis in the Amazon Region: natural infection of the sandfly Lutzomyia ubiquitalis (Psychodidae: Phlebotominidae) by Leishmania lainsoni in Pará State, Brazil. Mem Inst Oswaldo Cruz. 1991 Jan-Mar;86(1):127-30.
103 Souza A, Ishikawa E, Braga R, Silveira F, Lainson R, Shaw JJ. Psychodopygus complexus, a new vector of Leishmania braziliensis to humans in Pará State, Brazil. Trans R Soc Trop Med Hyg. 1996 Mar-Apr;90(2):112-3. [ Links ]
104 Souza AAA, Silveira FT, Lainson R, Barata IR, Silva MGS, Lima JAN, et al. Fauna flebotomínica da Serra dos Carajás, Estado do Pará, Brasil, e sua possível implicação na transmissão da leishmaniose tegumentar americana. Rev Pan-Amaz Saude. 2010;1(1):45-51. [ Links ]
105 Splendore A. Buba-blastomicosi-leishmanosi. Nota sopra alcune affezioni framboesiche osservate in Brasile. Arch für Schiffs-und Tropenhyg. 1911;15:105-15.
106 The thirtieth annual report of the work and operation of the Gorgas Memorial Laboratory, covering the fiscal year ended; 1957 June 30. Washington: United States Government Printing Office; 1957.
107 The twenty-ninth annual report of the work and operation of the Gorgas Memorial Laboratory, covering the fiscal year ended; 1956 June 30. Washington: United States Government Printing Office; 1957.
108 Travi BL, Jaramillo C, Montoya J, Segura I, Zea A, Gonçalves A, et al. Didelphis marsupialis, an important reservoir of Trypanosoma (Schizotrypanum) cruzi and Leishmania (Leishmania) chagasi in Colombia. Am J Trop Med Hyg. 1994 May;50(5):557-65. [ Links ]
109 Travi BL, Vélez ID, Brutus L, Segura I, Jaramillo C, Montoya J. Lutzomyia evansi, an alternative vector of Leishmania chagasi in a Colombian focus of visceral leishmaniasis. Trans R Soc Trop Med Hyg. 1990 Sep-Oct;84(5):676-7. [ Links ]
110 Velez IR. Uta et espundia. Bull Soc Path Exot. 1913;6:545.
111 Vianna G. Sobre uma nova especie de Leishmania (Nota Preliminar). Bras Med. 1911;25:411.
112 Ward RD, Lainson R, Shaw JJ. Experimental transmissions of Leishmania mexicana amazonensis Lainson & Shaw, between hamsters by the bite of Lutzomyia flaviscutellata (Mangabeira). Trans R Soc Trop Med Hyg. 1977;71(3):265-6.
113 Ward RD, Lainson R, Shaw JJ. Further evidence of the rôle of Lutzomyia flaviscutellata (Mangabeira) as the vector of Leishmania mexicana amazonensis in Brazil. Trans R Soc Trop Med Hyg. 1973;67(4):608-9. [ Links ]
114 Ward RD, Shaw JJ, Lainson R, Fraiha H. Leishmaniasis in Brazil: VIII. Observations on the phlebotomine fauna of an area highly endemic for cutaneous leishmaniasis, in the Serra dos Carajas, Pará State. Trans R Soc Trop Med Hyg. 1973;67(2):174-83. [ Links ]
115 Wright JH. Protozoa in a case of tropical ulcer ("Delhi sore"). J Med Res. 1903 Dec;10(3):472-82. [ Links ]
116 Zeledón R, Hidalgo H, Viquez A, Urbina A. Atypical cutaneous leishmaniasis in a semi-arid region of north-west Costa Rica. Trans R Soc Trop Med Hyg. 1989 Nov-Dec;83(6):786. [ Links ]
117 Zuckerman A, Lainson R. Leishmania. In: Kreier JP, editor. Parasitic protozoa. London: Academic Press; 1977. p. 57-133. [ Links ]
 Correspondência / Correspondence
/ Correspondencia:
Correspondência / Correspondence
/ Correspondencia:
Instituto Evandro Chagas
Seção de Parasitologia
Av. Almirante Barroso, 492
CEP: 66090-000
Belém-Pará-Brasil
E-mail: ralphlainson@iec.pa.gov.br
Recebido em / Received / Recibido en: 16/4/2010
Aceito em / Accepted / Aceito en: 28/5/2010











 texto em
texto em 

