Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.1 n.2 Ananindeua jun. 2010
http://dx.doi.org/10.5123/S2176-62232010000200013
Prevalencia de infección por los virus de las hepatitis A, B, C y D en la demanda de un hospital en el Municipio de Juruti, oeste del Estado de Pará, Brasil
Heloisa Marceliano Nunes; Manoel do Carmo Pereira Soares; Elisabete Maria de Figueiredo Brito; Max Moreira Alves; Olglaize do Socorro da Costa Souza; Ana Maria Borges; Ivanilda Silva da Silva; José Fábio da Paixão
Seção de Hepatologia, Instituto Evandro Chagas/SVS/MS, Belém, Pará, Brasil
Endereço para
correspondência
Correspondence
Dirección para correspondencia
Título original: Prevalência de infecção pelos vírus das hepatites A, B, C e D na demanda de um hospital no Município de Juruti, oeste do Estado do Pará, Brasil. Traducido por: Lota Moncada
RESUMEN
El Municipio de Juruti localizado a oeste del Estado de Pará posee una importante reserva de bauxita, cuya explotación se inició en 2005. El surgimiento o aumento de la frecuencia de enfermedades influenciadas por esa explotación, particularmente en relación a las Hepatitis virales, es diversa de la observada en cualquier otra región del mundo. Para definir la prevalencia de las infecciones por los virus de las hepatitis A, B, C y D en la demanda del hospital municipal de Juruti, entre febrero de 2007 y abril de 2008, se colectaron muestras de suero de personas de la demanda hospitalaria, y fueron sometidas al análisis de los marcadores serológicos de las hepatitis A (VHA), B (VHB), C (VHC) y D (VHD), por técnicas inmunoenzimáticas. En las muestras positivas para los virus B y C se realizaron investigaciones para la detección del VHB-DNA y del VHC-RNA, por PCR y RT-PCR, respectivamente. Entre las 1.630 muestras colectadas, hubo prevalencia de un 85,6% para el anti-VHA total; de 0,7% para el HBsAg; 9,1% anti-HBc/anti-HBs y 31,4% anti-HBs aislado. Entre los HBsAg+, 9,1% eran HBeAg+; 63,6% anti-HBe+ y 72,7% VHB-DNA+. El anti-VHC fue positivo en 0,1% y no se detectó serología positiva para VHD. Caracterizamos con base en laboratorio, alta prevalencia de infección por VHA, detección de portadores crónicos y de susceptibles para VHB, presencia de portador de VHC y la ausencia de portadores de VHD. Se recomienda la realización de estudios epidemiológicos locales, basados en comunidades, para comparar con los datos hospitalarios ahora presentados.
Palabras clave: Hepatitis A; Hepatitis B; Hepatitis C; Hepatitis D; Prevalencia.
INTRODUCCIÓN
Las hepatitis virales son enfermedades infecciosas que tienen en común el hepatotropismo viral primario y constituyen un importante problema de salud pública en todo el mundo15. Cinco virus son reconocidos como agentes etiológicos de las diferentes hepatitis virales humanas: los virus de las hepatitis A (VHA), B (VHB), C (VHC), D o Delta (VHD) y E (VHE). La mayoría de las hepatitis virales agudas son asintomáticas, presentando una evolución generalmente benigna, evolucionando hacia la cura, en la mayoría de los casos. Sin embargo, dependiendo del agente involucrado y las características inmunogenéticas del hospedero, pueden progresar hacia la cronicidad, o aún, de modo menos común, hacia la forma fulminante.
La hepatitis A presenta distribución mundial, la principal vía de contagio es la fecal-oral por vehiculación hídrica y de alimentos contaminados, contribuyendo para eso, la estabilidad del VHA en el medio ambiente y la gran cantidad del virus presente en las heces de los individuos infectados. El contacto entre familiares, la falta de hábitos de higiene, la manipulación de alimentos por personas infectadas, propician la diseminación del virus. En las áreas de elevada endemicidad, la infección alcanza con más frecuencia a niños y a adolescentes, en su mayoría asintomática o con una sintomatología ligera, caracterizándose como la hepatitis viral aguda más frecuente en el mundo9,15.
Las infecciones por el virus de la hepatitis B se mantienen como un serio problema de salud pública en todo el mundo, siendo este agente, importante determinante de formas graves de enfermedad aguda o crónica del hígado. Según la Organización Mundial de Salud aproximadamente 2 mil millones de personas ya han sido infectadas por el VHB, en todo el mundo, existiendo aproximadamente 325 millones de portadores crónicos, con 1 a 2 millones de óbitos por año18,20. El virus se transmite de forma horizontal, acometiendo a niños mayores de 5 años de edad y a adultos - por las vías sexual, parenteral y cutáneo-mucosa - y de forma vertical, de madre a hijo, abarcando a niños en el período perinatal hasta los 5 años de edad. El estándar epidemiológico de prevalencia de la infección crónica por el VHB de una región, tiende a ser definido por la prevalencia de los marcadores serológicos HBsAg, anti-HBc y anti-HBs, siendo consideradas áreas de alta endemicidad, aquellas con prevalencia de infección crónica superior a los 8% o superior al 60% de la población con evidencia serológica de infección previa; de endemicidad moderada, aquellas con prevalencia de infección crónica entre 2% y 7% o 20% a 60% de la población con evidencia serológica de infección previa y de baja endemicidad, las regiones con prevalencia de infección crónica menor a 2% o menos de 20% de la población con infección previa serológicamente evidenciada1,18. En Brasil, se encuentran los tres estándares de endemicidad15; en la Amazonía Legal, la endemicidad por el VHB no es uniforme, existiendo áreas de elevada endemicidad en los valles de los ríos Juruá, Purus y Madeira en la Amazonía occidental y en el valle del río Tapajós en la Amazonía oriental, y áreas de baja y mediana endemicidad, en los valles de los ríos Xingu, Trombetas y Tocantins, en Belém y Manaus4.
La hepatitis C generalmente es asintomática y considerada por muchos, como la enfermedad crónica más importante en todo el mundo. Se calcula que existan en torno de 170 millones de infectados en el mundo, con 3 a 4 millones de portadores crónicos en Brasil21.
La hepatitis D, o Delta, ocurre en áreas endémicas de hepatitis B, visto que el virus delta depende del virus B para ser infectante, se evalúa la existencia de 18 millones de infectados en el mundo, siendo que la prevalencia mayor se encuentra al sur de Italia y en algunas áreas de la ex URSS y en África, además de en la Cuenca Amazónica2,3,5,6,7,11,19.
La hepatitis E tiene epidemiología y curso clínico semejante a la hepatitis A, es importante causadora de brotes, y puede desarrollar cuadros graves de la enfermedad. En Brasil, a pesar de las condiciones sanitarias deficientes en muchas regiones, todavía no ha sido descrita ninguna epidemia.
El Municipio de Juruti localizado a oeste del Estado de Pará, sobre el margen derecho del río Amazonas (coordenadas geográficas 02o09'09"S y 56o05'42"W Gr), limita al norte con los municipios de Oriximiná y Óbidos, al este con Óbidos y Santarém, al sur con Aveiro y a oeste con Faro y con el Estado de Amazonas. Con una población estimada en 34.415 habitantes siendo la mayoría del área rural (20.418)13, en donde se distribuyen 178 comunidades, el municipio posee una importante reserva de bauxita cuya explotación se inició en el año 2005.
El surgimiento o aumento de la frecuencia de enfermedades determinadas por el crecimiento poblacional, urbanización, la deforestación para la extracción del mineral y su posterior recomposición, particularmente en relación a las hepatitis víricas, es verdaderamente diverso del observado en cualquier otra región del mundo, destacándose la posibilidad de la introducción del Virus de la Hepatitis D, en el Municipio de Juruti, a través de la migración de la población de trabajadores de los yacimientos y búsqueda de metales preciosos en los municipios de Santarém, Itaituba y Jacareacanga - en donde este virus ya es endémico.
El presente estudio tiene como objetivos: definir la prevalencia de las infecciones por los virus de las hepatitis A, B, C y D en el hospital municipal de Juruti, Pará, Brasil; analizar la frecuencia de los marcadores serológicos de las infecciones por los virus de las hepatitis A, B, C y D; registrar la frecuencia del estado de portador de las infecciones de las hepatitis B, C y D en el área en estudio; evaluar la respuesta inmune a la vacuna contra la hepatitis B; orientar complementos de vacunación para hepatitis B entre los susceptibles y promover aclaraciones referentes a las infecciones en aprecio, junto a la comunidad involucrada.
MATERIALES Y MÉTODOS
En cuatro etapas de estudio, entre febrero de 2007 y abril de 2008, fueron colectadas informaciones clínico-epidemiológicas y muestras de sangre en la Unidad Mixta de Salud (UMS) Francisco Barros, de Juruti, que se caracteriza por ser el único hospital municipal, de carácter público, con 28 camas y siete médicos desarrollando actividades de ambulatorio en clínica general, pediatría, ginecología/obstetricia, urgencia/emergencia y cirugía.
Fueron incluidas en el estudio, personas de la demanda habitual de la UMS encaminadas a la investigación,por el sector de selección del hospital; individuos sensibilizados por el conocimiento de la ocurrencia de la investigación o reclutados por miembros del equipo de campo en el ambiente de la unidad, tales como acompañantes y parientes de pacientes y profesionales actuantes en aquella unidad, que, en el período de colecta de datos y muestras, manifestaron deseo de participar de la investigación. Se excluyeron todos los que eran contrarios a participar en el estudio.
Los adultos y los niños, por medio de sus responsables fueron invitados a participar del estudio, y les fue explicado por miembros de los equipos, el objetivo y el significado de la investigación, con lectura y firma de Término de Consentimiento Informado.
Para cada participante de la investigación fue completada una ficha individual de averiguación y se colectó de cada uno, por punción venosa, cerca de 8 mL de sangre. En el laboratorio de campo instalado en la Secretaría Municipal de Salud (Semsa), el material, luego de identificado y centrifugado para separación del suero, fue acondicionado en criotubos de 3 mL y refrigerado en congelador hasta su traslado a la Sección de Hepatología del Instituto Evandro Chagas (SAHEP/IEC), en Belém, Pará, Brasil, en donde los sueros fueron congelados a -20o C. hasta la realización de los exámenes.
Por técnica inmunoenzimática, se realizaron en la SAHEP, análisis serológicos para las hepatitis A (anti-VHA total y anti-VHA IgM en los pacientes sintomáticos), B (HBsAg, anti-HBc total, y antiHBs) y C (anti-VHC), a través de kits comerciales de los laboratorios Symbiosys®, Biomérieux® y ORTHO®, respectivamente. En las muestras HBsAg positivo se investigó el HBeAg, anti-HBe (Bio-RAD® y RADIM®), anti-HD total (Biomérieux®) y se detectó el VHB-DNA por (Polymerase Chain Reaction - PCR), a través de la cuantificación del VHB-DNA por el método semiautomatizado COBAS AMPLICOR HBV MONITOR Test® (Roche Diagnostic Systems). En las muestras anti-VHC positivo, fueron efectuados análisis para detección del VHC-RNA por (Reverse Transcriptase Polymerase Chain Reaction - RT-PCR). En todos los análisis se obedecieron las recomendaciones del fabricante y los resultados se consideraron dudosos cuando la densidad óptica estuvo situada entre 20% superior o inferior al límite de cut-off. El excedente de las muestras fue congelado a -70o C, quedando bajo la responsabilidad del IEC.
Los datos y los resultados serológicos se almacenaron en base de datos. Los resultados de los exámenes, la situación de vacunación de los participantes y las orientaciones para el acompañamiento de los casos se entregó a Semsa, para ponerlos a disposición de cada participante de la investigación, para los debidos encaminamientos, conforme recomienda la Secretaría de Vigilancia en Salud (SVS), del Ministerio de Salud (MS).
El proyecto fue aprobado por el Comité de Ética en Investigación del IEC (CAAE 0013.0.072.000-6), en conformidad a la Resolución 196/96 del Consejo Nacional de Salud10.
RESULTADOS
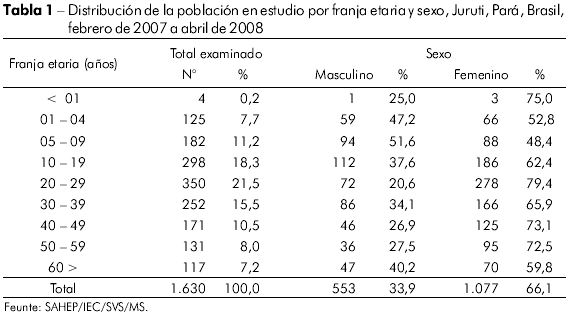
En la investigación, cuyos datos se presentan en la tabla 1, se incluyeron 1.630 individuos, con edad variable entre 5 meses y 89 años, se observó una frecuencia de un 66,1% de individuos de sexo femenino. La población examinada se constituyó principalmente por personas en la franja etaria de 20 a 29 años (21,5%) y la franja etaria menos prevalente (0,2%) estuvo entre los menores de 1 año de edad.
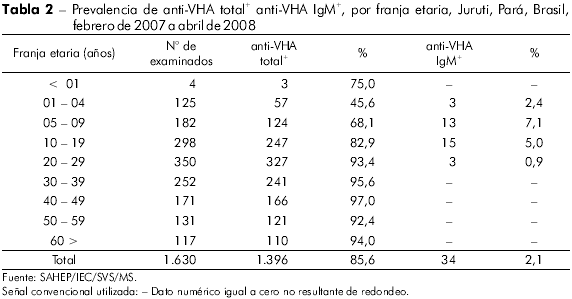
El análisis de las muestras presentado en la tabla 2 mostró prevalencia global de 85,6% para el anti-VHA total+, con 14,4% susceptibles al virus de la hepatitis A. En el período de colecta de material 34 individuos presentaron síntomas y señales compatibles con hepatitis, para los cuales también se realizó anti-VHA IgM mostrando una frecuencia de 2,1% para hepatitis aguda A.
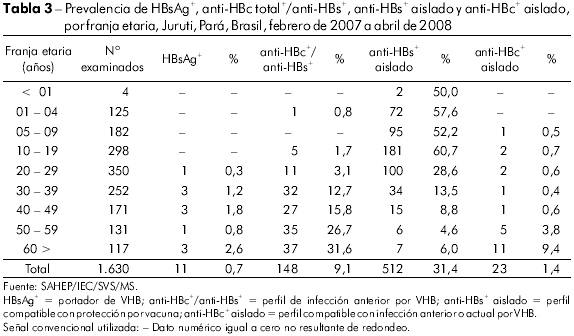
Con relación a la Hepatitis B, conforme lo presentado en la tabla 3, el análisis de las muestras demostró prevalencia total de 42,6% para algún marcador del VHB. Del total examinado, el perfil compatible con estado de portador del virus fue de 0,7%; 9,1% mostraron indicadores de infección anterior por VHB, 31,4% tuvieron perfil compatible con protección por vacunación y 57,4% eran susceptibles al virus de la hepatitis B. Los portadores del virus estaban en el grupo de edad superior a los 20 años. El perfil serológico de vacunas en niños por debajo de los 10 años de edad se mostró en un 54,3% y entre los adolescentes (de los 10 a los 19 años de edad) en un 60,7%.
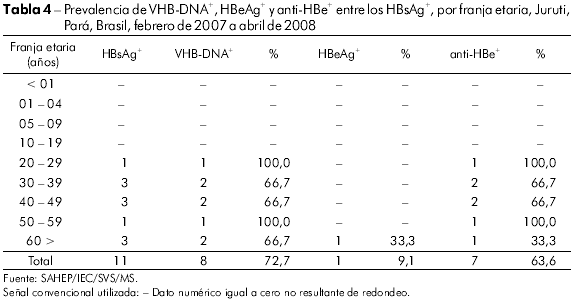
La evaluación de la replicación vírica entre los portadores del virus, mostró 9,1% con HBeAg+, 63,6% con anti-HBe+ y VHB-DNA+ en 72,7% (Tabla 4).
El análisis de las muestras detectó prevalencia de anti-VHC+ de 0,1% (2/1.630). Un individuo del sexo masculino, con edad superior a 60 años tuvo confirmación por RT-PCR.
La investigación del anti-HD se mostró negativa entre las muestras HBsAg+.
DISCUSIÓN
De fácil propagación, la infección por VHA, presenta mundialmente, regiones geográficas de alta, media y baja endemicidad. Estudios de seroprevalencia sobre la hepatitis A realizados en la Amazonia brasileña señalan a la Región Norte como área de alta endemicidad, con seroprevalencia de 92,8%, mayor que el promedio nacional encontrado en 2000, que era de 64,7%9.
La seroprevalencia de 85,6% para Hepatitis A encontrada en el Municipio de Juruti, lo clasifica como de alta endemicidad, compatible con condiciones sanitarias y de higiene desfavorables, destacando la necesidad de poner a disposición de la población agua potable en cantidad suficiente en las residencias, ya que actualmente apenas un 15,5% de la población urbana del Municipio tiene acceso al abastecimiento de agua13, medida más eficaz en el control de la enfermedad, o utilizan medidas alternativas para el abastecimiento de agua en el municipio, para detener el avance de la infección. También es necesario dar destino adecuado a los deyectos, utilizando fosas sépticas correctamente construidas y localizadas; desarrollar al mismo tiempo que las medidas de saneamiento básico, un trabajo educativo en el sentido de valorizar las medidas de saneamiento y consumo del agua, y esclarecer a la comunidad sobre la enfermedad, formas de transmisión, tratamiento y prevención. La vacunación contra la hepatitis A se recomienda a partir de los 12 meses de edad, en dos dosis, con intervalo de 6 meses entre la primera y la segunda dosis, por vía intramuscular, disponible apenas en los Centros de Referencia de Inmunobiológicos Especiales (CRIE) es indicada para hepatópatas crónicos susceptibles a la hepatitis A; menores de 13 años de edad con SIDA; adultos con SIDA portadores de VHB y VHC; portadores de coagulopatías, hemoglobinopatías, enfermedades por depósito, fibrosis quística y trisomías; individuos con inmunodepresión terapéutica o enfermedad inmunodepresora; candidatos a transplante de órgano sólido, transplantados o donadores de órgano sólido o de médula ósea16,17.
Para el Municipio de Juruti la vacunación contra la hepatitis A debe ser discutida como recurso efectivo para la prevención de la infección entre los susceptibles, principalmente entre los más ancianos, una vez que la gravedad de la enfermedad aumenta con la edad14,20. también es necesario dotar a la Semsa de vehículos (autos y embarcaciones), material de informática, área física y recursos humanos para el desarrollo de las actividades de vigilancia epidemiológica tales como: notificación, investigación de casos/brotes y cierre de casos.
La prevalencia de infección por VHB en la población estudiada mostró un estándar de endemicidad moderada, semejante al encontrado por Braga et al8, en Lábrea, Amazonas, en 2004. No se encontraron portadores del virus por debajo de los 20 años de edad y hay indicadores de que la infección es de baja ocurrencia en ese grupo, aunque los niveles de cobertura de vacunación sean inferiores a lo esperado, principalmente entre los adolescentes, tornándose necesaria una evaluación más detallada de la efectividad de la vacuna contra la hepatitis B en ese Municipio. La presión migratoria a la que el Municipio está siendo sometido, implica en riesgo de introducción del virus, principalmente entre niños y adolescentes.
La detección de portadores de VHB, solamente en adultos, reveló que medidas de control de la infección vienen siendo desarrolladas, aunque este estudio haya demostrado que un 62,1% de los examinados es susceptible al virus, habiendo necesidad de estructurar un programa municipal de control y prevención de las hepatitis víricas, con relación a la Hepatitis B, que deberá incluir: a) actividades de educación en salud, enfocando orientaciones sobre los cuidados con material contaminado como máquinas de afeitar, tijeras, cepillos de dientes, tatuajes, uso de condones y materiales médicos desechables y obediencia a las normas de seguridad en el trabajo; b) vacunación universal contra la hepatitis B, de niños y principalmente adolescentes hasta los 19 años de edad, en tres dosis dentro del esquema, 0, 1 y 6 meses, con intervalos de un mes entre la primera y la segunda dosis y de seis meses entre la primera y la tercera12,17 - la vacunación contra la hepatitis B en las primeras 12 horas luego al nacimiento confiere protección equivalente a la obtenida con la aplicación conjunta de vacuna e inmunoglobulina, siendo importante medida de prevención en la transmisión vertical12,17; y c) utilización de la Inmunoglobulina humana antiviral B en recién nacidos de madres portadoras de VHB, víctimas de abuso sexual, comunicantes sexuales de caso agudo o de portadores de hepatitis B, accidentados con material biológico17.
La primera detección de portador del Virus de la hepatitis C en el Municipio, refuerza la necesidad de implantar medidas de vigilancia epidemiológica efectivas para controlar los casos de la infección en esta población. En la ausencia de vacuna y de inmunoglobulina específica contra el VHC, las medidas para el control de la infección están relacionadas a actividades preventivas como: cuidados con material contaminado, evitar uso común de afeitadoras, tijeras, cepillos de dientes; usar preservativos y materiales médico quirúrgicos desechables y obediencia a las normas de bioseguridad17.
La ausencia de portadores del Virus de la Hepatitis D mostró que medidas de vigilancia epidemiológica efectivas, también deben ser implantadas en el Municipio, para eventualmente, detectar de forma precoz el surgimiento de infección por el VHD en esta población. La vacunación contra la hepatitis B es eficaz para reducción de la prevalencia e incidencia de la infección por el Virus de la hepatitis D en los casos de coinfección VHB + VHD, lo mismo no sucede en los casos de superinfección.
La intensificación de la ocupación humana por el aumento de las actividades económicas en el Municipio de Juruti, la apertura de nuevas carreteras, la deforestación, la inexistencia de vacuna para prevención de la infección por el virus de la hepatitis D, los intentos, todavía no satisfactorios de tratamiento, podrán proporcionar transmisión más intensa de VHD, a partir de personas procedentes de Acre, Rondônia y Amazonas, con consecuencias inconmensurables para los portadores crónicos asintomáticos del VHB.
El estudio ha beneficiado a los participantes, permitiendo la adopción de medidas preventivas y de tratamiento, cuando necesario, y ha auxiliado en la comprensión de la situación de vacunación de la hepatitis B en el Municipio, aunque los resultados encontrados hayan sido limitados a la población de la demanda hospitalaria de Juruti.
CONCLUSIÓN
Caracterizamos con base en laboratorio, la alta prevalencia de infección por el virus de la hepatitis A; detección de portadores crónicos y de susceptibles para el VHB; insuficiente cobertura de vacunación en contra del VHB, principalmente entre los adolescentes; presencia de portador del virus de la hepatitis C y ausencia de portadores del virus de la hepatitis D en las muestras examinadas.
Concluimos ser el Municipio de Juruti, de elevada endemicidad para el virus de la hepatitis A, de endemicidad moderada para el virus de la hepatitis B y de baja endemicidad para los virus de las hepatitis C y D.
AGRADECIMIENTOS
A Alcoa/Omnia Minérios Ltda., al Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) y a Semsa de Juruti que en colaboración con el IEC, permitieron la realización del proyecto "Salud en el municipio de Juruti, Pará: escenario actual, desafíos y posibilidades". A la población de Juruti, que nos recibió y aceptó participar de la investigación, contribuyendo de esa manera a ampliar el conocimiento de diversas enfermedades en la región, en particular de las hepatitis víricas.
REFERENCIAS
1 Beasley RP, Whang LY. Overview on the epidemiology of hepatocelular carcinoma. In: Hollinger FB, Lemon SM, Margolis HM, editors. Proceedings of the 1990 International Symposium on Viral Hepatitis and Liver Disease. Baltimore: Williams & Wilkins; 1991. p. 532-5.
2 Bensabath G, Dias LB. Hepatite de Lábrea (Febre Negra de Lábrea) e outras Hepatites fulminantes em Sena Madureira, Acre e Boca do Acre, Amazonas, Brasil. Rev Inst Med Trop Sao Paulo. 1983;25(4):182-94.
3 Bensabath G, Hadler SC, Soares MC, Fields H, Dias LB, Popper H, et al. Hepatitis delta virus infection and Labrea hepatitis. Prevalence and role fulminant hepatitis in the Amazon basin. JAMA. 1987 Jul;258(4):479-83. [ Links ]
4 Bensabath G, Leão RNQ. Epidemiologia na Amazônia Brasileira. In: Focaccia R. editor. Tratado de hepatites virais. São Paulo: Atheneu; 2003. p. 1-26.
5 Bensabath G, Soares MCP, Maia MMS. Hepatite por vírus. In: Instituto Evandro Chagas: 50 anos de contribuição às Ciências Biológicas e à Medicina Tropical. Belém: Fundação Serviços de Saúde Pública 1; 1986. p. 483-529.
6 Bensabath G, Soares MCP. Febre Negra de Lábrea e infecções pelo vírus Delta. In: Instituto Evandro Chagas: 50 anos de contribuição às ciências biológicas e à Medicina tropical. Belém: Ministério da Saúde; Fundação Serviços de Saúde Pública 2. 1986. p. 14-26.
7 Bensabath G, Soares MC. A evolução do conhecimento sobre as hepatites virais na região amazônica: da epidemiologia e etiologia à prevenção. Rev Soc Bras Med Trop. 2004;37 Suppl II:14-26.
8 Braga WSM, Brasil LM, Souza RAB, Melo MS, Rosas MDG, Castilho MC, et al. Prevalência da infecção pelos vírus da hepatite B (VHB) e da hepatite delta (VHD) em Lábrea, Rio Purus, Estado do Amazonas. Epidemiol Serv Saude. 2004;13(1):35-46. [ Links ]
9 Clemens SAC, Fonseca JC, Azevedo T, Cavalcante A, Silveira TR, Castilho MC, et al. Soroprevalência para hepatite A e hepatite B em quatro centros no Brasil. Rev Soc Bras Med Trop. 2000 jan-fev;33(1):1-10. [ Links ]
10 Conselho Nacional de Saúde. Comissão Nacional de Ética em Pesquisa. Normas para pesquisa envolvendo seres humanos: Resolução CNS 196/1996. Brasília: Ministério da Saúde; 2000.
11 Fonseca JC, Simonetti SR, Schatzmayr HG, Castejón MJ, Cesário AL, Simonetti JP. Prevalence of infection with hepatitis Delta virus (HDV) among carriers of hepatitis B surface antigen in Amazonas State, Brazil. Trans R Soc Trop Med Hyg. 1988;82(3):469-71. [ Links ]
12 Fundação Nacional de Saúde. Centro Nacional de Epidemiologia. Coordenação do Programa Nacional de Imunizações. Manual de normas de vacinação. Brasília: Ministério da Saúde; 2002.
13 Instituto Brasileiro de Geografia e Estatística. Censo demográfico 2000. Rio de Janeiro: IBGE; 2001.
14 Lednar WM, Lemon SM, Kirkpatrick JW, Redfield RR, Fields ML, Kelley PW. Frequency of illness associated with epidemic hepatitis A virus infection in adults. Am J Epidemiol. 1985 Aug;122(2):226-33. [ Links ]
15 Secretaria de Vigilância em Saúde. Guia de Vigilância Epidemiológica. 7. ed. Brasília: Ministério da Saúde; 2009.
16 Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Manual dos Centros de Referência para Imunobiológicos Especiais. 3. ed. Brasília: Ministério da Saúde; 2006.
17 Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Hepatites Virais: O Brasil está atento. 3. ed. Brasília: Ministério da Saúde; 2008.
18 Souto FJD. Distribuição da Hepatite B no Brasil: atualização do mapa epidemiológico e proposições para seu controle. Gastrointest Endosc Digest. 1999;18(4):143-50.
19 Viana S, Paraná R, Moreira RC, Compri AP, Macedo V. High prevalence of Hepatitis B Virus and Hepatitis D Virus in the western brazilian Amazon. Am J Trop Med Hyg. 2005;73(4):808-14.
20 Villarejos VM, Serra JC, Anderson-Visoná K, Mosley JW. Hepatitis A virus infection in households. Am J Epidemiol. 1982 Apr;115(4):577-86.
21 World Health Organization. Hepatitis B [Internet]. 2008. Disponível em: http://www.who.int/vaccines-diseases/diseases/hepatitis_b.htm. Acesso em: fev. 10, 2009. [ Links ]
22 World Health Organization. Hepatitis C [Internet]. 2008. Disponível em: http://www.who.int/diseases/diseases/hepatitis_c.htm. Acesso em: fev. 12, 2009.
 Correspondência / Correspondence /
Correspondencia:
Correspondência / Correspondence /
Correspondencia:
Heloisa Marceliano Nunes
Seção de Hepatologia,
Instituto Evandro Chagas/SVS/MS
Av. Almirante Barroso, 492.
Bairro: Marco
66000-000
Belém-Pará-Brasil
Tel.: 55 (91) 3214-2131
E-mail:heloisanunes@iec.pa.gov.br
Recebido em / Received / Recibido en: 13/1/2010
Aceito em / Accepted / Aceito en: 24/3/2010











 texto em
texto em 

