Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.1 n.3 Ananindeua set. 2010
http://dx.doi.org/10.5123/S2176-62232010000300012
Flebótomos (Diptera: Psychodidae: Phlebotominae) en el Municipio de Três Lagoas, área de transmisión intensa de leishmaniasis visceral, Estado de Mato Grosso do Sul, Brasil
Gloria Maria Gelle de OliveiraI; Ernesto Antonio Figueiró FilhoII; Geórgia Medeiros de Castro AndradeIII; Laura Abrahão de AraújoIII; Myrna Lícia Gelle de OliveiraII; Rivaldo Venâncio da CunhaIV
IUniversidade
Federal de Mato Grosso do Sul, Três Lagoas, Mato Grosso
do Sul, Brasil
IIFaculdade de Medicina, Universidade Federal de Mato Grosso do Sul, Campo
Grande, Mato Grosso do Sul, Brasil
IIISecretaria Municipal
de Saúde de Três Lagoas, Três Lagoas,
Mato Grosso do Sul, Brasil
IVDepartamento
de Clínica Médica, Faculdade de Medicina, Universidade
Federal de Mato Grosso do Sul, Campo Grande, Mato Grosso do Sul, Brasil. Instituto
Cerrado-Pantanal, Fundação Oswaldo Cruz, Campo Grande,
Mato Grosso do Sul, Brasil
Endereço para correspondência
Correspondence
Dirección para correspondencia
Título original: Flebotomíneos (Diptera: Psychodidae: Phlebotominae) no Município de Três Lagoas, área de transmissão intensa de leishmaniose visceral, Estado de Mato Grosso do Sul, Brasil. Traducido por: Lota Moncada
RESUMEN
El estudio tuvo como objetivo identificar la fauna flebotomínica urbana y rural; determinar su distribución espacio-temporal; investigar la infección natural por Leishmania de los flebótomos hembras; verificar el impacto de la aplicación de insecticidas sobre la población vectorial; correlacionar datos entomológicos, epidemiológicos y biogeográficos para comprensión de las condiciones favorables a la ocurrencia de la enfermedad; y suministrar informaciones para el control de la leishmaniasis en esa área. Las colectas se realizaron un día por mes, entre agosto de 2000 y diciembre de 2006, con trampas tipo CDC. Fueron capturados 4.277 especímenes, pertenecientes a 14 especies de flebótomos (76,61% en peridomicilio), siendo 3.071 machos y 1.206 hembras. Lutzomyia longipalpis, la especie más frecuente (87,02%), tuvo un índice de constancia estándar igual a 1,0. Los estándares temporo-espaciales de distribución de esa especie ratificaron su importante papel en la transmisión de la leishmaniasis visceral americana. Fue hallada infección por flagelados sugestivos de Leishmania spp. en 1,18% de las hembras disecadas de Lu. longipalpis. Análisis estadísticos mostraron una correlación significativa (p < 0,05) entre el número de vectores, precipitación y humedad. El test de regresión linear demostró asociación significante entre el número de Lu. longipalpis capturado y los casos de leishmaniasis visceral americana humana y canina (p < 0,001). La población de vectores fue reducida en 2002, con la aplicación de insecticidas, pero se elevó en los anos siguientes, debido a la irregularidad de las aspersiones. Son sugeridas en la conclusión, estrategias que podrán ser utilizadas en el control de la enfermedad.
Palabras clave: Entomología; Psychodidae; Insectos Vectores; Leishmania; Leishmaniasis; Vigilancia Epidemiológica.
INTRODUCCIÓN
Los flebótomos (Díptera: Psychodidae: Phlebotominae) son considerados importantes para la salud pública en todo el mundo, especialmente en las regiones tropicales y subtropicales. Las especies del género Phlebotomus encontradas en el Viejo Mundo, y las del género Lutzomyia, en las Americas, son consideradas vectores de innumerables patógenos de vertebrados, incluso Leishmania spp. zoonótica o antropozoonótica, la cual afecta las poblaciones de aproximadamente 90 países, siendo considerada una de las seis enfermedades tropicales más importantes en todo el mundo1. Diversos estudios han incriminado a los flebótomos como hospederos y transmisores de innumerables otros microorganismos2,3,4,5. Cabe recordar que la picada de estos insectos pode causar irritación considerable y reacciones alérgicas en personas sensibles6.
En las Americas, la leishmaniasis visceral, forma más grave de la enfermedad y que puede ser fatal si no es tratada adecuadamente, es endémica en varios países y denominada leishmaniasis visceral americana (LVA). El agente etiológico es la Leishmania {Leishmania) chagasi (Cunha & Chagas, 1937), sus hospederos naturales son los cánidos silvestres (zorros) y, posiblemente, roedores y marsupiales; en los ambientes domiciliarios y peridomiciliarios de las áreas urbanas y rurales son los perros7,8,9. En Brasil, la transmisión ha sido atribuida, principalmente, a Lutzomyia longipalpis (Lutz & Neiva, 1912)7,8, pero otras especies de flebótomos son consideradas como potenciales transmisoras de la enfermedad10. En Pará, Lutzomyia antunesi (Coutinho, 1939) puede ser un vector alternativo de la LVA8. En Mato Grosso do Sul, en la región de Corumbá y Ladário, Lutzomyia cruzi (Mangabeira, 1938) y Lutzomyia forattinii (Galati, Rego, Nunes & Teruya, 1985) son las especies predominantes y simpátricas; ambas han sido consideradas transmisoras del agente de la leishmaniasis visceral11. Otra especie de la fauna flebotomínica de la Serra da Bodoquena, la Lutzomyia almerioi (Galati & Nunes, 1999), presentó infección natural por L. (L.) chagasi y Leishmania (Viannia) sp., alta densidad y acentuada antropofilia, sugestivas de la posibilidad de estar involucrada en la transmisión de la enfermedad en esa región12,13,14,15,16,17.
A pesar de los avances obtenidos en las últimas décadas en el mapeo de la distribución geográfica de las enfermedades transmitidas por vectores, con el uso de sensores remotos por satélite, de sistema de posicionamiento global por satélite (GPS) y de sistemas de informaciones georreferenciadas18,19,20,21, la ocurrencia de expansión de los vectores de la LVA no ha sido sistemáticamente monitoreadas y documentadas. La presente investigación tuvo como objetivo principal conocer aspectos de la ecoepidemiología de la fauna flebotomínica en Três Lagoas, Estado de Mato Grosso do Sul, contribuyendo a la mejoría de los conocimientos sobre la ocurrencia de la LVA en esta localidad, y suministrar informaciones para la vigilancia epidemiológica y control del vector y de la enfermedad.
MATERIALES Y MÉTODOS
ÁREA DE ESTUDIO
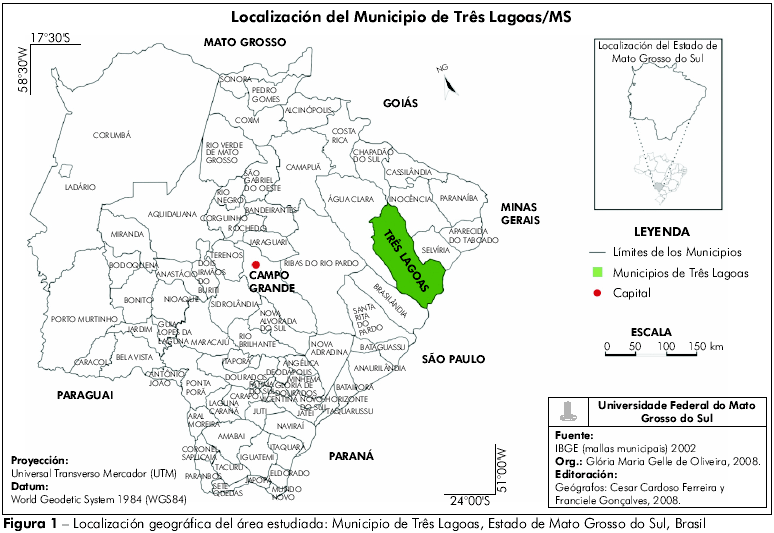
El Municipio de Três Lagoas (52033'44"W, 19036'56"S) se sitúa en el extremo este del Estado de Mato Grosso do Sul, Región Centro-Oeste de Brasil (Figura 1). La altitud promedio en el núcleo urbano es de 319 metros sobre el nivel del mar. Posee clima tropical caluroso y húmedo, precipitación promedio anual de 1.500 mm. y dos estaciones bien definidas: verano lluvioso e invierno seco22. El trimestre de mayor precipitación es el período de noviembre a enero. Las temperaturas promedio mensuales varían entre los 29,3 oC en verano y los 18,1 oC en invierno23 . Su territorio se localiza en la cuenca del río Paraná y presenta biomas naturales importantes, como el cerrado (vegetación predominante) y franjas de mata ciliar, que se alternan perpendicularmente en los márgenes del río Paraná y en la reserva de la Usina Hidroeléctrica de Jupiá; los paisajes son diferenciados, con una amplia variedad de especies de flora y fauna. El área territorial es de 10.206 km2 (2,85% del área total del Estado) y la población es de 85.914 habitantes (densidad poblacional de 8,4 hab./km2), un 94% de los cuales, vive en el área urbana. La economía está basada principalmente, en la pecuaria, complementada por el extractivismo vegetal y el turismo; pasa, actualmente, por un acelerado proceso de industrialización, en vías de tornarse un importante polo industrial en el Estado22.
CAPTURA Y IDENTIFICACIÓN DE LOS FLEBÓTOMOS
El registro de la fauna flebotomínica se realizó entre agosto de 2000 y diciembre de 2006. Se emplearon trampas automáticas luminosas de tipo CDC, instaladas en pares, en peri e intradomicilio, a 50-70 cm sobre el nivel del suelo, al atardecer (18 h) y retiradas al amanecer (6 h), una vez por mes, en locales previamente seleccionados24. El criterio de selección de los locales de captura se basó en la ocurrencia de casos humanos y/o caninos de LVA. Fueron elegidas, por sorteo, dos viviendas en las proximidades (aproximadamente 200 m) de locales con registro de la enfermedad, y donde las condiciones ambientales fueran favorables a los criadores de los vectores. En el extradomicilio se eligieron áreas de silvicultura y de cerrado, propicias a la proliferación de flebótomos. Los especímenes colectados a cada mes eran agrupados y considerados representativos del mes correspondiente.
Luego de la captura, los flebótomos fueron entorpecidos con éter y separados, de modo aleatorio, cinco hembras, por fecha de colecta, para investigar las formas evolutivas de Leishmania. Los demás especímenes fueron acondicionados en frascos de vidrio con tapa plástica conteniendo alcohol a 70%, etiquetados con el nombre, código del área y fecha de la colecta y enviados al laboratorio del Centro de Control de Zoonosis (CCZ) de la Secretaría Municipal de Salud (SMS) de Três Lagoas. En seguida, se realizaron los procesos de clarificación, montaje e identificación de los flebótomos, usando, para el último, la nomenclatura de Young e Duncan25 posteriormente adaptada a la propuesta de Galati26. Se adoptó el sistema de abreviaturas para género y subgénero propuesto por Marcondes27. El material-testimonio fue encaminado al Laboratorio Regional de Entomología de Dourados / Secretaría de Estado de Salud de Mato Grosso do Sul (SES/MS) para confirmar los datos y quedar en depósito.
La presencia de flagelados fue investigada por la disecación de las hembras capturadas, en solución salina a 0,85% y anticontaminantes24 y la observación del intestino al microscopio de contraste de fase (400x); posteriormente, el material teñido con Giemsa fue observado nuevamente. El número, el sexo y las especies de flebótomos capturados fueron registrados en cuadros mensuales por el CCZ/SMS de Três Lagoas.
DATOS CLIMÁTICOS
Los datos climáticos para el período de estudios (temperatura y precipitación promedio mensuales, humedad relativa del aire y velocidad de los vientos) se obtuvieron en el Instituto Nacional de Meteorologia (INMET)23.
ANÁLISIS ESTADÍSTICO
Para el análisis de la abundancia relativa (%) de especies, se utilizaron los datos de capturas efectuadas entre agosto de 2000 y diciembre de 2006. La diversidad de especies encontrada en el Municipio fue calculada con la utilización del índice de Fisher-Willians28,29. La razón sexual (machos:hembras) intra y peridomiciliar se comparó utilizando la prueba del Chi-Cuadrado. La correlación no paramétrica de Spearman se aplicó entre el número de especímenes encontrados, las precipitaciones promedio mensuales y las temperaturas promedio compensadas mensuales, medidas a lo largo del período de estudio. Para analizar la proporción entre individuos infectados por Leishmania (Leishmania) chagasi y el número de flebótomos capturados, se empleó un modelo linear simple para realizar un análisis de regresión logística. El índice de constancia de Lu. longipalpis fue calculado con la fórmula: C = Px100/N, en la que P representa el número de colectas con la especie estudiada y N el número total de colectas realizadas28,29. La distribución mensual de los flebótomos capturados fue comprobada para normalidad con el ensayo de Kolmogorov-Smirnov. Todos los análisis se realizaron utilizando el programa BioEstat, versión 5.030.
RESULTADOS
Entre los puntos monitoreados en Três Lagoas, un 86,8% fue positivo para flebótomos.
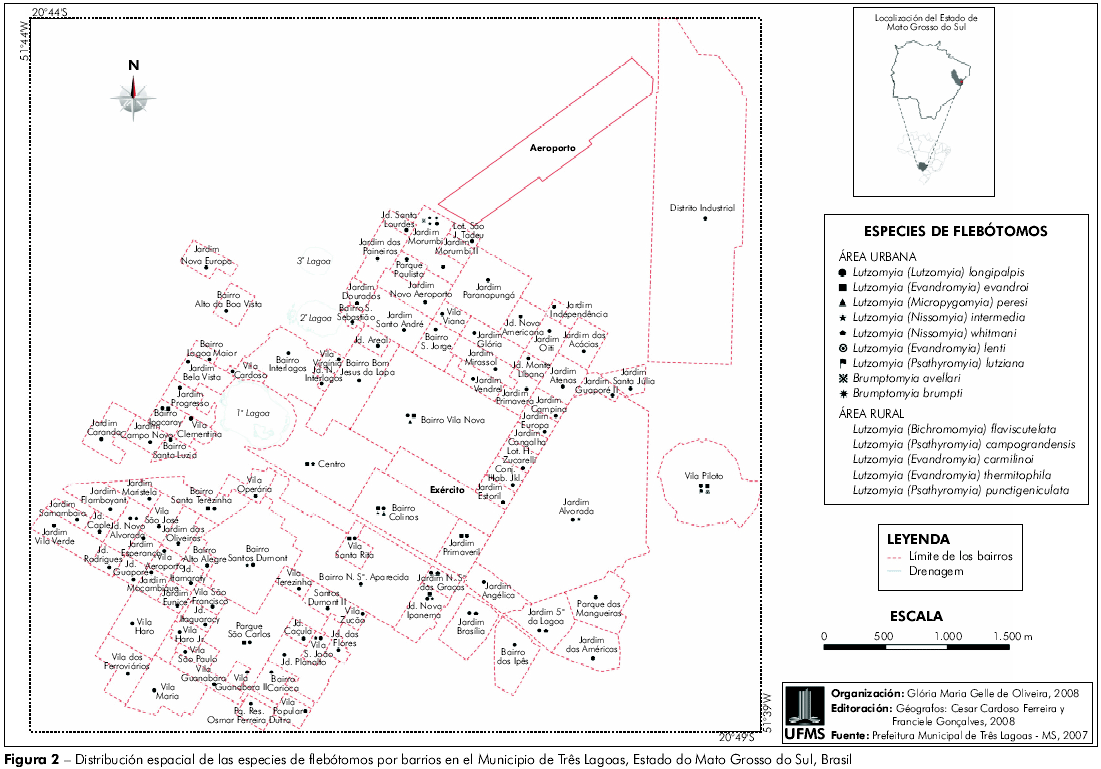
De agosto de 2000 a diciembre de 2006, se colectaron un total de 4.277 especímenes: 3.071 machos (71,81%) y 1.206 hembras (28,19%) pertenecientes a cuatro subtribus, siete géneros y 14 especies. Las dos especies pertenecientes a la subtribu Brumptomyiia fueron: Brumptomyia avellañ (Costa Lima, 1932) e Brumptomyia brumpti (Larrousse, 1920); de la subtribu Lutzomyiina, Lutzomyia longipalpis (Lutz & Neiva, 1912); de la subtribu Psychodopygina, Bichromomyia flaviscutellata (Mangabeira, 1942), Nyssomyia whitmani (Antunes & Coutinho, 1939), Nyssomyia intermedia (Lutz & Neiva, 1912), Psathyromyia punctigeniculata (Floch & Abonnenc, 1944), Psathyromyia campograndensis (Oliveira, Andrade-Filho, Falcão & Brazil), Psathyromyia lutziana (Costa Lima, 1932) y de la subtribu Sergentomyiina, Micropygomyia peresi (Mangabeira, 1942), Evandromyia evandroi (Costa Lima & Antunes, 1936), Evandromyia termitophila (Martins, Falcão & Silva, 1964), Evandromyia carmelinoi (Ryan, Fraiha, Lainson & Shaw, 1986), Evandromyia lenti (Mangabeira, 1938) (Figura 2 y Tabla 1).
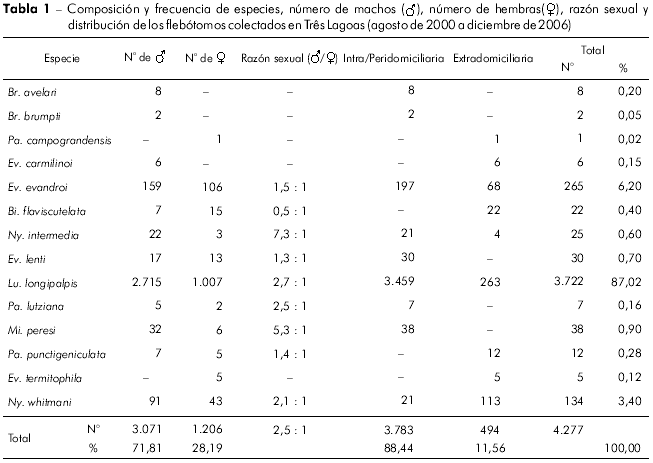
La razón M/F de capturados fue de 2,5 y varió de acuerdo con cada especie de flebótomo (Tabla 1); el número de machos de Lutzomyia longipalpis fue cerca de tres veces superior al de hembras. El índice de diversidad de especies (Fisher-Willians) fue de 1,56. De acuerdo al ensayo de Kolmogorov-Smirnov, hubo una distribución normal de la densidad poblacional de los flebótomos durante el período de investigación (p < 0,01), con un promedio mensual de 59 ± 19.Excepcionalmente, en los meses de marzo de 2002, abril, mayo, agosto y octubre de 2005 y marzo del 2006, se capturó un número relativamente elevado de vectores. En esos meses se registraron bajos niveles de precipitación, pero los índices pluviométricos más elevados en los meses precedentes, humedad relativa superior a 70%, temperaturas entre 22 y 28,5o C y la baja velocidad de los vientos, pueden haber favorecido el aumento poblacional.
Del total de flebótomos, 88,44% fueron colectados en peri e intradomicilio, en ambientes profundamente alterados por la actividad antrópica, y 11,56% en áreas rurales. La especie más abundante fue Lutzomyia longipalpis y correspondió a un 87,02% de los especímenes capturados (Tabla 1), con 3.459 ejemplares (92,93%) en el intra y en el peridomicilio y 263 (7,06%) en el extradomicilio (áreas remanentes de cerrado y huertos forestales); el índice de constancia de C = 1 y la especie estuvo presente en todos los barrios y meses de colectas.
En relación al comportamiento de las especies (endo y exofilia), 2.898 ejemplares (76,61%) fueron capturados en el peridomicilio, siendo 2.087 machos (72,02%) y 811 hembras (27,98%); 885 (23,39%) en el intradomicilio: machos 689 (77,85 %) y 196 hembras (22,15%). Esos datos mostraron que los flebótomos fueron más abundantes en el área peri doméstica y que la predominancia de los machos, en todos los ambientes investigados, fue estadísticamente significante (χ2 = 16,632; p = 0,0002). Las especies más frecuentes en el ambiente intra y peridomiciliar fueron, en orden decreciente, Lu. longipalpis, Ev. evandroi y Mi. peresi.
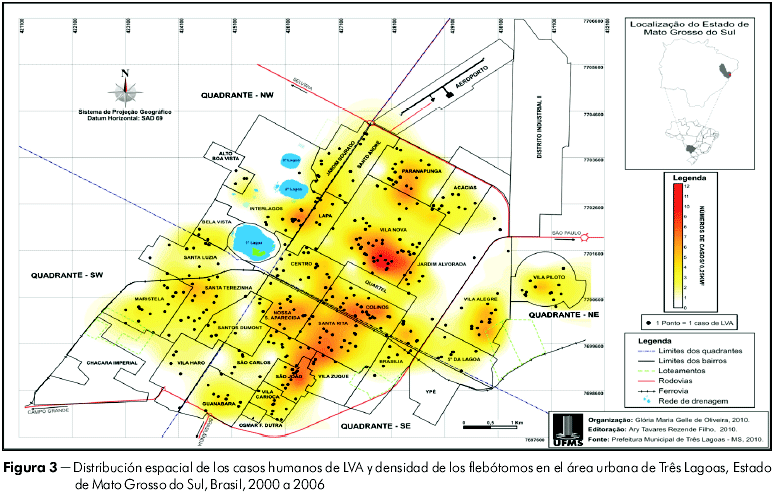
En el área urbana de Três Lagoas, se capturaron flebótomos en todos los barrios investigados (Figura 2); en un 87,71% de ellos, fueron registrados 8.437 casos caninos acumulados de leishmaniasis visceral (promedio de 1.205,3 casos/año) y 284 casos humanos notificados en 64,21% de esas localidades. En el período estudiado, el promedio anual fue de 40,6 casos de LVA humana y hubo un total de 27 óbitos (tasa de letalidad/año = 9,50%), siendo clasificado como municipio "de transmisión intensa" (promedio de casos humanos n ≥ 4,4) por el Ministerio de Salud de Brasil15. Las localidades consideradas de transmisión intensa de LVA y en donde la abundancia relativa de Lu. longipalpis también fue más elevada, se muestran en la figura 3. El análisis de regresión linear resultó en asociación estadísticamente significante entre el número de vectores, casos caninos y humanos de LVA (p < 0,05).
Un total de 928 hembras de Lu. longipalpis seleccionadas al azar, entre las colectadas en peri, intra y extradomicilio, fueron disecadas y en apenas 11 (1,18 %) se encontró positividad para flagelados. Las láminas teñidas con Giemsa mostraron la presencia de formas flageladas sugestivas de Leishmania spp.
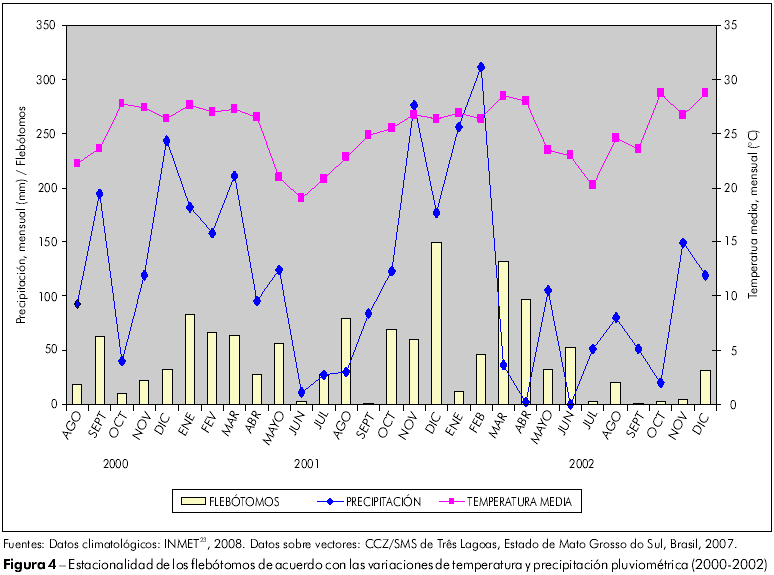
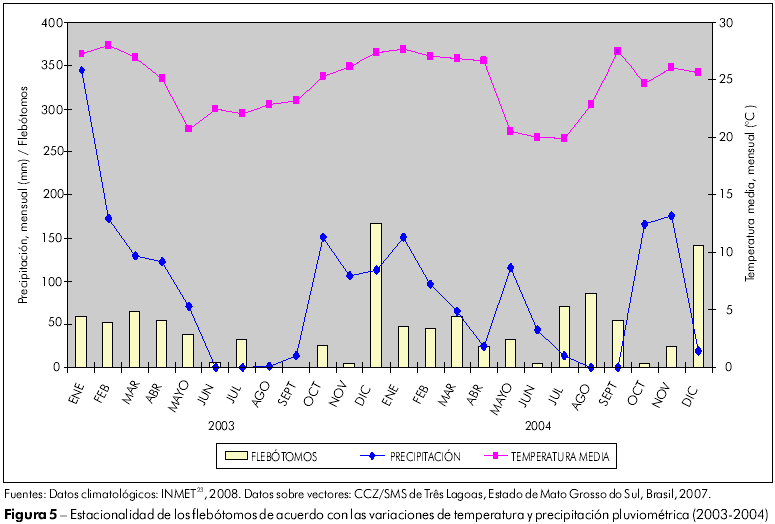
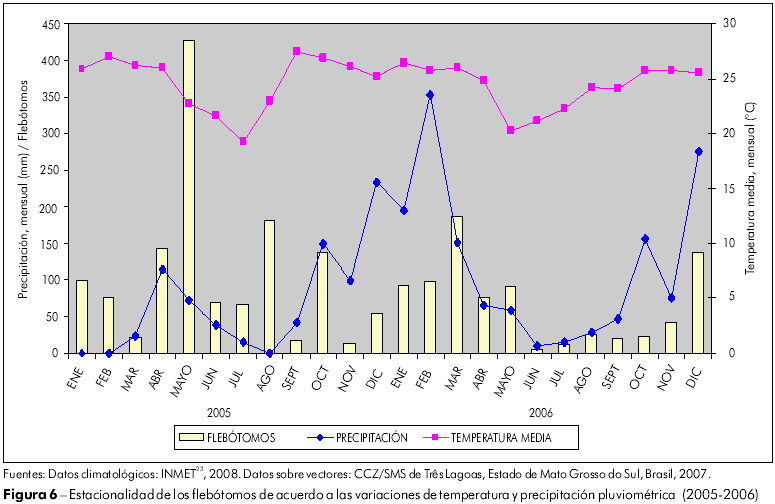
La estacionalidad de los flebótomos a lo largo del período de estudio está representada en las figuras 4, 5 y 6, en las que fueron ploteados: el número total de especímenes colectados mensualmente en todos los locales de captura, la precipitación total mensual y la temperatura promedio compensada mensual en Três Lagoas. El ensayo de correlación de Spearman dejó evidente la correlación, estadísticamente significante (p < 0,05) entre el número de flebótomos capturados y las tasas de precipitación en los años de 2000, 2003, 2004 y 2006 (p < 0,05); en relación a las temperaturas promedio mensuales, la correlación no fue estadísticamente significante (p > 0,05) para los años estudiados, excepto para 2006 (p = 0,0397; p < 0,05).
DISCUSIÓN
El presente estudio entomológico es la primera descripción de la fauna flebotomínica en el Municipio de Três Lagoas, en el cual fueron colectadas e identificadas 14 especies. Los resultados obtenidos son similares a los registrados en otras investigaciones sobre vectores de leishmaniasis, realizadas en diversas regiones brasileñas, en las cuales Lu. longipalpis fue la especie más abundante31,32,33,34,35,36,37.
El índice más alto de abundancia observado en esta investigación fue el de Lu. longipalpis (1,0). Su predominancia en el ambiente doméstico y peri doméstico en la zona urbana (87,02%), especialmente en la región central y barrios, con mayor prevalencia de casos humanos y caninos de LVA, es un fuerte indicativo del comportamiento antropofílico de esa especie, evidencia su importante papel en la transmisión local de la leishmaniasis visceral y sus hábitos alimentares eclécticos. Esto puede conducir al surgimiento de brotes de la enfermedad en perros y en humanos, y, por ese motivo, este vector ha sido considerado el más importante de la LVA en la mayor parte de Brasil34,35,36,37,38.
Algunos flebótomos de importancia médica han demostrado habilidad para adaptarse y explorar ambientes alterados, contribuyendo a la endemicidad de Leishmania spp.39,9. En el Municipio estudiado, poco resta de la vegetación original, que fue sustituida por pastajes, cañaverales y huertos forestales. El área urbana fue casi totalmente desmatada para construir habitaciones y el parque industrial, estando en este momento muy antropizada. Se postula que la predominancia de algunas especies en ambientes profundamente alterados por la acción humana sea un factor de alta magnitud para la transmisión de la leishmaniasis40.
En Mato Grosso do Sul, Lu. longipalpis fue colectado en 92,3% de los municipios estudiados con transmisión de LVA41. Porém, pesquisas realizadas nas cavernas e florestas da serra da Bodoquena; em Corumbá e Ladário, na região do Pantanal sul-mato-grossense; e em Bonito, apontam Lu. cruzi como a espécie mais abundante nessas áreas, dentre os possíveis vetores de leishmaniose visceral. Tais fatos poderiam ser explicados por diferenças na cobertura vegetal, condições climáticas e pelo grau de alterações ambientais antrópicas específicas de cada localidade13,26,14,42,15,16,17.
Evandromyia evandroi, la segunda especie más numerosa en el área estudiada, habitualmente se encuentra en las mismas áreas geográficas de ocurrencia de Lu. longipalpis; Mi. peresi fue la tercera entre las más frecuentes. E. evandroi y Mi. peresi están en franco proceso de domiciliación y no están asociadas a la transmisión de leishmanias al hombre y a los animales. Ny. whitmani y Ny.intermedia presentaron menor frecuencia, aunque están involucradas como vectores de leishmanias habiendo sido capturadas en peri e intradomicilio. Esto puede ser un indicador de alta antropofilia y del gran potencial invasor de esas especies. La ocurrencia simpátrica de Lu. longipalpis y otras especies consideradas posibles vectores de leishmaniasis también se registró en diversas localidades brasileñas en los Estados de Minas Gerais, Espírito Santo, Mato Grosso, Mato Grosso do Sul, Maranhão, Rio Grande do Norte, entre otros, por innúmeros investigadores31,32,33,34,35,43,15,40.
La proporción de machos fue más elevada en relación a las hembras (2,7:1). Esto parece ser resultado de los siguientes hechos: los machos eclosionan antes que las hembras; los criaderos están localizados próximos a las casas de condiciones precarias, con agrietamientos que acumulan lodo y ofrecen abrigo durante el día; la humedad del suelo, que prolonga la vida de los flebótomos; y la abundante presencia de animales domésticos (principalmente perros y aves) en el peridomicilio, los atraerían por el olor (kairomonas) o la liberación de CO2. Los machos, entonces, liberarían feromonas atrayendo a las hembras para la cópula44,45,46. Esas observaciones sugieren proximidad de los machos junto a los hospederos por más tiempo que las hembras, y puede explicar la mayor razón sexual en favor de los machos en las colectas. Por otro lado, las hembras, por sus hábitos hematófagos, son los agentes transmisores de Leishmania y su estrategia reproductiva consistiría en volar hacia afuera de sus abrigos y buscar un local para el repasto sanguíneo, sucediendo entonces el acoplamiento y la disputa por locales para criaderos7,8.
En Três Lagoas, se verificó que Lu. longipalpis estuvo presente, prácticamente, en todos los meses durante el período de estudio. A lo largo del tiempo, esta especie presentó un estándar anual de abundancia irregular, probablemente por la intermitencia de las condiciones climáticas, con picos de aumento poblacional, siguiendo con algún atraso, los períodos lluviosos (aún con pequeños volúmenes de precipitación en el otoño/invierno) y temperaturas entre 22 y 28o C. en la mayor parte del año. Aunque la temperatura parezca ser el factor climático menos importante, el número absoluto de mosquitos fue mayor luego de los períodos en los que hubo una combinación de temperaturas medias más altas, precipitación de lluvias más regular y, consecuentemente, humedad relativa más elevada (Figuras 4, 5 y 6).
La correlación entre la densidad poblacional de los flebótomos y los factores abióticos ya está bien establecida, una vez que esos factores interfieren con el ciclo evolutivo de los flebótomos y alteran sus sitios reproductivos. Innúmeros autores consideran las precipitaciones y la humedad relativa del aire como factores favorables al crecimiento poblacional de estos vectores, debido al desarrollo de la vegetación y al incremento de la cantidad de materia orgánica y de locales favorables a la instalación de criaderos44,32,47.
Fue observada una disminución, tanto del número total de flebótomos capturados en 2002, como de la diversidad de especies, luego de la aplicación domiciliaria, en toda el área urbana, de insecticida piretroide, a partir del mes de junio. En 2003 y en los años subsecuentes, el número de vectores volvió a crecer, debido a la irregularidad de los rociados, los que pasaron a ser realizados apenas en las casas con casos confirmados de LVA humana o canina, en razón de la escasez de insecticida. Otros factores, como condiciones climáticas y fisiográficas desfavorables, pueden haber contribuido también a la reducción observada en los meses más fríos y secos del año.
La densidad de los vectores y la infección natural por Leishmania spp., el bajo nivel socioeconómico de la población, con una tasa de pobreza igual a 32,88%22, la cantidad expresiva de residencias pobres con malas condiciones sanitarias y colecta precaria de residuos, la baja densidad o la ausencia de animales silvestres, el gran número de animales domésticos (principalmente, perros y gallinas) que acumulan detritos en el ambiente peri doméstico y el enorme flujo migratorio causado por el reciente cicl o de industrialización pueden ser determinantes favorables para la instalación y la transmisión de la LVA en el área estudiada, ya que crean diferentes nichos ecológicos propicios a la proliferación y a la concentración de flebótomos44,48.
Por otro lado, diferentes comportamientos antrópicos en el manejo del ambiente familiar, como la remoción de la vegetación y de materiales orgánicos del área peri doméstica, pueden explicar la menor densidad vectorial en residencias en donde la limpieza de las habitaciones y los patios es más cuidadosa. Nuestras constataciones, verificadas in loco, están de acuerdo a los estudios de Dujardin49, Monteiro et al43 y de otros autores.
El número de humanos y perros portadores de LVA en las localidades investigadas fue estadísticamente asociado a la abundancia de Lu. longipalpis (p < 0,05).
El índice de positividad de las hembras de flebótomos para formas promastigotes de Leishmania spp. fue igual a 1,18%; ese valor, aunque bajo, está en acuerdo a los estudios nacionales e internacionales que encontraron tasas entre 1% y 2%42,15,50,5. En la naturaleza, la prevalencia de la infección por Leishmania en la población global de flebótomos puede ser inferior a 0,1%, aún en áreas endémicas y de alta transmisión. Con la intención de aumentar la eficiencia de la transmisión, el parásito manipula de modo adaptado el comportamiento alimentario de los vectores, especialmente Lu. longipalpis, estimulando la persistencia de los insectos para picar y alimentarse a múltiples hospederos; pero eso ocurre solamente si las leishmanias han producido formas infectantes y un gel adhesivo filamentoso de proteoglicanos en la porción anterior del tubo digestivo de los flebótomos51.
Los estudios de la dispersión espacial y temporal de las poblaciones de vectores de leishmaniasis en el Municipio de Três Lagoas y sus habitats preferenciales, indicando las áreas vulnerables o propicias a la transmisión de la enfermedad, permitieron obtener informaciones que pueden subsidiar acciones de prevención y control en el campo de la salud pública. Tener esos datos posibilita la vigilancia entomo-epidemiológica, acompañar de forma continua el comportamiento de los vectores y el estado de salud de la población, de modo que, disponiendo las informaciones necesarias, se pueda detectar o prever alteraciones, dirigir y orientar de modo eficaz la aplicación de medidas preventivas contribuyendo a la mejoría de las condiciones de salud de la comunidad.
REFERENCIAS
1 Desjeux P. Leishmaniasis: current situation and new perspectives. Comp Immunol Microbiol Infect Dis. 2004;27(5):305-18. [ Links ]
2 Ashford RW. Phlebotomus fever. In: Encyclopedia of arthropod transmitted Infections. Wallingford: CABI Publishing; 2001. p. 397-401.
3 Birtles RJ. Carrion's disease. In: Encyclopedia of arthropod transmitted. Wallingford: CABI Publishing; 2001. p. 104-6.
4 Gouveia C, Asensi MD, Zahner V, Rangel EF, Oliveira SMP. Study on the bacterial midgut microbiota associated to different Brazilian populations of Lutzomyia longipalpis (Lutz & Neiva) (Diptera: Psychodidae). Neotrop Entomol. 2008 Sep-Oct;37(5):597-601. [ Links ]
5 Shaw JJ, Travassos de Rosa A, Souza A, Cruz AC. Os flebotomíneos brasileiros como hospedeiros e vetores de determinadas espécies. In: Rangel EF, Lainson R, organizadores. Flebotomíneos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 337-51.
6 El-Badry A, Al-Juhani A, El-Kheir I, Al-Zubiany S. Distribution of sand flies in El-Nekheil province, in Al-Madinah Al-Munawwarah region, western of Saudi Arabia. Parasitol Res. 2008 Jun;103(1):151-6. [ Links ]
7 Lainson R, Rangel EF. Ecologia das leishmanioses: Lutzomyia longipalpis e a ecoepidemiologia da leishmaniose visceral americana (LVA) no Brasil. In: Rangel EF, Lainson R, organizadores. Flebotomíneos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 311-36.
8 Lainson R, Rangel EF. Lutzomyia longipalpis and the ecoepidemiology of American visceral leishmaniasis, with particular reference to Brazil - A review. Mem Inst Oswaldo Cruz. 2005 Dec;100(8):811-27. [ Links ]
9 Travi BL, Osório Y, Becerra MT, Adler GH. Dynamics of Leishmania chagasi infection in small mammals of the undisturbed and degraded tropical dry forests of northern Colombia. Trans R Soc Trop Med Hyg. 1998 May-Jun;92(3):275-8.
10 Carvalho MR, Lima BS, Marinho-Junior JF, Silva FJ, Valença HF, Almeida FA, et al. A fauna de flebotomíneos envolvida em área de incidência de leishmaniose visceral americana na Zona da Mata de Pernambuco, Brasil. Cad Saude Publica. 2007;23(5):1227-32. DOI:10.1590/S0102-311X2007000500024 [ Links ]
11 Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Leishmaniose Visceral. In: Guia de Vigilância Epidemiológica [Internet]. 6. ed. Brasília: Ministério da Saúde; 2005. p. 467-501 [citado 2008 dez 18] . Disponível em : http://portal.saude.gov.br.
12 Aguiar GM, Medeiros WM. Distribuição regional e hábitats das espécies de flebotomíneos do Brasil. In: Rangel EF, Lainson R, organizadores. Flebotomíneos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 207-55.
13 Galati EAB, Nunes VLB, Rego Jr FA, Oshiro ET, Rodrigues M. Estudo de flebotomíneos (Diptera, Psychodidae), em foco de leishmaniose visceral no Estado de Mato Grosso do Sul, Brasil. Rev Saude Publica. 1997 ago;37(4):378-90. [ Links ]
14 Galati EAB, Nunes VLB, Boggiani PC, Dorval MEC, Cristaldo G, Rocha HC, et al. Phlebotomines (Diptera, Psychodidae) in forested areas of the Serra da Bodoquena, Mato Grosso do Sul State, Brazil. Mem Inst Oswaldo Cruz. 2006 Mar;101(2):175-93. DOI:10.1590/S0074-02762006000200010 [ Links ]
15 Pita-Pereira D, Cardoso MAB, Alves CR, Brazil RP, Britto CFPC. Detection of natural infection in Lutzomyia cruzi and Lutzomyia forattinii (Diptera: Psychodidae: Phlebotominae) by Leishmania infantum chagasi in an endemic area of visceral leishmaniasis in Brazil using PCR multiplex assay. Acta Trop. 2008 Jul;107(1):66-9. [ Links ]
16 Santos SO, Arias J, Ribeiro AA, Hoffmann MF, Freitas RA, Malacco MAF. Incrimination of Lutzomyia cruzi as a vector of American Visceral Leishmanisis. Med Vet Entomol. 1998 Jul;12(3):315-7. DOI:10.1046/j.1365-2915.1998.00104.x [ Links ]
17 Savani ESMM, Galati EAB, Nunes VLB, Castilho TM, Camargo COM, D'Ária SRN, et al. Natural infection in sand fly vector in cutaneous and visceral leishmaniasis in Mato Grosso do Sul State, Brazil. Arch Inst Pasteur Tunis. 2005;82:48-9.
18 Barcellos C, Ramalho WM, Gracie R, Magalhães MAFM, Fontes MF, Skaba D. Georreferenciamento de dados de saúde na escala submunicipal: algumas experiências no Brasil. Epidemiol Serv Saude. 2008 mar;17(1):59-70. [ Links ]
19 Cox JSTH. The role of geographic information systems and spatial analysis in area-wide vector control programmes. In: Vreysen MJB, Robinson AS, Hendrichs J, editors. Area-Wide Control of Insect Pests. Dordrecht: Springer; 2007. p. 199-209.
20 Kalluri S, Gilruth P, Rogers D, Szczur M. Surveillance of vector-borne infectious diseases using remote sensing techniques: a review. PLoS Pathog. 2007 Oct;3(10):1361-71. [ Links ]
21 Martins MS, Bavia ME, Silva AB, Cardim LL, Silva CEP, Carneiro DDMT. Técnicas de geoprocessamento aplicadas ao estudo de risco ambiental da leishmaniose visceral em área urbana de Feira de Santana, Bahia. Anais do 13o Simpósio Brasileiro de Sensoriamento Remoto; 2007 abr 21-26; Florianópolis. Florianópolis: INPE; 2007. p. 2825-32. [ Links ]
22 Instituto Brasileiro de Geografia e Estatística. Censo demográfico 2007. [Internet]. Rio de Janeiro: IBGE [citado 2009 set 09]. Disponível em: www.ibge.gov.br.
23 Instituto Nacional de Meteorologia. Mapa dos dados climáticos do município de Três Lagoas/MS no período de 01/01/90 a 31/12/06. Brasília: Ministério da Agricultura, Pecuária e do Abastecimento; 2008.
24 Vilela ML, Rangel EF, Lainson R. Métodos de coleta. In: Rangel EF, Lainson R, organizadores. Flebotomíneos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 353-67.
25 Young DG, Duncan MA. Guide to the identification and geographic distribution of Lutzomyia sand flies in Mexico, the West Indies, Central and South America (Diptera: Psychodidae). American Entomological Institute; 1994. 881 p.
26 Galati EAB. Classificação de Phlebotominae. In: Rangel EF, Lainson R, organizadores. Flebotomíneos do Brasil. Rio de Janeiro: Fiocruz; 2003. p. 23-51.
27 Marcondes CB. A proposal of generic and subgeneric abbreviations for phlebotomine sandflies (Diptera: Psychodidae: Phlebotominae) of the world. Entomol News. 2007 Sep;118(4):351-6. DOI:10.3157/0013-872X(2007)118[351:APOGAS]2.0.CO;2 [ Links ]
28 Silveira Neto S, Nakano O, Barbin D, Vila Nova NA. 1976. Manual de ecologia dos insetos. Piracicaba: Agronômica Ceres; 1976. 419 p.
29 Southwood TRE. Ecological methods, with particular reference to the study of insect populations. New York: Chapman and Hall Publishers; 1984. 524 p.
30 Ayres M, Ayres Jr M, Ayres DL, Santos AS. BioEstat 5.0: aplicações estatísticas nas áreas das ciências biológicas e médicas [CD-ROM]. Belém: Sociedade Civil Mamirauá; 2007. 364 p.
31 Barata RA, Silva JCF, Costa RT, Fortes-Dias CL, Silva JC, Paula EV, et al. Phlebotomine sand flies in Porteirinha, an area of American Visceral Leishmaniasis transmission in the State of Minas Gerais, Brazil. Mem Inst Oswaldo Cruz. 2004;99(5):481-7. [ Links ]
32 Dias ES, França-Silva JC, Silva JC, Monteiro EM, Paula KM, Gonçalves CM, et al. Flebotomíneos (Diptera: Psychodidae) de um foco de leishmaniose tegumentar no Estado de Minas Gerais. Rev Soc Bras Med Trop. 2007;40(1):49-52. [ Links ]
33 Martin MCB, Rebelo JMM. Dinâmica espaço-temporal de flebotomíneos (Diptera: Psychodidae: Phlebotominae) do município de Santa Quitéria, área de cerrado do Estado do Maranhão, Brasil. Iheringia Ser Zool. 2006 set;96(3):283-8. DOI:10.1590/S0073-47212006000300002 [ Links ]
34 Missawa NA, Dias ES. Phlebotomine sand flies (Diptera: Psychodidae) in the municipality of Várzea Grande: an area of transmission of visceral leishmaniasis in the State of Mato Grosso, Brazil. Mem Inst Oswaldo Cruz. 2007 Dec;102(8):913-8. DOI:10.1590/S0074-02762007000800004 [ Links ]
35 Missawa NA, Lorosa ES, Dias ES. Preferência alimentar de Lutzomyia longipalpis (Lutz & Neiva, 1912) em área de transmissão de leishmaniose visceral em Mato Grosso. Rev Soc Bras Med Trop. 2008 jul-ago;41(4):365-8. DOI:10.1590/S0037-86822008000400008 [ Links ]
36 Nunes VLB, Galati EAB, Cardoso C, Rocca MEG, Andrade ARO, Santos MFC, et al. Estudo de flebotomíneos (Diptera, Psychodidae) em área urbana do município de Bonito, Mato Grosso do Sul, Brasil. Rev Bras Entomol. 2008 set;52(3):446-51. DOI:10.1590/S0085-56262008000300019 [ Links ]
37 Oliveira AG, Galati EAB, Oliveira O, Oliveira GR, Espíndola IAC, Dorval MEC, et al. Abundance of Lutzomyia longipalpis (Diptera: Psychodidae: Phlebotominae) and urban transmission of visceral leishmaniasis in Campo Grande, State of Mato Grosso do Sul, Brazil. Mem Inst Oswaldo Cruz. 2006 Dec;101(8):869-74.
38 Silva EAE, Andreotti R, Honer MR. Behavior of Lutzomyia longipalpis, the main vector of american visceral leishmaniasis, in Campo Grande, State of Mato Grosso do Sul. Rev Soc Bras Med Trop. 2007 Jul-Aug;40(4):420-5. DOI:10.1590/S0037-86822007000400010 [ Links ]
39 Marinho RM, Fonteles RS, Vasconcelos GC, Azevedo PCB, Moraes JLP, Rebelo JMM. Flebotomíneos (Diptera: Psychodidae) em reservas florestais da área metropolitana de São Luís, Maranhão, Brasil. Rev Bras Entomol. 2008;52(1):112-6. DOI:10.1590/S0085-56262008000100019 [ Links ]
40 Ximenes MFFM, Silva VPM, Queiroz VS, Rego MM, Cortez AM, Batista LMM, et al. Flebotomíneos (Diptera; Psychodidae) e leishmanioses no Rio Grande do Norte, Nordeste do Brasil: reflexos do ambiente antrópico. Neotrop Entomol. 2007 jan-fev;36(1):128-37. DOI:10.1590/S1519-566X2007000100016 [ Links ]
41 Vigilância em Saúde. Relatório Anual da leishmaniose visceral em Mato Grosso do Sul [Internet]. Campo Grande: Secretaria de Estado da Saúde de Mato Grosso do Sul; 2008 [citado 2008 out 29]. Disponível em: http://www.ses.ms.gov.br.
42 Nascimento JC, Paiva BR, Malafronte RS, Fernandes WD, Galati EAB. Natural infection of phlebotomines (Diptera, Psychodidae) in a visceral leishmaniasis focus in Mato Grosso do Sul, Brazil. Rev Inst Med Trop Sao Paulo. 2007 Mar-Apr;49(2):119-22. DOI:10.1590/S0036-46652007000200011 [ Links ]
43 Michalsky EM, França-Silva JC, Barata RA, Lara e Silva FO, Loureiro AMF, Fortes-Dias CL, et al. Phlebotominae distribution in Janaúba, an area of transmission for visceral leishmaniasis in Brazil. Mem Inst Oswaldo Cruz. 2009 Feb;104(1):56-61. DOI:10.1590/S0074-02762009000100009 [ Links ]
44 Alvar J, Yactayo S, Bern C. Leishmaniasis and poverty. Trends Parasitol. 2006 Dec;22(12):552-7. [ Links ]
45 Kelly DW, Dye C. Pheromones, kairomones and the aggregation dynamics of the sandfly Lutzomyia longipalpis. Anim Behav. 1997;53(4):721-31. DOI:10.1006/anbe.1996.0309 [ Links ]
46 Ward RD, Hamilton JGC, Dougherty M, Falcão AL, Feliciangeli MD, Perez JE, et al. Pheromone disseminating structures in tergides of male phlebotomines (Diptera; Psychodidae). Bull Entomol Res. 1993;83:437-45.
47 Resende MC, Camargo MCV, Vieira JRM, Nobi RCA, Porto NMN, Oliveira CDL, et al. Seasonal variation of Lutzomyia longipalpis in Belo Horizonte, State of Minas Gerais. Rev Soc Bras Med Trop. 2006 Jan-Feb;39(1):51-5. DOI:10.1590/S0037-86822006000100010 [ Links ]
48 Departamento de Vigilância Epidemiológica. Relatório anual das doenças transmitidas por vetores. Três Lagoas: Secretaria da Saúde; 2007.
49 Dujardin JC. Risk factors in the spread of leishmaniasis: towards integrated monitoring? Trends Parasitol. 2006 Jan;22(1):4-6.DOI:10.1016/J.PT.2005.11.004 [ Links ]
50 Ranasinghe S, Rogers ME, Hamilton JG, Bates PA, Maigon RD. A real-time PCR assay to estimate Leishmania chagasi load in its natural sand fly vector Lutzomyia longipalpis. Trans R Soc Trop Med Hyg. 2008 Sep;102(9):875-82. [ Links ]
51 Ready PD. Leishmania manipulates sandfly feeding to enhance its transmission. Trends Parasitol. 2008 Apr;24(4):151-3. [ Links ]
 Correspondência / Correspondence /
Correspondencia:
Correspondência / Correspondence /
Correspondencia:
Gloria Maria Gelle de Oliveira
Universidade Federal de Mato Grosso do Sul,
Departamento de
Enfermagem e Biotecnologia,
Campus de Três Lagoas
Av. Ranulpho Marques Leal, 3884.
Distrito Industrial
CEP:79620-080
Três
Lagoas-Mato Grosso do Sul-Brasil
Tel.: + 55 (67) 3509-3747
E-mail:gloriagelle@gmail.com / gmgol@cptl.ufms.br
Recebido em / Received / Recibido en: 8/7/2010
Aceito
em / Accepted / Aceito en: 13/9/2010











 texto em
texto em 
 Curriculum ScienTI
Curriculum ScienTI
