Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.2 n.1 Ananindeua mar. 2011
http://dx.doi.org/10.5123/S2176-62232011000100012
RELATO DE CASO
Enfermedad de Chagas congénita por infección aguda maternal por Trypanosoma cruzi transmitida vía oral
Ana Yecê das Neves PintoI; Vera da Costa ValenteI; Sebastião Aldo da Silva ValenteI; Amira Consuelo de Melo FigueirasII
ISeção de Parasitologia, Instituto Evandro Chagas/SVS/MS, Ananindeua, Pará, Brasil
IIUniversidade Federal do Pará, Belém, Pará, Brasil
Endereço para correspondência
Correspondence
Dirección para correspondencia
RESUMEN
Una familia de cuatro personas, incluyendo a una mujer de 24 años de edad, se presentó en nuestro laboratorio en diciembre de 2006 con un síndrome febril prolongado de etiología desconocida. Luego de una extensa selección y análisis de laboratorio, se confirmó, por medio de hemocultivo positivo para T. cruzi, combinado con hallazgos clínicos, epidemiológicos y serológicos, la ocurrencia de la enfermedad de Chagas aguda. La paciente, sus padres y marido recibieron una dosis diaria de benzonidazol, pero ella desarrolló intolerancia severa a la droga y amenorrea. Su tratamiento fue interrumpido debido a la confirmación del embarazo con cerca de 12 semanas de edad gestacional. El niño nació prematuramente el 18 de abril de 2007 con bajo peso y señales de síndrome de dificultad respiratoria. Pruebas de selección diagnóstica para infecciones congénitas, incluyendo la enfermedad de Chagas, resultaron negativas durante el período perinatal. Aproximadamente cuatro meses después del nacimiento, los hallazgos clínicos suministraron los siguientes indicadores clínicos de enfermedad congénita: esotropia, microcefalia y retraso en el desarrollo psicomotor. Pruebas serológicas confirmaron la seroconversión y la resonancia magnética presentó lesiones císticas y calcificaciones intracraneanas. Los autores discuten la naturaleza crítica de este grave problema de salud pública en la región y sugieren revisiones necesarias al tratamiento recomendado para pacientes embarazadas con la enfermedad de Chagas aguda.
Palabras clave: Enfermedad de Chagas; Transmisión Vertical de Enfermedad Infecciosa; Agentes Tripanocidas.
INTRODUCCIÓN
Brasil ya fue certificado por la erradicación del Triatoma infestans, el principal vector de la enfermedad de Chagas. El último análisis de seroprevalencia de la enfermedad de Chagas realizado en áreas rurales de Brasil demostró baja tasa de infección entre niños de hasta cinco años de edad y una transmisión congénita de 0,025%1.
A pesar de esos buenos resultados, la vigilancia entomológica continua no debe ser interrumpida. En realidad, este estudio de caso presenta evidencias de que la transmisión directa e indirecta por otros vectores no domiciliarios puede haber sido especialmente aumentada en la Región Amazónica, que tiene ciclos enzoóticos de T. cruzi bien establecidos y ha sido escenario de desequilibrio ecológico resultante de grandes cambios antropogénicos ocurridos en la década de 1990. Esas influencias multifactoriales aumentan el riesgo focal de ocurrencia de la enfermedad de Chagas en la región, como ha sido descrito en estudios anteriores2,3,4.
Este es el primer relato de enfermedad de Chagas congénita autóctona en la Amazonía, resultante de infección materna aguda durante un brote familiar de transmisión oral.
PRESENTACIÓN DEL CASO
Una familia compuesta por cuatro personas, una pareja (hombre con 26 y mujer con 24 años de edad) y los padres de la joven (con 52 y 56 anos de edad), se presentó al Instituto Evandro Chagas (IEC) para solicitar atención en virtud de un síndrome febril prolongado. Los cuatro miembros de la familia fueron acometidos simultáneamente por la enfermedad y la duración fue de 18 días. Los análisis diagnósticos se realizaron a través de dos pruebas serológicas y tres exámenes parasitológicos. Los hallazgos parasitológicos (cultivo de sangre positivo para T. cruzi en dos pacientes), clínicos y serológicos confirmaron un brote de enfermedad de Chagas aguda (ECA) en la familia (Tabla 1).

La investigación epidemiológica no encontró vectores asociados a la transmisión entre los miembros de la familia-sujeto de la investigación. Además su ocurrencia en un área urbana y el aparecimiento casi simultáneo de los síntomas en los cuatro pacientes sugiere una asociación entre la enfermedad y un alimento (asaí) ingerido por todos ellos, aunque este dato no se discute en detalle en el presente estudio.
Todos los pacientes recibieron dosis diarias de benznidazol en enero de 2007. La joven presentó una severa intolerancia a la droga, sufriendo nauseas, vómitos, dolores abdominales y mareos. A consecuencia de eso, y debido a una sospecha de embarazo (amenorrea), el tratamiento fue interrumpido y la paciente experimentó una mejoría espontánea de los síntomas. Confirmado un embarazo de 12 semanas de edad gestacional, fue realizado acompañamiento clínico de la paciente durante toda la gestación. Las pruebas serológicas de hemoaglutinación indirecta (HAI) y el ensayo de inmunofluorescencia indirecta (IFI) realizados arrojaron resultado positivo para los anticuerpos de clase IgG anti-T. cruzi. Las tres pruebas parasitarias seriales dieron resultado negativo. Durante la gestación, la paciente no presentó ningún síntoma de la enfermedad de Chagas. Una ultrasonografía morfológica de la 29a semana de embarazo no señaló ninguna anormalidad.
El recién nacido de sexo femenino, nació prematuramente (34 semanas) el día 18 de abril de 2007, por cesariana y presentó bajo peso (1.850 g), ictericia y síntomas de síndrome de dificultad respiratoria, demandando internación en unidad de terapia intensiva. Durante la internación, el niño fue diagnosticado con neumonía bacteriana. Dos días después del nacimiento, fueron sometidos a exámenes parasitarios y serológicos con el objetivo de detectar la infección por T. cruzi por el método de gota espesa, IFI y HAI. Todas las pruebas resultaron negativas (Tabla 1).
Luego de tres semanas, el recién nacido se recuperó y no presentó ninguna alteración hasta el cuarto mes de vida. Durante una visita de rutina al laboratorio, a los cuatro meses de edad, fue observado esotropía y retraso en el desarrollo psicomotor (no sostenía la cabeza). El examen clínico señaló microcefalia y cierre de la sutura bregmática. Los parámetros hematológicos presentaron un nivel de hemoglobina del 9,7 g %.
Durante este período, los resultados de la investigación por T. cruzi en sangre periférica por el método de microhematocrito, por cultivo de sangre para T. cruzi y por xenodiagnóstico indirecto permanecieron negativos; sin embargo, fue observada una conversión serológica positiva por HAI e IFI (IgG anti-T. cruzi: 80). La tabla 1 muestra todos los resultados de la madre y del niño en diferentes momentos y los resultados relacionados a todos los individuos analizados durante el brote, en la fase aguda de la enfermedad de Chagas. Para evaluar otros posibles agentes de infección congénita, se realizó un estudio serológico para detectar toxoplasmosis (IFI); citomegalovirus por ELISA; sífilis por los métodos de VDRL y FTA-Abs; y rubéola por ELISA. Todos los resultados fueron negativos tanto en la madre como en el niño, con excepción de la prueba para detección de anticuerpos IgG contra el citomegalovirus, que fue positivo en la madre.
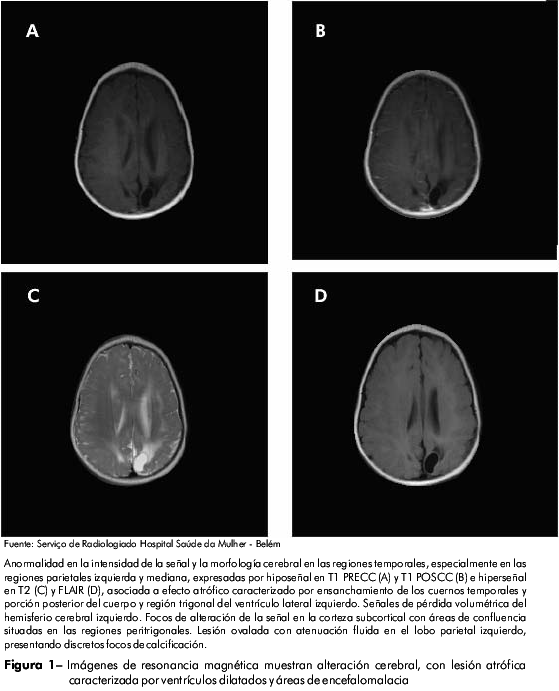
Las imágenes de resonancia magnética señalaron anormalidades en el cerebro del niño, tales como lesiones atróficas caracterizadas por ventrículos dilatados y áreas con encefalomalacia, lo que sugiere la existencia de calcificaciones intracraneanas y lesiones císticas (Figura 1).
La niña fue tratada con benznidazol por 45 días y el caso notificado a la Secretaría Municipal de Salud de Ananindeua. A los 12 meses de edad permanece bajo monitoreo clínico. La madre fue sometida a tratamiento y los efectos colaterales fueron rigurosamente controlados. Las pruebas serológicas de madre e hija permanecieron positivas.
DISCUSÍON
Anteriores investigaciones realizadas en áreas endémicas para T. cruzi hallaron un índice de prevalencia de la enfermedad de Chagas de cerca de 1% en mujeres embarazadas en Brasil, 4% a 6% en gestantes de Argentina, 2% a 3% en Chile y 12% en Bolivia5. Esos índices se relacionan a infección maternal crónica, en la cual los niveles de parásitos en sangre son bajos (1 a 10%)6. En contraste, durante la fase aguda, los niveles del parásito en sangre son altos e inducen a respuesta inmunológica del huésped, lo que aumenta el riesgo de infección congénita7. Sin embargo, la Amazonía Brasileña es un área que se caracteriza por la transmisión activa de ECA y por índices subestimados de infección chagásica8. La ocurrencia de brotes de ECA en áreas urbanas, probablemente libres de vectores y la transmisión por forma no usual, sugieren la adopción de nuevos abordajes metodológicos en estrategias de control de esta antigua enfermedad.
Moretti et al, relataron tres gestantes con ECA en Argentina. Dos de ellas fueron infectadas durante el tercer trimestre y dieron a luz a niños no infectados. La tercera fue infectada durante el segundo trimestre y dio a luz a un niño con hepatoesplenomegalia9. Como en todos los casos en los que hay posibilidad de transmisión vertical, el inicio de la gravidez está asociado a un alto riesgo de infección. Así, la infección de la madre durante el primer trimestre puede haber sido determinante para la infección del niño, bien como para el comprometimiento neurológico severo.
Estudios realizados en Argentina, Bolivia, Paraguay y Brasil describen los espectros clínicos de la infección congénita y sus formas sintomáticas y asintomáticas. Los síntomas clínicos de las formas sintomáticas varían de leves a graves: normalmente se relatan nacimientos prematuros, bajo peso, hepatomegalia, esplenomegalia, señales neurológicas, ictericia, anemia, anasarca y síndrome de dificultad respiratoria10,11,12,13. En el niño objeto de este estudio las principales señales clínicas observadas fueron ictericia, anemia y síndrome de dificultad respiratoria; hay raras descripciones de bajo desarrollo neurológico con calcificación intracraneana en casos de enfermedad de Chagas congénita. Existe apenas un registro, de La Paz, Bolivia, semejante al descrito en este estudio14. Por otro lado, una serie de casos observados en Argentina demuestran que un 64,8% de los niños no presenta síntomas clínicos y que en niños sintomáticos, la hepatomegalia fue el principal síntoma observado12.
En ningún momento se encontraron parásitos en la sangre periférica del niño durante el período de monitoreo. El diagnóstico fue hecho por pruebas de conversión serológica, datos epidemiológicos (datos relacionados a la transmisión vertical de una madre con ECA) y hallazgos clínicos. La sensibilidad de las pruebas parasitarias se reduce en casos congénitos debido a la baja parasitemia y el diagnóstico se hace, frecuentemente, por serología. Por eso, el acompañamiento clínico de un niño desempeña un papel importante en el diagnóstico y, posteriormente, en la respuesta potencial (serología negativa) al tratamiento.
El riguroso control de la ECA en gestantes y recién nacidos de áreas de alto riesgo en la Región Amazónica durante los períodos prenatal y perinatal es un desafío importante para los sistemas de vigilancia en salud pública. Madres y sus recién nacidos con reacciones serológicas positivas deben pasar por exámenes parasitarios directos por el método de microhematocrito inmediatamente después del parto. Además, los niños deben ser monitoreados hasta alcanzar, por lo menos, nueve meses de edad. En Brasil, el Consenso Brasileño en Enfermedad de Chagas refuerza la necesidad de análisis serológico de gestantes y el monitoreo de niños nacidos de madres acometidas por la enfermedad de Chagas15,16. Sin embargo, esta importante recomendación es frecuentemente ignorada en el país y en la mayoría de las naciones en las que la enfermedad de Chagas es endémica.
El segundo desafío en el control de la enfermedad de Chagas es la revisión de protocolos de tratamiento con el uso de benznidazol en gestantes con ECA. Mujeres grávidas necesitan cuidados individualizados para hacer uso de esta droga17. Se sugiere que la indicación de benznidazol sea discutida con la madre, especialmente después de la vigésima cuarta semana de embarazo (cuando hay una reducción del potencial lesivo de la droga para el feto). El desarrollo de drogas eficaces, con el mínimo posible de efectos colaterales, debe ser una prioridad para los sistemas de salud pública en áreas que presenten focos activos de transmisión de enfermedad de Chagas.
Además, todos los esfuerzos son válidos para fortalecer los sistemas de vigilancia en enfermedad de Chagas en Brasil. Para tal, la capacitación de recursos humanos se configura una estrategia de control esencial tanto para perfeccionar la calidad de los diagnósticos de laboratorio, como para mejorar la sensibilidad de sospecha clínica a nivel de atención primaria individual y también formar personal habilitado, con desempeño sustentable, para, de esta manera, comprender los varios componentes de la cadena de transmisión de este agravamiento, antiguo en Brasil, pero emergente en la Región Amazónica.
CONCLUSÍON
Mujeres con ECA presentan mayor riesgo de transmisión de enfermedades al feto que madres con infección crónica. El potencial de ocurrencia de lesiones irreversibles en recién nacidos, como resultado de esta transmisión vertical (como descrito en este relato), indica la necesidad de la revisión de las recomendaciones sobre el uso de drogas tripanosomicidas en esos casos.
AGRADECIMIENTOS
A Francelino de Almeida Araújo Júnior, del Hospital Saúde da Mulher, Belém, por las imágenes de resonancia magnética.
APOYO FINANCEIRO
Instituto Evandro Chagas e UNESCO
REFERENCIAS
1 Ostermayer AL, Passos ADC, Silveira AC, Ferreria AW, Macedo V, Prata A. O inquérito nacional de soroprevalência de avaliação do controle da doença de Chagas no Brasil (2001-2008). Rev Soc Bras Med Trop. 2011;44 Suppl 2:S108-21. [Link]
2 Coura JR, Junqueira AC, Fernandes O, Valente SA, Miles MA. Emerging Chagas disease in Amazonian Brazil. Trends Parasitol. 2002 Apr;18(4):171-6. Doi:doi:10.1016/S1471-4922(01)02200-0 [Link]
3 Pinto AYN, Ferreira Jr AG, Valente VC, Harada GS, Valente SAS. Urban Outbreak of Emerging acute Trypanosomiasis in Brazilian Amazon: 4-year follow-up post treatment with benznidazol. Rev Panam Salud Publica. 2009 Jan;25(1):77-83.
4 Valente SA, Valente VC, Pinto AYN. Epidemiologia e transmissão oral da doença de Chagas na Amazônia brasileira. In: Organización Panamericana de la Salud. Organización Mundial de la Salud. Unidad. Informe de la consulta técnica en Epidemiología, Prevención y Manejo de la Transmisión de la Enfermedad de Chagas como Enfermedad Transmitida por Alimentos. Rio de Janeiro: OPS/OMS; 2006. p. 21-6. [Link]
5 Schmunis GA. A Tripanosomíase Americana e seu impacto na Saúde Pública das Américas. In: Brener Z, Andrade ZA, Barral-Neto M, editors. Trypanosoma cruzi e Doença de Chagas. 2. ed. Rio de Janeiro: Guanabara Koogan; 2000. p. 1-15.
6 Bittencourt AL. Transmissão vertical da doença de Chagas. In: Brener Z, Andrade ZA, Barral-Neto M, editors. Trypanosoma cruzi e doença de Chagas. 2. ed. Rio de Janeiro: Guanabara Koogan; 2000. p. 16-20.
7 Hermann E, Truyens C, Alonso-Vega C, Rodriguez P, Berthe A, Torrico F, et al. Congenital transmission of Trypanosoma cruzi is associated with maternal enhanced parasitemia and decreased production of interferon- gamma in response to parasite antigens. J Infect Dis. 2004 Apr;189(7):1274-81. [Link]
8 Organização Pan Americana da Saúde. Guia para vigilância, prevenção, controle e manejo clínico da doença de Chagas aguda transmitida por alimentos. Rio de Janeiro: PANAFTOSA-VP/OPAS/OMS; 2009. p. 92. (Serie de Manuais Técnicos, 12). [Link]
9 Moretti E, Basso B, Castro I, Carrizo Paez M, Chaul M, Barbieri G, et al. Chagas disease: study of congenital transmission in cases of acute maternal infection. Rev Soc Bras Med Trop. 2005 Jan-Feb;38(1):53-5. [Link]
10 Torrico F, Alonso-Vega C, Suarez E, Rodríguez P, Torrico MC, Dramaix M, et al. [Endemic level of congenital Trypanosoma cruzi infection in the areas of maternal residence and the development of congenital Chagas disease in Bolivia]. Rev Soc Bras Med Trop. 2005;38 Suppl 2:17-20. [Link]
11 Negrette OS, Mora MC, Basombrio MA. High prevalence of Congenital Trypanosoma cruzi infection and family clustering in Salta, Argentina. Pediatrics 2005 Jun; 115(6):668-72. [Link]
12 Freilij H, Altched J. Congenital Chagas' disease: diagnostic and clinical aspects. Clin Infect Dis. 1995 Sep;21(3):551-5. [Link]
13 Gürtler ER, Segura E, Cohen J. Congenital transmission of Trypanosoma cruzi infection in Argentina. Emerg Inf dis. 2003 Jan;9(1):29-32. [Link]
14 Pehrson P, Walgren M, Bengstsson E. Intracranial calcifications probably due to congenital chagas disease. Am J Trop Med Hyg. 1982 May;31(3):449-51.
15 Ministério da Saúde (BR). Secretaria de Vigilância em Saúde. Consenso Brasileiro em Doença de Chagas. Rev Soc Bras Med Trop. 2005;38 Suppl 3:S30.[Link]
16 Gontijo ED, Andrade GMQ, Santos SE, Galvã LMC, Moreira EF, Pinto FS, et al. Triagem neonatal da infecção pelo Trypanosoma cruzi em Minas Gerais, Brasil: transmissão congênita e mapeamento das áreas endêmicas. Epidemiol Serv Saúde. 2009 jul-set;18(3):243-54. [Link]
17 Bittencourt AL. Actual aspects and epidemiological significance of congenital transmission of Chagas' disease. Mem Inst Oswaldo Cruz. 1984;79 Suppl:133-7. [Link]
 Correspondence / Correspondência / Correspondencia:
Correspondence / Correspondência / Correspondencia:
Ana Yecê das Neves Pinto,
Setor Médico Unificado (SOAMU)/Epidemiologia,
Instituto Evandro Chagas/SVS/MS
BR 316 Km 7 s/n,
ZIP code: 67030-070, Ananindeua/PA
Phone – FAX number: 91 32142189
E.mail:ayece@iec.pa.gov.br
Recebido em / Received / Recibido en: 10/5/2011
Aceito em / Accepted / Aceito en: 18/7/2011











 texto em
texto em 
 Curriculum ScienTI
Curriculum ScienTI
