Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Pan-Amazônica de Saúde
versão impressa ISSN 2176-6215versão On-line ISSN 2176-6223
Rev Pan-Amaz Saude v.6 n.1 Ananindeua mar. 2015
http://dx.doi.org/10.5123/S2176-62232015000100006
ARTIGO ORIGINAL | ORIGINAL ARTICLE | ARTÍCULO ORIGINAL
Detecção de atividade de fosfatase ácida nos hemócitos de Biomphalaria glabrata (Gastropoda: Planorbidae): um estudo em moluscos da Região Amazônica, Brasil
Detection of acid phosphatase activity in hemocytes of Biomphalaria glabrata (Gastropoda: Planorbidae): a study in molluscs from Amazon Region, Brazil
Detección de actividad de fosfatasa ácida en los hemocitos de Biomphalaria glabrata (Gastropoda: Planorbidae): un estudio en moluscos de la Región Amazónica, Brasil
Daniel Valle Vasconcelos SantosI; José Antonio Picanço Diniz JuniorII; Marco Antonio Vasconcelos SantosI
ILaboratório de Biologia e Eletrofisiologia em Células Parasitárias, Seção de Parasitologia, Instituto Evandro Chagas/SVS/MS, Ananindeua, Pará, Brasil
IILaboratório de Microscopia Eletrônica, Seção de Hepatologia, Instituto Evandro Chagas/SVS/MS, Ananindeua, Pará, Brasil
Endereço para correspondência
Correspondence
Dirección para correspondencia
RESUMO
Foram utilizados hemócitos de planorbídeos da espécie Biomphalaria glabrata para a realização de citoquímica para detecção de atividade da fosfatase ácida, usando a técnica de laranja de acridina, com o objetivo de marcação de compartimentos ácidos citoplasmáticos. Essa espécie de caramujo é a mais utilizada para o estudo de interação parasito-hospedeiro devido à maior suscetibilidade em infectar-se pelo Schistosoma mansoni e por ser capaz de grande multiplicação parasitária em seus tecidos, apesar da atividade do seu sistema imunológico. A citoquímica ultraestrutural foi também utilizada para marcação de atividade da fosfatase ácida em inclusões citoplasmáticas limitadas por membrana. Os resultados mostram que o uso de laranja de acridina possibilita a marcação de compartimentos ácidos no interior de granulócitos; entretanto, essa marcação não ocorreu em hialinócitos, o que pode auxiliar na distinção desses dois tipos de células presentes na hemolinfa desse molusco. A citoquímica ultraestrutural possibilitou a visualização de depósitos eletrodensos localizados no interior dos grânulos citoplasmáticos constituídos basicamente por membranas, confirmando a atividade da fosfatase ácida.
Palavras-chave: Biomphalaria glabrata; Schistosoma mansoni; Hemócitos; Fosfatase Ácida; Citoquímica.
ABSTRACT
Planorbidae hemocytes of Biomphalaria glabrata were utilized for cytochemical detection of acid phosphatase activity, using acridine orange technique for marking the cytoplasmic acid compartments. This species of snail is the most widely used for studying host-parasite interaction due to greater susceptibility to becoming infected by Schistosoma mansoni, and to be capable of fast parasite multiplication in their tissues, despite the activity of its immune system. The ultrastructural cytochemistry was also used for marking the acid phosphatase activity in cytoplasmic inclusions limited by a membrane. The results show that acridine orange may be a marker for the acid compartments within granulocytes; however, this did not occur in hyalinocytes marking, which may help to distinguish these two types of cells present in the hemolymph of this mollusk. The ultrastructural cytochemistry enabled the visualization of electron dense deposits located within the cytoplasmic granules basically consisting of membranes, confirming the activity of acid phosphatase.
Keywords: Biomphalaria glabrata; Schistosoma mansoni; Hemocytes; Acid Phosphatase; Cytochemistry.
RESUMEN
Se utilizaron hemocitos de planorbideos de la especie Biomphalaria glabrata para realizar la detección citoquímica de la actividad de la fosfatasa ácida usando la técnica del naranja de acridina, con el objetivo de marcar los compartimientos de ácidos citoplasmáticos. Esta especie de caracol es la más utilizada para el estudio de la interacción parásito/huésped debido a su gran susceptibilidad para infectarse por Schistosoma mansoni y por ser capaz de gran multiplicación parasitaria en los tejidos a pesar de la actividad de su sistema inmunológico. La citoquímica ultraestructural también fue utilizada para marcar la actividad de la fosfatasa ácida en inclusiones citoplasmáticas limitadas por membrana. Los resultados muestran que el uso del naranja de acridina posibilita la marcación de compartimientos ácidos al interior de los granulocitos; sin embargo, esa marcación no ocurrió en hialinocitos, lo que puede auxiliar en la distinción de esos dos tipos de células presentes en la hemolinfa de ese molusco. La citoquímica ultraestructural posibilitó la visualización de depósitos electrodensos localizados al interior de los gránulos citoplasmáticos constituidos básicamente por membranas, confirmando la actividad de la fosfatasa ácida.
Palabras clave: Biomphalaria glabrata; Schistosoma mansoni; Hemocitos; Fosfatasa Ácida; Citoquímica.
INTRODUÇÃO
A esquistossomose é uma parasitose que tem como agente etiológico um trematódeo pertencente da subclasse digênea, família Schistosomatidae e gênero Schistosoma, onde todas as espécies são adaptadas ao parasitismo.
As três espécies de moluscos vetores dessa enfermidade no Brasil são: Biomphalaria tenagophila, Biomphalaria straminea e Biomphalaria glabrata. A distribuição geográfica desses caramujos mostra B. tenagophila com habitat mais frequente nos estados das Regiões Sul e Sudeste, e pouca presença no Centro-Oeste. B. straminea tem ampla distribuição nos estados do nordeste e pouca presença no centro-oeste e norte; e, finalmente a B. glabrata tem presença em quase todo o território brasileiro.
A presença no Brasil dessas três espécies de caramujo, somada às correntes migratórias promovidas inicialmente pelo processo de colonização brasileira, fez com que essa doença despertasse cada vez mais a atenção da saúde pública. Assim, o conhecimento sobre a ecologia dos moluscos transmissores da esquistossomose mansônica é de fundamental importância para a caracterização do quadro epidemiológico desta parasitose em uma região.
Vários estudos acerca da infecção e da reação imunológica de gastrópodes concluíram que o primeiro mecanismo de defesa interno desses moluscos resistentes à infecção por endoparasitos metazoários é o encapsulamento do organismo orquestrado por invasor pelas células de defesa do organismo invadido1,2,3,4. Esse encapsulamento é realizado pelos hemócitos, presentes na hemolinfa destes moluscos, e fazem parte do sistema imune do invertebrado, atuando contra possíveis organismos invasores2,4,5. Outros estudos que demonstram o mecanismo celular e as substâncias envolvidas nesse processo, vêm sendo desenvolvidos desde as décadas de 1970 e 19806,7,8,9,10,11
Enzimas como a fosfatase ácida, lisozimas, fosfatase alcalina, β-glucuronidase, amilase e lipase foram encontradas na hemolinfa de B. glabrata12. Os autores desses achados sugerem que essas enzimas possam ser produzidas nos lisossomos dos granulócitos, as quais seriam lançadas na hemolinfa como um mecanismo de defesa humoral contra a invasão de microrganismos12.
Poucos estudos demonstraram o local de produção destas enzimas, que são de fundamental importância para o entendimento da fisiologia dessas células fagocitárias13,14,15,16. Conclusões importantes foram obtidas a respeito da produção de enzimas hidrolíticas pelas células17. Outros estudos também demonstraram que a elevação da atividade enzimática deve-se a um aumento na síntese das enzimas e não a um aumento do número de hemócitos6, embora algumas pesquisas tenham registrado que o número de hemócitos foi duas vezes maior quando os caramujos foram expostos aos miracídios de Schistosoma mansoni8,18,19,20. Com essas importantes contribuições, torna-se necessária a identificação das organelas celulares responsáveis pela sua produção. Entretanto, muitas organelas só podem ser identificadas utilizando-se técnicas citoquímicas, o que é o caso do lisossomo, pois apenas a sua caracterização morfológica não é suficiente para afirmar a sua presença na célula.
No contexto da transmissão da esquistossomose, a espécie B. glabrata é o caramujo mais utilizado para o estudo de interação parasito/hospedeiro, principalmente em função de dois fatores: 1) maior suscetibilidade para infectar-se pelo S. mansoni e dessa forma garantir a sobrevivência da espécie8; e 2) ser capaz de grande multiplicação parasitária em seus tecidos, apesar da atividade do seu sistema imunológico10,15. Trabalhos anteriores mostraram que não foram encontradas marcações para fosfatase ácida em hialinócitos, porém a detecção foi positiva em granulócitos8,11.
Diante das informações apresentadas, nosso trabalho teve como objetivo identificar o local de atividade das enzimas fosfatase ácida lisossoma (E.C. 3.1.3.2), utilizando técnicas de fluorescência e de citoquímica ultraestrutural.
MATERIAIS E MÉTODOS
MOLUSCOS UTILIZADOS
Para o desenvolvimento deste estudo foram utilizados 140 caramujos da espécie B. glabrata, criados e reproduzidos em laboratório a partir de posturas de caramujo coletados na região bragantina, a nordeste do Estado do Pará, Brasil. Todos os espécimes apresentaram diâmetro de concha variando entre 1,8 cm a 2,2 cm. Estes foram infectados individualmente com cinco miracídios de S. mansoni. Os caramujos foram confinados em pequenos potes de vidro contendo 3 mL de água potável sem cloro (em temperatura ambiente), sob iluminação artificial, durante 90 min, e posteriormente mantidos em aquários de vidro contendo água sem cloro e permaneceram no laboratório, em ambiente pouco ilumidado. A água do aquário foi trocada a cada 72 h e os animais foram alimentados ad libitum com folhas de alface frescas.
COLETA DA HEMOLINFA
A retirada da hemolinfa foi realizada com introdução de agulha 30 x 8 (21G 1 1/4) na região cefalopodal até que a cavidade do manto fosse atingida. Após a retirada da agulha e consequente retração do animal, a hemolinfa fluiu para a curvatura da concha de onde ela foi aspirada com seringa siliconada. Esta hemolinfa foi, então, transferida para um tubo de vidro de 10 mL, também siliconado, e mantido a 4° C.
MICROSCOPIA DE FLUORESCÊNCIA
Para a identificação de compartimentos ácidos na célula, utilizou-se a técnica de fluorescência indicativa de acidificação na presença de laranja de acridina. Foi utilizado um pool de 10 mL de hemolinfa colhida de 50 caramujos selecionados pelo diâmetro da concha (mínimo de 1 cm e máximo de 2 cm de diâmetro). Esta amostra foi centrifugada a 223 xg por 10 min, tendo o sobrenadante sido retirado e mantido a 4° C. O sedimento restante foi ressuspendido e incubado em 100 μL de solução de laranja de acridina (5 μg/mL) em temperatura ambiente na ausência de luz. Este material foi novamente centrifugado a 223 xg e o sobrenadante, retirado. O sedimento foi lavado três vezes com a hemolinfa estocada na primeira centrifugação. Foram aderidos 200 μL desta suspensão em uma lamínula e observados imediatamente em microscopia de fluorescência11.
CITOQUÍMICA ULTRAESTRUTURAL
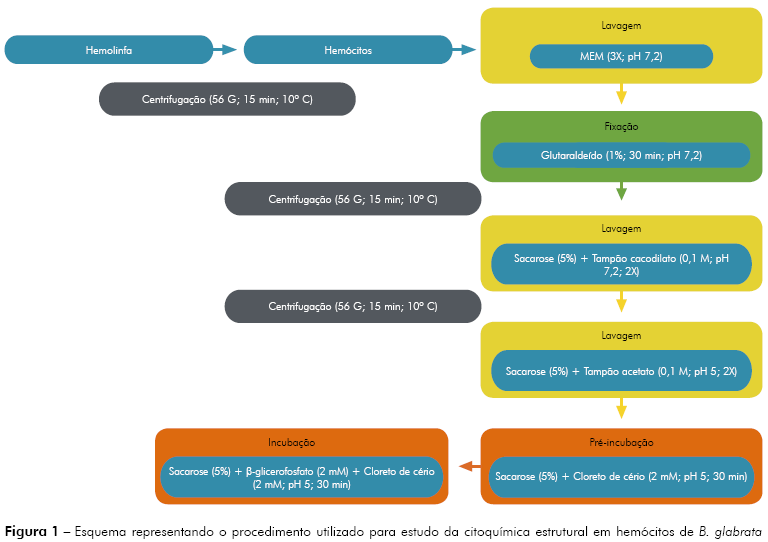
Para a caracterização ultraestrutural das organelas e a detecção da enzima, utilizou-se a técnica de citoquímica ultraestrutural para a localização de fosfatase ácida por microscopia eletrônica de transmissão. Foram utilizados 90 caramujos B. glabrata com diâmetro de concha variando entre 1,5 cm a 2,0 cm. O volume de hemolinfa colhido de cada caramujo variou de 100 μL a 200 μL. Desta forma, o volume final de hemolinfa foi de 15 mL. Esta amostra foi processada de acordo com o esquema disposto na figura 1 e posterior procedimento de rotina para microscopia eletrônica de transmissão21.
RESULTADOS
Neste estudo, utilizando-se a laranja de acridina, foi possível evidenciar a presença de compartimentos citoplasmáticos marcados após incubação com este corante fluorocromático. A marcação ocorreu em compartimentos de células com características morfológicas de granulócitos, entretanto o mesmo não ocorreu em células com morfologia típica de hialinócitos (Figuras 2A e 2C). A figura 2B mostra as mesmas células evidenciadas por microscopia de luz, utilizando o sistema de contraste interferencial diferencial de Nomarski (DIC).
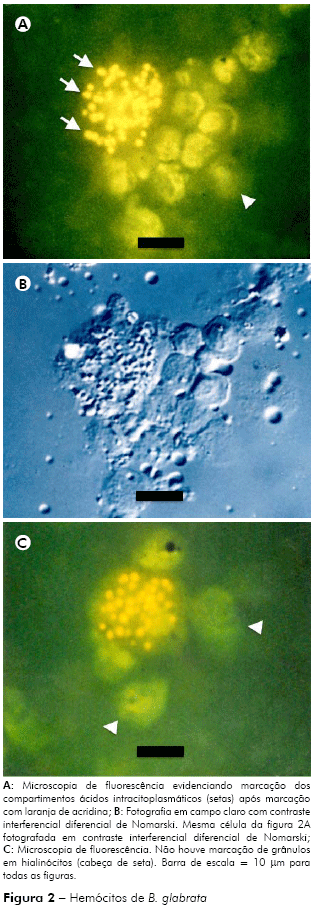
Como resultado da técnica de citoquímica ultraestrutural para detecção da atividade da enzima fosfatase ácida, foi possível observar a presença de depósitos eletrodensos em vesículas citoplasmáticas de dimensões variadas (2,20 ± 0,55 μm2; máximo: 3,49 μm2; mínimo: 1,45 μm2; n = 31) (Figuras 2A e 2C) resultantes desta reação (setas). Dentro destas vesículas também foram identificados subcompartimentos, com depósitos eletrodensos de aspecto granuloso, revestidos por membrana.
DISCUSSÃO
Estudos anteriores1,3,15,17,18,22,23 procuraram explicar a ação fagocitária dos dois tipos celulares (hialinócitos e granulócitos) responsáveis pela defesa do caramujo contra a cercária do S. mansoni6,8,9,10,13,24. Outros estudos25,26 têm procurado atribuir aos granulócitos a produção de enzimas hidrolíticas27,28, enquanto que nos hialinócitos (obtidos a partir de Crassostrea virginica e Mercenaria mercenaria) foi demonstrado apenas que estes são capazes de fagocitar bactérias in vitro25,26.
Poucos estudos procuraram demonstrar o local de produção da fosfatase ácida em hemócitos de caramujos infectados ou não infectados utilizando técnicas citoquímicas14,15,16,28. Já havia sido observado que a fosfatase alcalina apresentou níveis mais elevados na hemolinfa de moluscos infectados16,19; entretanto, não foi demonstrada a localização dessa enzima nos hemócitos. Em outros estudos desenvolvidos na hemolinfa de B. glabrata não infectados foi constatada a presença de seis enzimas cuja origem foi atribuída apenas aos lisossomos celulares24. No presente trabalho, portanto, foi possível mostrar a existência dessas enzimas e sua localização em caramujos infectados e não infectados.
A identificação de compartimentos ácidos citoplasmáticos, utilizando-se a técnica de laranja de acridina21, sugere a presença de lisossomos celulares em granulócitos de B. glabrata, e os experimentos de citoquímica ultraestrutural confirmam a presença da fosfatase ácida nesses compartimentos (Figura 2). Outro dado extraído dos resultados foi a ausência de marcação de grandes compartimentos ácidos em células com características de hialinócitos, o que poderia representar uma forma de distinção entre estes tipos celulares de hemócitos.
Na figura 3 observam-se depósitos eletrodensos localizados no interior de grânulos citoplasmáticos de hemócitos de B. glabrata, cujas características morfológicas apontam para um granulócito. Observam-se, em ambos os casos (Figuras 3A e 3B), que os grânulos marcados com a presença da enzima (depósitos eletrodensos) apresentam características morfológicas de estruturas membranosas (Figura 3A) e também de estruturas formadas por pequenos subcompartimentos (Figura 3B). A figura 3C mostra os depósitos eletrodensos fotografados em grande aumento.
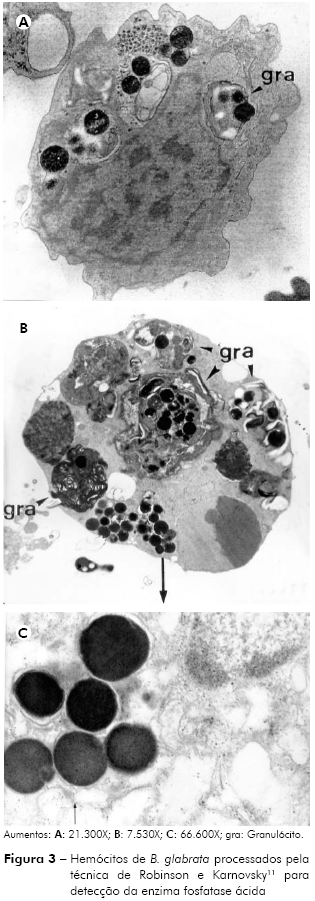
Os resultados ultraestruturais obtidos corroboram com trabalhos precedentes8,11,14,15,16,24, que também demonstraram a atividade de fosfatase ácida em hemócitos de B. glabrata.
CONCLUSÃO
Com este trabalho demonstra-se a presença de grandes lisossomos em hemócitos granulócitos de caramujo da espécie B. glabrata, pela identificação de compartimentos ácidos contendo a enzima fosfatase ácida. Estas organelas apresentaram grânulos envoltos por membrana com formas e disposições variadas por todo o citoplasma celular.
REFERÊNCIAS
1 Bayne CJ, Buckley PM, DeWan PC. Macrophagelike hemocytes of resistant Biomphalaria glabrata are cytotoxic for sporocysts of Schistosoma mansoni in vitro. J Parasitol. 1980 Jun;66(3):413-9.
2 Bayne CJ, Hahn UK, Bender RC. Mechanisms of molluscan host resistance and of parasite strategies for survival. Parasitology. 2001 Nov;123(7):159-67. Doi: 10.1017/S0031182001008137 [Link]
3 Foley DA, Cheng TC. A quantitative study of phagocytosis by hemolymph cells of the pelecypods Crassostrea virginica and Mercenaria mercenaria. J Invertebr Pathol. 1975 Mar;25(2):189-97. Doi:10.1016/0022-2011(75)90068-3 [Link]
4 Maramorosch K, Shope RE, editors. Invertebrate immunity. New York: Academy Press; 1975.
5 Jeong KH, Heyneman D. Leukocytes of Biomphalaria glabrata: morphology and behavior of granulocytic cells in vitro. J Invertebr Pathol. 1976 Nov;28(3):357-62. Doi:10.1016/0022-2011(76)90011-2 [Link]
6 Cheng TC, Chorney MJ, Yoshino TP. Lysozymelike activity in the hemolymph of Biomphalaria glabrata challenged with bacteria. J Invertebr Pathol. 1977 Mar;29(2):170-4.
7 Cheng TC, Dougherty WJ. Ultrastructural evidence for the destruction of Schistosoma mansoni sporocysts associated with elevated lysosomal enzyme levels in Biomphalaria glabrata. J Parasitol. 1989 Dec;75(6):928-41.
8 Cheng TC, Garrabrant TA. Acid phosphatase in granulocytic capsules formed in strains of Biomphalaria glabrata totally and partially resistant to Schistosoma mansoni. Int J Parasitol. 1977 Dec;7(6):467-72. Doi:10.1016/0020-7519(77)90008-X [Link]
9 Kassim OO, Richards CS. Schistosoma mansoni: lysozyme activity in Biomphalaria glabrata during infection with two strains. Exp Parasitol. 1978 Dec;46(2):213-7. Doi:10.1016/0014-4894(78)90133-9 [Link]
10 Kassim OO, Richards CS. Biomphalaria glabrata: lysozyme activities in the hemolymph, digestive gland, and headfoot of the intermediate host of Schistosoma mansoni. Exp Parasitol. 1978 Dec;46(2):218-24. Doi:10.1016/0014-4894(78)90134-0 [Link]
11 Robinson JM, Karnovsky MJ. Ultrastructural localization of several phosphatases with cerium. J Histochem Cytochem. 1983 Oct;31(10):1197-208. Doi: 10.1177/31.10.6309949 [Link]
12 Rodrick GE, Cheng TC. Activities of selected hemolymph enzymes in Biomphalaria glabrata (Mollusca). J Invertebr Pathol. 1974 Nov;24(3):374-5. Doi: 10.1016/0022-2011(74)90146-3 [Link]
13 Cheng TC, Butler MS. Experimentally induced elevations in acid phosphatase activity in hemolymph of Biomphalaria glabrata (Mollusca). J Invertebr Pathol. 1979 Sep;34(2):119-24. Doi:10.1016/0022-2011(79)90090-9 [Link]
14 Dingle JT, Dean R, editors. Lysosomes in biology and pathology. Amsterdam: Elsevier; 1975.
15 Harris KR. The fine structure of encapsulation in Biomphalaria glabrata. Ann N Y Acad Sci. 1975 Nov;266:446-64. Doi: 10.1111/j.1749-6632.1975.tb35123.x [Link]
16 Reuck AVS, Cameron MP. Lysosomes. London: J & A Churchill; 1963.
17 Matricon-Gondran M, Letocart M. Internal defenses of the snail Biomphalaria glabrata: I. Characterization of hemocytes and fixed phagocytes. J Invertebr Pathol. 1999 Nov;74(3):224-34. Doi: 10.1006/jipa.1999.4876 [Link]
18 Abdul-Salam JM, Michelson EH. Biomphalaria glabrata amoebocytes: effect of Schistosoma mansoni infection on in vitro phagocytosis. J Invertebr Pathol. 1980 May;35(3):241-8. Doi: 10.1016/0022-2011(80)90157-3 [Link]
19 Michelson EH, Dubois L. Increased alkaline phosphatase in the tissues and hemolymph of the snail Biomphalaria glabrata infected with Schistosoma mansoni. Comp Biochem Physiol B. 1973 Mar;44(3):763-7.
20 Stumpf JL, Gilbertson DE. Differential leukocytic responses of Biomphalaria glabrata to infection with Schistosoma mansoni. J Invertebr Pathol. 1980 Mar;35(2):217-8. Doi: 10.1016/0022-2011(80)90189-5 [Link]
21 Wasley GD, May JW. Animal cell culture methods. Philadelphia: Lippincott-Raven; 1971.
22 van der Knaap WP, Loker ES. Immune mechanisms in trematode-snail interactions. Parasitol Today. 1990 Jun;6(6):175-82. Doi: 10.1016/0169-4758(90)90349-9 [Link]
23 Sapp KK, Loker ESA. Comparative study of mechanisms underlying digenean-snail specificity: in vitro interactions between hemocytes and digenean larvae. J Parasitol. 2000 Oct;86(5):1020-9. Doi: 10.1645/0022-3395(2000)086[1020:ACSOMU]2.0.CO;2 [Link]
24 Cheng TC. Functional morphology and biochemistry of molluscan phagocytes. Ann N Y Acad Sci. 1975 Nov;266:343-79. Doi: 10.1111/j.1749-6632.1975.tb35116.x [Link]
25 Gress FM, Cheng TC. Alterations in total serum proteins and protein fractions in Biomphalaria glabrata parasitized by Schistosoma mansoni. J Invertebr Pathol. 1973 Nov;22(3):382-90. Doi:10.1016/0022-2011(73)90169-9 [Link]
26 Stumpf JL, Gilbertson DE. Hemocytes of Biomphalaria glabrata: factors affecting variability. J Invertebr Pathol. 1978 Sep;32(2):177-81. Doi:10.1016/0022-2011(78)90027-7 [Link]
27 Barracco MA, Steil AA, Gargioni R. Morphological characterization of the hemocytes of the pulmonate snail Biomphalaria tenagophila. Mem Inst Oswaldo Cruz. 1993 Jan-Mar;88(1):73-83. Doi: 10.1590/S0074-02761993000100012 [Link]
28 Yoshino TP, Cheng TC. Experimentally induced elevation of aminopeptidase activity in hemolymph cells of the American oyster, Crassostrea virginica. J Invertebr Pathol. 1976 May;27(3):367-70. Doi:10.1016/0022-2011(76)90098-7 [Link]
 Correspondência / Correspondence / Correspondencia:
Correspondência / Correspondence / Correspondencia:
Daniel Valle Vasconcelos Santos
Laboratório de Biologia e Eletrofisiologia em Células Parasitárias
Instituto Evandro Chagas
Rodovia BR 316, km 7, s/n°.
Bairro: Levilândia CEP: 67030-000
Ananindeua-Pará-Brasil
Tel.: +55 (91) 3214-2055
E-mail: danielsantos@iec.pa.gov.br
Recebido em / Received / Recibido en: 27/5/2014
Aceito em / Accepted / Aceito en: 24/11/2014













