INTRODUÇÃO
As infecções do trato urinário estão entre as doenças infecciosas mais comuns que acometem a população1. Aproximadamente 60% das mulheres entre 18 e 24 anos de idade irão apresentar pelo menos uma infecção urinária sintomática durante a vida, sendo que 5% delas apresentarão episódios recorrentes2.
Os principais microrganismos relacionados às infecções do trato urinário são as enterobactérias, destacando-se a Escherichia coli, considerada o agente etiológico mais prevalente, responsável por 80% das infecções. Outros uropatógenos comuns são Staphylococcus saprophyticus (15%), seguido de Klebsiella, Proteus, Enterobacter, Pseudomonas e Serratia. Ainda estão envolvidos os cocos Gram-positivos, como Enterococcus, Staphylococcus aureus e Streptococcus agalactiae3.
Além desses, os microrganismos do gênero Mycoplasma e Ureaplasma apresentam importância clínica, pois são responsáveis pelo desenvolvimento de várias doenças, principalmente geniturinárias e respiratórias4. Pertencem à classe Mollicutes e se caracterizam por serem os menores organismos capazes de autorreplicação, possuindo genoma reduzido e ausência de parede celular5. Esse fato leva a não suscetibilidade desses microrganismos aos antibióticos que atuam em nível de parede celular. A infecção por esses agentes está associada à imunodepressão, obstrução ou instrumentação urinária prévia6.
As espécies Mycoplasma hominis e Ureaplasma urealyticum são as principais causadoras de infecções urogenitais entre os micoplasmas7. U. urealyticum está associada a uretrites não gonocócicas. Já a espécie M. hominis foi isolada de pacientes com pielonefrite aguda, correlacionada também à doença inflamatória pélvica, a vaginoses bacterianas e, em gestantes, a abortos espontâneos, a partos prematuros e à febre pós-parto8. Além dessas, a espécie Mycoplasma genitalium foi relatada como causadora de uretrite em homens e cervicite mucopurulenta em mulheres9.
Devido aos problemas associados à terapêutica de diversas infecções, principalmente a resistência aos antibióticos, substâncias oriundas de vegetais têm adquirido novas perspectivas, como o aumento do interesse do seu uso na busca de compostos antimicrobianos10,11.
O uso de plantas para curar ou combater doenças é muito antigo12, sendo ainda uma prática muito presente no cotidiano da população. Segundo dados da Organização Mundial da Saúde, cerca de 65 a 80% da população mundial não têm acesso ao atendimento primário de saúde e recorre à medicina tradicional, especialmente às plantas medicinais, na procura de alívio para muitas doenças10.
Estudos demonstraram que as plantas, incluindo aquelas de uso popular, produzem metabólitos ativos, que apresentam atividades antibacteriana, anti-helmíntica, antifúngica, antiviral, anti-inflamatória, antioxidante, dentre outras11, descobertas essas que tornaram as plantas uma das fontes para o desenvolvimento de novos fármacos13.
O gênero Alternanthera (Amaranthaceae) é formado por 80 espécies, amplamente distribuídas pelo mundo, sendo que 25% delas são encontradas no Brasil14. São plantas nativas das regiões litorânea e Amazônica. A espécie Alternanthera brasiliana (L.) Kuntze é comumente conhecida como "penicilina", "terramicina" ou "doril" e é utilizada na medicina tradicional para o tratamento de diarreia, cistite, infecções de garganta e gerais15,16. A infusão de suas folhas é considerada diurética, digestiva, depurativa, sendo empregada para moléstias do fígado e da bexiga17.
Já o gênero Phyllanthus (Phyllanthaceae), conhecido popularmente como "quebra-pedra", é encontrado no Brasil, em toda a região tropical17. As plantas desse gênero, especialmente a Phyllanthus niruri L., são recomendadas pela medicina popular para o tratamento de problemas renais, gastroenterites, infecções geniturinárias, hepatite B e diabete11,12,14,17,18,19.
Plantago major L. (Plantaginaceae), também conhecida como "tansagem", é uma erva pequena, nativa da Europa e naturalizada em todo o sul do Brasil17. Estudos etnofarmacológicos mostraram que P. major é utilizada no tratamento de inúmeras patologias, como doenças de pele, infecções, problemas digestivos, respiratórios, circulatórios, entre outros20.
Arctostaphylos uva-ursi (L.) Spreng. pertence à família Ericaceae e é usada, principalmente, como antisséptico, anti-inflamatório e no tratamento de infecções do trato urinário, como cistite, uretrite, disúria e pielonefrite. Essa planta foi introduzida, na prática médica, na região da Europa, e continua sendo um dos mais comuns e importantes desinfetantes do trato urinário, no que se refere às ervas medicinais. Seu principal componente medicinal ativo é o arbutin, um glicosídeo fenólico que gera hidroquinona como resultado da glicólise, sendo que uma pequena quantidade de hidroquinona livre é encontrada nas folhas. Ácido p-cumárico e ácido cafeico, também encontrados na espécie, são componentes com propriedades antibacterianas e ácido salicílico, conhecido pela sua ação anti-inflamatória e bacteriostática21.
Diante desse contexto, os objetivos deste trabalho foram avaliar a atividade antibacteriana de A. brasiliana, P. major, A. uva-ursi e P. niruri, plantas medicinais de uso popular, frente a diferentes espécies de bactérias causadoras de infecções urogenitais, bem como analisar seus perfis cromatográficos. É importante ressaltar que este é o primeiro trabalho que avalia a atividade antimolicute dessas espécies.
MATERIAIS E MÉTODOS
MATERIAL VEGETAL
Partes aéreas da espécie A. brasiliana foram coletadas em casas de de moradores do bairro Água Verde, na cidade de Blumenau, estado de Santa Catarina, Brasil. Após a identificação, um exemplar foi arquivado no Herbário Dr. Roberto Miguel Klein, da Universidade Regional de Blumenau, sob o número de registro 36295. As demais espécies vegetais, P. major (Lote: 0040), A. uva-ursi (Lote: 0024) e P. niruri (Lote: 0050), da marca NatuBlu, foram adquiridas comercialmente em uma farmácia de dispensação, no centro de Blumenau, na forma de planta in natura.
Quanto à preparação dos extratos e frações vegetais, a espécie A. brasiliana foi submetida à secagem em temperatura ambiente e, em seguida, moída em moinho de facas. As demais espécies, adquiridas secas, também foram moídas em moinho de facas. Os produtos obtidos foram macerados com solução hidroalcoólica 70% durante sete dias. Em seguida, os extratos foram filtrados e concentrados em um evaporador rotatório sob pressão, reduzidos à temperatura de 45 ºC, sem necessidade de liofilização. Os extratos obtidos foram submetidos ao processo de partição líquido-líquido com solventes de diferentes polaridades, a fim de se obterem as frações diclorometano (DCM), acetato de etila (AcOEt), n-butanol (BuOH) e aquosa (Aq) de cada amostra.
ANÁLISE CROMATOGRÁFICA
Os extratos e frações submetidos à análise em cromatografia de camada delgada (CCD) e foram selecionados de acordo com os valores da concentração inibitória mínima (CIM), de modo a correlacionar os perfis cromatográficos com a atividade antibacteriana evidenciada. Os padrões cromatográficos de A. uva-ursi e P. niruri foram selecionados de acordo com os marcadores de identificação dessas espécies, conforme a Farmacopeia Brasileira IV22; os de A. brasiliana, coforme o estudo de Pereira23; e os de P. major, segundo Braz et al.24. Cerca de 0,015 g das amostras e padrões foram pesados e diluídos em 1 mL de metanol, obtendo-se uma concentração final de 15 mg/mL de cada amostra.
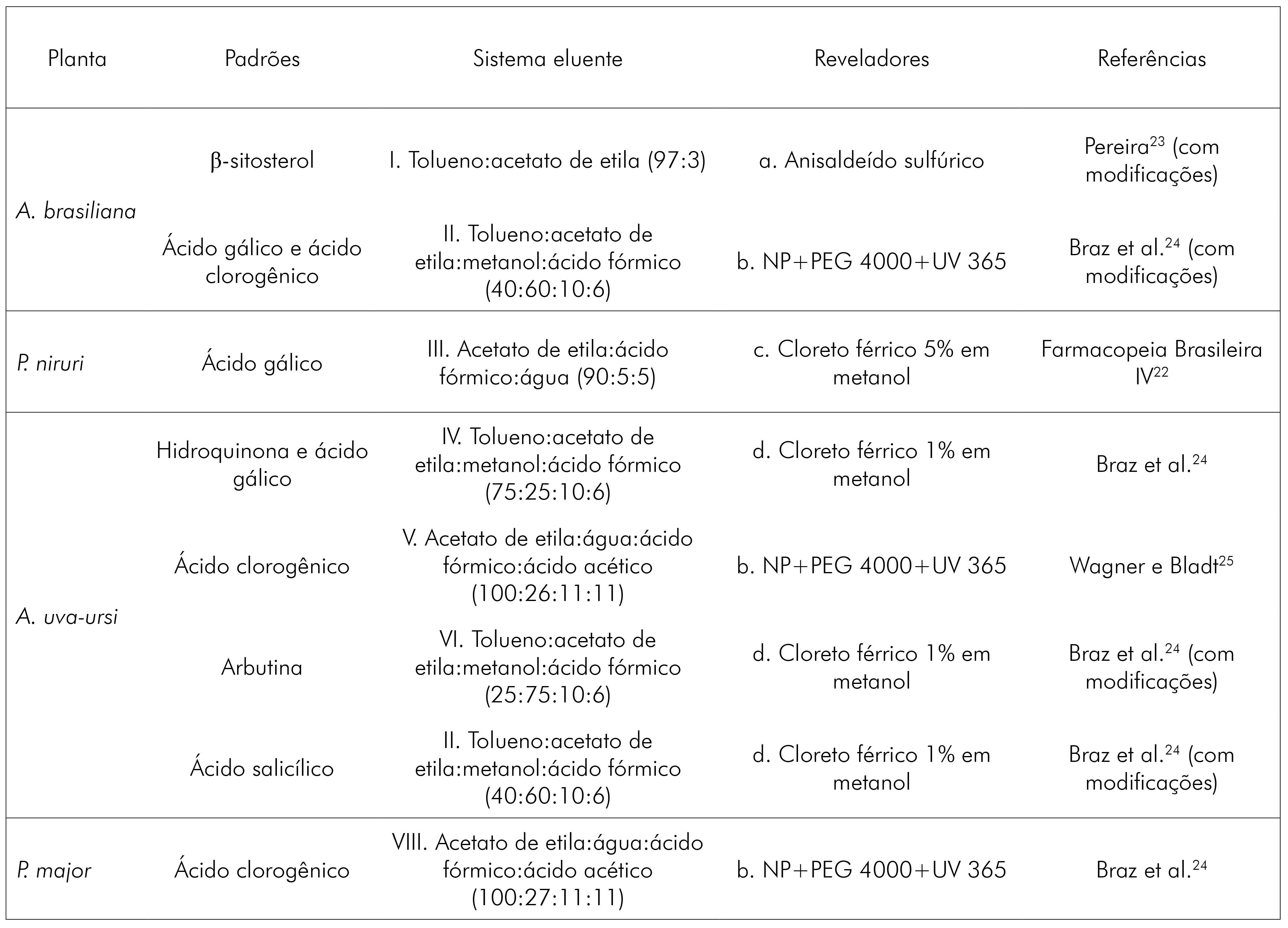
Foram utilizadas placas de sílica GF254, no tamanho de 6x8 cm, e cuba de saturação com migração ascendente. Alíquotas de 5 µL das amostras e padrões foram aplicadas nas placas, com o auxílio de um pipetador automático. Os sistemas de eluentes e os agentes cromogênicos utilizados neste estudo foram selecionados de acordo com informações obtidas previamente da literatura e encontram-se descritos no quadro 1.
ATIVIDADES BIOLÓGICAS
Foram utilizadas cepas de referência de molicutes, como M. genitalium (ATCC 33530), M. hominis (ATCC 23114), U. urealyticum (ATCC 27618), e cepas de E. coli (ATCC 25922), S. aureus (ATCC 25923), Proteus mirabilis (ATCC 25933), Klebsiella pneumoniae (ATCC 13883) e S. saprophyticus (ATCC 15305).
As cepas de molicutes foram cultivadas no Laboratório de Pesquisa em Bioanálises da Universidade de Blumenau, de acordo com Taylor-Robinson26, com modificações. As bactérias com parede celular E. coli, S. aureus, P. mirabilis, K. pneumoniae e S. saprophyticus foram cultivadas em meio ágar-sangue e incubadas em estufa a 35 ºC, por 24 h, na presença de oxigênio.
As amostras foram dissolvidas em água estéril, com 10% de dimetilsulfóxido (DMSO), e testadas pelo do método de microdiluição, na concentração inicial de 2 mg/mL, frente às cepas de bactérias.
A determinação da atividade antimicrobiana contra bactérias sem parede celular foi testada pelo método da microdiluição em caldo com os extratos e frações vegetais, conforme metodologia proposta por Bebear e Robertson27, com modificações. Em uma placa de microtitulação estéril de fundo chato com 96 poços, foi realizada uma diluição seriada dos extratos e frações das plantas, na qual, em 100 µL de meio líquido de arginina (MLA), SP4 ou meio líquido de ureia (U10), foram adicionados 100 µL das amostras, individualmente, procedendo-se a uma série de diluições (diluídos em razão 2). A essas diluições, foram adicionados 100 µL de um inóculo de cultura de molicutes em fase log de crescimento, contendo 103 microrganismos/mL. Como controle negativo, foi feita uma diluição seriada do próprio solvente (DMSO), sem extrato de planta; e, como controle de viabilidade da cepa, foi feita uma diluição seriada da cultura de microrganismo, sem a adição de solvente ou de extrato de planta. Por fim, foram adicionadas, em cada poço, de duas a três gotas de vaselina, de modo a isolar os microrganismos do meio externo e criar um ambiente de microaerofilia. As placas foram incubadas a 37 ºC por no mínimo 48 h, e o crescimento foi observado, a olho nu, pela mudança de coloração do meio, devido à presença do indicador vermelho de fenol. A CIM foi determinada como sendo a concentração correspondente ao poço anterior àquele onde foi possível verificar a mudança de coloração.
A determinação da atividade antimicrobiana contra bactérias com parede celular foi testada pelo método da microdiluição em caldo com os extratos e frações vegetais, conforme o Clinical and Laboratory Standards Institute28. A CIM foi determinada como sendo a concentração correspondente ao poço anterior àquele onde foi possível se verificar a formação do "botão".
Para a análise dos resultados de atividade antibacteriana, levou-se em consideração o parâmetro estabelecido por Machado et al.29: para extratos de plantas e frações, são considerados ativos valores de CIM abaixo de 100 μg/mL; moderadamente ativos, valores entre 100 e 500 μg/mL; fracamente ativos, valores entre 500 e 1.000 μg/mL; e, acima de 1.000 μg/mL, os extratos e frações foram considerados inativos.
RESULTADOS
Os resultados da obtenção dos extratos hidroalcoólicos (EH) e das frações estão apresentados na tabela 1. Conforme os perfis cromatográficos das plantas avaliadas (Figura 1), a A. brasiliana demonstrou, nas frações DCM e AcOEt, manchas que se assemelham ao padrão β-sitosterol, quando revelados com anisaldeído sulfúrico (Figura 1A). As manchas dos padrões testados não foram observadas no extrato hidroalcoólico e nas frações dessa espécie (Figura 1B). Conforme o cromatograma exposto na figura 1C, a fração DCM de A. uva-ursi apresentou uma mancha característica para terpenos; enquanto o extrato hidroalcoólico e as frações AcOEt e BuOH apresentaram manchas similares ao padrão ácido gálico, quando revelados com cloreto férrico 1% em metanol. Para a mesma espécie, os padrões ácido clorogênico e ácido salicílico não foram observados, conforme o perfil cromatográfico revelado nas figuras 1E e 1F. As frações AcOEt e BuOH de P. niruri demonstraram manchas características de compostos fenólicos (Figura 1G), assim como para o extrato hidroalcoólico e a fração AcOEt de P. major (Figura 1H).
Tabela 1 - Rendimento do extrato hidroalcoólico e frações obtidos das espécies vegetais analisadas
| Extrato/ Frações | Espécies vegetais | |||||||
| A. brasiliana | P. niruri | P. major | A. uva-ursi | |||||
| Peso (g) | Rendimento (%) | Peso (g) | Rendimento (%) | Peso (g) | Rendimento (%) | Peso (g) | Rendimento (%) | |
| EH* | 196,40 | 9,87 | 124,87 | 17,09 | 194,93 | 18,44 | 144,49 | 22,11 |
| DCM† | 0,44 | 2,86 | 1,10 | 6,33 | 0,26 | 0,82 | 1,77 | 6,34 |
| AcOEt† | 0,18 | 1,17 | 1,24 | 7,17 | 0,32 | 1,01 | 8,35 | 29,89 |
| BuOH† | 0,94 | 6,10 | 3,45 | 19,87 | 4,10 | 12,83 | 6,04 | 21,61 |
| Aq† | 9,11 | 59,21 | 9,55 | 55,05 | 17,83 | 55,79 | 9,22 | 32,98 |
* O rendimento do extrato hidroalcoólico (EH), para cada espécie, foi calculado em relação à amostra pulverizada seca. † O rendimento das respectivas frações (DCM, AcOEt, BuOH, Aq) foi calculado em relação ao extrato hidroalcoólico utilizado no procedimento de partição.

A e B: Cromatogramas de A. brasiliana (AB); C, D, E e F: Cromatogramas de A. uva-ursi (AU); G: Cromatograma de P. niruri (PN);
H: Cromatogramas de P. major (PM).
Cromatogramas: A - (1) β-sitosterol, (2) Extrato hidroalcoólico AB, (3) Fração DCM AB, (4) Fração AcOEt AB, Eluente: I, Revelador: a. B - (5) Ácido gálico, (6) Ácido clorogênico, (2) Extrato hidroalcoólico AB, (3) Fração DCM AB, (4) Fração AcOEt AB, Eluente: II, Revelador: b. C - (7) Hidroquinona, (5) Ácido gálico, (8) Extrato hidroalcoólico AU, (9) Fração DCM AU, (10) Fração AcOEt AU, (11) Fração BuOH AU, (12) Fração Aq AU, Eluente: IV, Revelador: d. D - (13) Arbutina, (8) Extrato hidroalcoólico AU, (9) Fração DCM AU, (10) Fração AcOEt AU, (11) Fração BuOH AU, (12) Fração Aq AU, Eluente: VI, Revelador: d. E - (6) Ácido clorogênico, (8) Extrato hidroalcoólico, (9) Fração DCM AU, (10) Fração AcOEt AU, (12) Fração Aq AU, Eluente: V, Revelador: b. F - (14) Ácido salicílico, (8) Extrato hidroalcoólico AU, (9) Fração DCM AU, (10) Fração AcOEt AU, (11) Fração BuOH AU, (12) Fração Aq AU, Eluente: II, Revelador: d. G - (5) Ácido gálico (15), Extrato hidroalcoólico PN, (16) Fração DCM PN, (17) Fração AcOEt PN, (18) Fração BuOH PN, Eluente: III, Revelador: c. H - (6) Ácido clorogênico, (19) Extrato hidroalcoólico PM, (20) Fração DCM PM, (21) Fração AcOEt PM, Eluente: VIII, Revelador: b.
Figura 1 - Resultados da análise cromatográfica das espécies vegetais analisadas
Nos testes de microdiluição realizados frente às cepas bacterianas, verificou-se, de maneira geral, uma atividade antibacteriana muito semelhante entre os extratos e frações das diferentes espécies vegetais, merecendo destaque a atividade da fração AcOEt e extrato hidroalcoólico de A. uva-ursi, com CIM de 31,25 µg/mL e 125 µg/mL, respectivamente, frente à cepa de S. aureus, conforme demonstrado na tabela 2.
Tabela 2 - Resultados da avaliação de CIM das espécies vegetais analisadas frente a cepas bacterianas
| Plantas | Microrganismos | |||||||
| M. genitalium | M. hominis | U. urealyticum | E. coli | P. mirabilis | K. pneumoniae | S. aureus | S. saprophyticus | |
| A. brasiliana | CIM (µg/mL) | |||||||
| EH | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| DCM | >1.000 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| AcOEt | 1.000 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| BuOH | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| Aq | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| A. uva-ursi | CIM (µg/mL) | |||||||
| EBH | 500 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | 125 | 1.000 |
| DCM | 500 | 500 | 500 | >1.000 | >1.000 | >1.000 | 500 | 500 |
| AcOEt | 125 | 500 | 250 | 1.000 | 1.000 | >1.000 | 31,25 | 250 |
| BuOH | 1.000 | >1.000 | 1.000 | >1.000 | >1.000 | >1.000 | 500 | 1.000 |
| Aq | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| P. niruri | CIM (µg/mL) | |||||||
| EH | 500 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| DCM | 1.000 | 500 | 1.000 | >1.000 | >1.000 | >1.000 | 250 | 250 |
| AcOEt | 250 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | 500 | 500 |
| BuOH | 500 | >1.000 | 1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| Aq | 1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| P. major | CIM (µg/mL) | |||||||
| EH | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| DCM | 500 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | 1.000 | 1.000 |
| AcOEt | 1.000 | 1.000 | 1.000 | >1.000 | >1.000 | >1.000 | 1.000 | 1.000 |
| BuOH | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
| Aq | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 | >1.000 |
DISCUSSÃO
As plantas selecionadas nesta pesquisa são muito procuradas pela população como remédio no tratamento de infecções urinárias, porém nenhum estudo revelou ainda sua real atividade antimicrobiana contra cepas de molicutes.
De acordo com os rendimentos percentuais, observou-se que todas as espécies apresentaram alto rendimento da fração Aq, o que pode estar relacionado à presença majoritária de compostos glicosilados e polímeros30. Estudos cromatográficos sugerem que a espécie A. brasiliana apresentou menor complexidade química nas frações mais apolares, demonstrando um perfil quantitativo diferente, em comparação às espécies P. niruri e P. major. Percebe-se que essas últimas espécies apresentaram alto rendimento da fração BuOH, enquanto A. uva-ursi apresentou bom rendimento, tanto nas frações AcOEt como na BuOH.
A espécie A. brasiliana foi inativa, tanto para o extrato hidroalcoólico quanto para as diferentes frações testadas. Frente às cepas de molicutes, as frações DCM e AcOEt foram inativas (CIM = 1.000 μg/mL), exceto em relação à cepa de M. genitalium, que não teve seu crescimento inibido na presença da fração DCM. O extrato hidroalcoólico e as demais frações mostraram-se inativas. Nenhuma atividade inibitória foi evidenciada contra as diferentes espécies de bactérias com parede celular. Esse resultado vai de encontro ao evidenciado por Coutinho et al.31, que testaram o extrato etanólico das folhas de A. brasiliana contra cepas de E. coli, S. aureus e Pseudomonas aeruginosa, tendo sido também considerado inativo perante os parâmetros de Machado et al.29.
Vários estudos foram realizados na busca de efeitos antimicrobianos dessa espécie vegetal, uma vez que popularmente é conhecida como "penicilina". Entretanto, nenhum estudo foi realizado com bactérias sem parede celular (molicutes). Pereira et al.32 avaliaram o extrato hidroalcoólico e a fração AcOEt de A. brasiliana e encontraram valores de CIM = 1.250 μg/mL, contra S. aureus, e CIM > 2.500 μg/mL, contra E. coli e P. aeruginosa. Nenhuma atividade foi evidenciada frente ao fungo Saccharomyces cerevisiae, no qual o extrato hidroalcoólico foi fungistático e fungicida na concentração de 625 μg/mL.
A ausência de atividade antimicrobiana de A. brasiliana, relatada no presente estudo e em trabalhos anteriores, não corrobora os efeitos terapêuticos relatados pelo uso popular15,16,17. Esse fato pode ser explicado, provavelmente, por essa espécie não estar relacionada ao combate a microrganismos através de efeitos bacteriostático ou bactericida, mas sim por sua ação anti-inflamatória32. A análise fitoquímica qualitativa de diferentes extratos de A. brasiliana revelou a presença de compostos como carboidratos, alcaloides, saponinas, flavonoides, fenóis, taninos e proteínas33. Os polifenóis, flavonoide e ácidos fenólicos apresentam diversas funções, como atividade antioxidante, ação hormonal, estimulação enzimática e propriedades antibacterianas33,34. Além dessas, foram relatadas a ação anti-inflamatória e a presença de compostos com possível ação analgésica, o que contribuiria no alívio dos sintomas de processos infecciosos e poderia levar à ideia de uma possível ação antibacteriana33,35. Pode haver ainda a inibição da formação de biofilmes, devido a um impedimento da adesão desses microrganismos em superfícies biológicas, a exemplo do cranberry (Vaccinium macrocarpon)36. Os biofilmes correspondem a uma associação entre células bacterianas, formando uma matriz multicelular, que podem se aderir a superfícies biológicas e não biológicas. São sistemas complexos e dinâmicos, que apresentam um modo de crescimento protegido contra as defesas do hospedeiro, assim como da ação de antibióticos, além de permitir que os microrganismos sobrevivam em ambientes hostis37,38. Tais hipóteses poderiam justificar o uso dessa planta como medicamento pela população em processos infecciosos in vivo.
Em relação às bactérias com parede celular, a fração AcOEt de A. uva-ursi foi capaz de inibir o crescimento de S. aureus a uma concentração de 31,25 µg/mL, uma atividade excelente que corresponde ao melhor resultado deste trabalho. O extrato hidroalcoólico apresentou CIM = 125 µg/mL, seguido das frações DCM e BuOH com CIM = 500 µg/mL, caracterizando uma atividade moderada. Diante dos resultados, a fração AcOEt mostrou-se mais ativa em relação ao extrato hidroalcoólico e demais frações. Segundo estudos de Cechinel Filho e Yunes30, essa fração concentra um grande número de metabólitos secundários, como flavonoides, taninos, saponinas, ácidos triterpênicos e compostos fenólicos, entre eles a hidroquinona24. No entanto, acredita-se que alguns dos metabólitos secundários concentrados na fração AcOEt possam estar contribuindo para a melhor atividade. Além disso, o alto rendimento dessa fração pode ser um fato interessante para estudos posteriores39. Estudos in vitro, citados por Blumenthal et al.40, demonstraram que preparações à base de A. uva-ursi também têm atividade antibacteriana contra Proteus vulgaris, E. coli, U. urealyticum, M. hominis, S. aureus, P. aeruginosa, Enterococcus faecalis e Candida albicans.
Em relação à espécie P. niruri, a fração AcOEt apresentou atividade antibacteriana moderada, com valores de CIM = 250 µg/mL, frente à cepa M. genitalium. Contra S. aureus, as frações DCM e AcOEt apresentaram atividade antibacteriana moderada, com CIM = 250 µg/mL e 500 µg/mL, respectivamente. P. niruri tem demonstrado atividade antibacteriana in vitro contra Staphylococcus, Micrococcus e Pasteurella, bem como atividade antimalárica in vivo. Outras espécies do gênero, como P. burchellii e P. parvulus, apresentaram atividade contra E. coli, P. mirabilis, P. aeruginosa, Klebsiella oxytoca, Serratia marcescens e Bacillus subtilis (CIM ± 5 mg/mL)18. Em um trabalho de Sumathi e Parvathi41, a CIM do extrato das folhas de P. niruri foi de 50 µg/mL contra Salmonella enterica sorovar Typhi e S. aureus, resultados que justificam o uso popular dessa planta para tratamento de gastroenterites. A atividade antimicrobiana dos extratos etanólico e acetônico de P. niruri também foi testada pelo método de difusão em disco por Divya et al.42, que evidenciaram zonas de inibição efetivas dos extratos contra os isolados de Staphylococcus sp., E. coli, Pseudomonas sp. e Bacillus sp. Esse resultado se deve à presença de taninos, flavonoides e compostos fenólicos encontrados na espécie vegetal42. O extrato etanólico das folhas de P. niruri apresentou alta atividade contra K. pneumoniae (18 mm), P. aeruginosa (16 mm) e P. mirabilis (26 mm), sendo esse último superior ao controle positivo (23 mm)43.
P. major apresentou valores de CIM inativos contra as cepas testadas. Os resultados obtidos para a espécie se assemelham àqueles relatados na literatura, uma vez que evidências de atividade antimicrobiana só foram possíveis em extratos com alta concentração de compostos bioativos. Metiner et al.44 analisaram a atividade antimicrobiana, através do método de microdiluição, e verificaram que o extrato acetônico foi inativo contra Bacillus cereus, com CIM = 3.562 µg/mL, assim como frente às cepas de B. subtilis, P. mirabilis, P. aeruginosa e Staphylococcus epidermidis, com CIM = 28.500 µg/mL. O extrato etanólico também foi inativo contra E. coli e B. cereus na CIM = 12.500 µg/mL. Nos estudos de Okmen45, o extrato metanólico das folhas de P. major apresentou-se inativo (CIM = 1.625 µg/mL) contra diferentes cepas de S. aureus.
A análise cromatográfica mostrou que a espécie A. brasiliana apresenta um metabólito com Rf similar ao β-sitosterol (Rf = 0,17) nas frações DCM e AcOEt, com Rfs ~ 0,18, conforme demonstrado na figura 1A. Na composição dessa espécie, destacam-se os fitoesteróis, como estigmasterol, β-sitosterol e espinasterol. Tais substâncias são comumente encontradas nos vegetais, sendo que o estigmasterol e o β-sitosterol são os esteroides majoritários presentes nas membranas celulares das plantas. Estudos prévios realizados com o β-sitosterol demonstraram significativo efeito analgésico e anti-inflamatório32. Na figura 1B, não se observou a presença de compostos ativos similares ao ácido gálico (Rf = 0,56) e ao ácido clorogênico (Rf = 0,11), utilizados como padrões nas amostras analisadas. Outros trabalhos demonstram a presença de compostos fenólicos46 e flavonoides47, compostos esses conhecidos pelo seu efeito antibacteriano48.
Romm et al.21 sugeriram que a atividade antimicrobiana da espécie A. uva-ursi esteja relacionada à presença de arbutina e sua aglicona, a hidroquinona. Ainda, segundo a Farmacopeia Brasileira IV22, esses compostos são considerados padrões de qualidade para a identificação dessa espécie. Porém, de acordo com o perfil cromatográfico mostrado nas figuras 1C e 1D, não foi possível observar a presença de compostos similares à hidroquinona/Rf = 0,40 e à arbutina/Rf = 0,24 nas amostras analisadas. Essa planta destaca-se pelo alto teor de glicosídeos de fenóis simples, sendo o principal deles a arbutina, cujo teor varia de 6 a 10%48. Braz et al.24 demonstraram a presença de hidroquinona na fração AcOEt de A. uva-ursi por meio de CCD e nas mesmas condições de estudo do presente trabalho.
O baixo teor ou a ausência desses compostos nas espécies vegetais analisadas pode ser atribuído, por exemplo, à época do ano em que a planta foi coletada, aos procedimentos de secagem e armazenamento48, ou até mesmo por uma possível troca de espécie. Essa última hipótese foi descartada, pois a autenticidade das espécies foi confirmada por parâmetros da Farmacopeia Brasileira IV22. Outra hipótese pode estar relacionada à estabilidade dos compostos fenólicos, que são facilmente oxidáveis tanto por meio de enzimas vegetais específicas quanto por influência da luz e do calor. A hidroquinona, por exemplo, é um composto facilmente fotodegradável e apresenta alta reatividade química, podendo sofrer oxidação, dependendo das condições de temperatura, pH e presença de oxigênio no meio, além das formas de armazenamento, que não são apresentadas em amostras adquiridas comercialmente48,49. Ainda, ressalta-se a sensibilidade do método como um interferente. Na análise por CCD, os compostos identificados, normalmente, apresentam-se em maior quantidade nos vegetais (majoritários). Técnicas analíticas mais sensíveis podem auxiliar na detecção de compostos em minoritários presentes.
A espécie A. uva-ursi é caracterizada ainda pelo elevado teor de taninos, derivados do ácido gálico, podendo sua concentração ser superior a 10%48. Por tal motivo, foi pesquisada também a presença desse composto nas amostras, que, na metodologia empregada (Quadro 1), aparece em Rf = 0,12 (Figura 1C). A análise cromatográfica mostrou que um metabólito similar ao ácido gálico encontra-se presente no extrato hidroalcoólico, na fração DCM e AcOEt, podendo ser um dos fatores responsáveis pela atividade antibacteriana evidenciada na presente amostra. Além disso, não se verificou a presença de compostos similares ao ácido clorogênico (Rf = 0,55) e nem ao ácido salicílico (Rf = 0,74), compostos conhecidos por sua ação anti-inflamatória e bacteriostática21 (Figuras 1E e 1F, respectivamente).
O perfil cromatográfico de P. niruri está demonstrado na figura 1G. Os resultados revelaram a presença de um metabólito similar ao ácido gálico (Rf = 0,73) nas frações AcOEt e BuOH, o que pode ter contribuído para a atividade moderada evidenciada contra M. genitalium. A análise fitoquímica dessa planta, em estudos anteriores, registrou a presença de vários flavonoides, triterpenoides, lignanas, fenóis e taninos. Porém, ainda existem poucos estudos correlacionando a atividade da planta com uma única substância ou ao efeito sinérgico entre os diferentes constituintes17,18.
Os resultados do perfil cromatográfico de P. major estão demonstrados na figura 1H. É possível verificar uma mancha similar ao padrão de ácido clorogênico (Rf = 0,42), sugerindo a presença do metabólito no extrato hidroalcoólico e na fração AcOEt. Braz et al.24 evidenciaram a presença do ácido clorogênico e do ácido cafeico na fração AcOEt de P. major.
Devido aos poucos relatos na literatura sobre a ação de plantas medicinais contra espécies de molicutes e a busca por melhores resultados frente às bactérias com parede celular, os dados encontrados podem auxiliar na obtenção de moléculas farmacologicamente ativas e na elucidação do uso de plantas para fins terapêuticos, assim como a fração AcOEt de A. uva-ursi, que apresentou uma atividade antibacteriana excelente (31,25 μg/mL) frente à cepa de S. aureus.
CONCLUSÃO
Não foi possível estabelecer uma estreita relação entre o uso popular, a atividade antibacteriana in vitro e o perfil fitoquímico das plantas, uma vez que os efeitos antibacterianos das espécies vegetais estudadas variaram frente às diferentes espécies de bactérias, e, na maioria dos casos, foram considerados inativos. Os resultados deste estudo ressaltaram que a espécie A. brasiliana, apesar de ser conhecida popularmente como "penicilina", um potente antibiótico da classe dos β-lactâmicos, não possui qualquer atividade antibacteriana contra as cepas testadas in vitro.
Outro resultado relevante foi que a fração AcOEt, obtida de A. uva-ursi, demonstrou uma excelente atividade contra S. aureus, o que, segundo dados da literatura, deveria estar relacionado à presença de compostos como arbutina e hidroquinona. Porém, em análise cromatográfica, os compostos não foram encontrados, sugerindo, assim, a existência de mais compostos responsáveis por essa atividade.










 texto en
texto en