Triagem neonatal da infecção pelo Trypanosoma cruzi em Minas Gerais, Brasil: transmissão congênita e mapeamento das áreas endêmicas*
Neonatal screening program for the infection by Trypanosoma cruzi in Minas Gerais, Brazil: Congenital transmission and tracking of the endemic areas
Eliane Dias GontijoI; Gláucia Manzan Queiroz de AndradeII; Silvana Eloi SantosIII; Lúcia Maria da Cunha GalvãoIV; Eliana Furtado MoreiraV; Fabiane Scalabrini PintoII; João Carlos Pinto DiasVI; José Nélio JanuárioVII
IDepartamento de Medicina Preventiva e Social, Faculdade de Medicina, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil
IIDepartamento de Pediatria Setor de Infectologia Pediátrica, Faculdade de Medicina, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil ]]>
IIIDepartamento de Propedêutica Complementar, Faculdade de Medicina, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil
IVDepartamento de Parasitologia, Instituto de Ciências de Biológicas, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil. Programas de Pós-Graduação em Ciências da Saúde e Ciências Farmacêuticas, Universidade Federal do Rio Grande do Norte, Natal-RN, Brasil
VFundação Ezequiel Dias, Secretaria do Estado de Saúde de Minas Gerais, Belo Horizonte-MG, Brasil
VICentro de Pesquisas René Rachou, Fundação Instituto Oswaldo Cruz, Belo Horizonte-MG, Brasil
VIIDepartamento de Clínica Médica, Núcleo de Ações e Pesquisa em Apoio Diagnóstico, Faculdade de Medicina, Universidade Federal de Minas Gerais, Belo Horizonte-MG, Brasil
RESUMO
No Brasil, uma vez controlada a transmissão pelas vias vetorial e transfusional, a via vertical adquiriu maior importância na transmissão da doença de Chagas (DC). A alta possibilidade de cura da doença de Chagas congênita (DCC) faz com que seu diagnóstico seja imperativo. Visando definir o risco de transmissão vertical e mapear áreas de risco, realizou-se inquérito sorológico em 63.673 neonatos do Programa de Triagem Neonatal de Minas Gerais. A prevalência de DC em puérperas foi 0,5% (IC95% 0,37-0,54) e, as prevalências mais elevadas foram observadas na região norte do estado, variando de 2,3% a 23%. O risco de transmissão vertical foi 0,2% (IC95% 0,00-0,55) e a incidência de DCC foi 1,6 em cem mil nascidos vivos (IC95% 0,00-5,00). A sorologia demonstrou ser eficiente ferramenta para o diagnóstico da DCC, e propõe-se que deva ser incluída no Programa de Triagem Neonatal nas áreas consideradas endêmicas. No estudo, a IgG materna persistiu positiva, em 17 crianças, entre seis e nove meses de idade. Portanto, filhos assintomáticos de mães chagásicas devem ser submetidos à sorologia após seis meses e, se positiva, deve ser repetida aos nove meses, antes de intervenção terapêutica.
]]> Palavras-chave: Doença de Chagas; Trypanosoma cruzi; infecção congênita; epidemiologia; Minas Gerais.SUMMARY
In Brazil, once vectoral and transfusional transmissions are under control, congenital transmission of Chagas disease has become the main form. Treatment of congenital infection is often successful, so early detection becomes a relevant issue of public health. To determine the risk of congenital Chagas disease (CCD), were studied 63. 673 newborns enrolled at Neonatal Screening Program, at Minas Gerais, Brazil. The prevalence of Chagas disease in pregnant women was 0.5%(IC95% 0,37-0,54), varying from 2,3 to 23%, with higher rates found in the northern state region. Transmission risk was estimated at 0.2%(IC95% 0,00-0,55) leading to an incidence rate of 1.6 per 100,000 live births(IC95% 0,00-5,00) Serology survey was shown to be an efficient diagnostic tool, it should be included at neonatal screening programs in endemic areas. Asymptomatic children from infected mothers should be tested at six months of age, and if positive, serology should be repeated at nine months of age, before initiating therapeutic interventions.
Key words: Chagas disease; Trypanosoma cruzi; congenital infection; epidemiology; Minas Gerais State.
Introdução
A doença de Chagas é uma parasitose causada pelo Trypanosoma cruzi que atinge 13 milhões de indivíduos nas Américas Central e do Sul.1 No Brasil, o número de infectados situa-se em torno de três milhões, dos quais aproximadamente 600 mil residem em Minas Gerais.2 Em 2001, o Estado de Minas Gerais recebeu o certificado da Organização Pan-Americana da Saúde (OPAS) da Organização Mundial da Saúde (OMS) de eliminação do Triatoma infestans, vetor do parasito que, por ser domiciliado, foi o principal responsável pela expansão da endemia.2 Com o controle do principal vetor e da transmissão transfusional, outros mecanismos de transmissão da doença de Chagas são colocados em evidência e, no momento, a via vertical (mãe-filho), no Brasil, passou a ser considerada uma das principais formas de transmissão da infecção chagásica. A prevalência da infecção por T. cruzi em gestantes, principal fator de risco para a infecção congênita, varia de 5 a 40% dependendo da área geográfica.3 No Brasil, oscila entre 0,3 e 33% e, em Minas Gerais, em 1997, a análise de 18.443 amostras de sangue do Programa Estadual de Triagem Neonatal (PETN) determinou o índice de 1% (175) de puérperas com doença de Chagas. Dentre as 175 mães chagásicas, foi confirmada a infecção congênita em três crianças, estimando o risco de transmissão em 1,7%.2 A principal via da transmissão vertical é a transplacentária e pode ocorrer em qualquer fase da doença materna: aguda ou crônica, em qualquer época da gestação, sendo mais provável no último trimestre, podendo ocorrer também no canal do parto, pelo contato das mucosas do feto com o sangue da mãe infectada.4
Os fatores relacionados com a transmissão congênita da doença de Chagas ainda são pouco conhecidos, mas sabe-se que a mãe pode transmitir o parasito em uma gestação e não transmitir na gestação seguinte.5 O grau de parasitemia e as características da população do parasito nas mães infectadas, fatores placentários, obstétricos, imunitários e de nutrição materna podem estar relacionados com esse mecanismo de transmissão.4,6
Na gravidez ocorre depressão transitória da imunidade mediada por células, importante na preservação do feto, que pode favorecer a infecção materna. Estudo realizado na Bolívia7 encontrou maior freqüência de hemoculturas positivas em mães que transmitiram o parasito para o feto, além de menor produção de interferon γ (IFN-γ), com associação significativa com a baixa idade materna (p=0,0043) e menor número de gestações anteriores (p=0,027).8
]]> A infecção materna pelo T. cruzi pode afetar o crescimento e a maturidade dos fetos infectados, predispondo ao abortamento, prematuridade, crescimento intra-uterino restrito (CIUR) e malformações fetais.5,6,9 Não há um perfil clínico único da doença de Chagas congênita, que varia desde ausência de sintomas em 50 a 90% dos casos até quadros graves,3,6 reforçando a necessidade do diagnóstico laboratorial.3,5,6,9,10A transmissão congênita deve ser considerada em crianças nascidas de mãe com sorologia positiva para T. cruzi, que apresentam exame parasitológico positivo ou naquelas com sorologia positiva após 6-8 meses, excluídos outros mecanismos de transmissão. O tratamento específico é considerado obrigatório em todos os casos de infecção congênita, pela alta eficácia e segurança.11 Como o tratamento das gestantes infectadas não é recomendado, em virtude da toxicidade da droga disponível, a estratégia para controle da doença de Chagas congênita se apóia no diagnóstico precoce das crianças infectadas e no controle sistemático e eficiente das vias de transmissão da infecção (principalmente vetorial e transfusional) em áreas endêmicas, com o objetivo de reduzir a prevalência das mulheres infectadas.3,12 A criança é suspeita de ter infecção se a mãe tem diagnóstico confirmado na gestação ou se o recém-nascido apresenta resultado positivo para IgG anti-T.cruzi em sangue periférico (triagem neonatal). Sabe-se que o transporte de IgG da mãe para o filho, através da placenta, se inicia em torno da 17a semana de gestação e, em torno da 33a semana, os níveis de IgG da mãe e do feto têm níveis equivalentes.13 Em 2005, o Consenso Brasileiro em doença de Chagas14 recomendou que a identificação da transmissão vertical de doença de Chagas em Saúde Pública deveria ser realizada pelo PETN, levando em consideração a existência de estrutura laboratorial, com ambulatório multidisciplinar especializado, rede assistencial complementar e sistema de informação automatizado em todos os estados. Minas Gerais conta com eficiente programa de triagem neonatal, executado pelo Núcleo Ações e Pesquisa em Apoio Diagnóstico (Nupad) da Faculdade de Medicina da Universidade Federal de Minas Gerais (FM/UFMG) e, nesse sentido, foi proposto o presente estudo, que visa estimar o risco de transmissão vertical da infecção pelo T. cruzi, por meio da realização de sorologia para doença de Chagas nas amostras de sangue de neonatos colhidas no programa de triagem neonatal, além de mapear as áreas de risco no Estado.
Metodologia
Desenho do estudo
O inquérito, iniciado em agosto de 2005, foi desenvolvido em duas etapas. A primeira, para definir a prevalência da infecção chagásica em puérperas no Estado de Minas Gerais, foi realizada em todos os 853 Municípios. Em cada Município foram colhidas amostras de sangue consecutivas equivalentes ao maior número entre a média mensal de nascimentos observada pelo Sistema de Informações de Nascidos Vivos (Sinasc) em 2004 e a média mensal de nascimentos observada pelo Nupad no mesmo ano, acrescidos de 5% e arredondado para cima. Assim que o número mínimo era atingido, a triagem no Município era interrompida. Apesar de não ter havido diferença significativa no número total de nascidos vivos em Minas Gerais nos períodos de 2004 e 2005, não pode ser descartada a possibilidade de algumas crianças nascidas em determinado Município durante o período da pesquisa não terem sido submetidas à triagem. Foram, então, calculados os intervalos com 95% de confiança para os coeficientes encontrados.
A segunda etapa foi desenhada de forma a favorecer a detecção de casos de infecção congênita na criança nascida de mãe com sorologia positiva em, pelo menos, dois testes com princípios diferentes,15 que apresentassem exames parasitológicos positivos a partir do nascimento ou exames sorológicos positivos após o sexto mês de vida em dois métodos diferentes, excluídas outras formas de transmissão da doença. Nesta etapa, a triagem foi expandida nos Municípios de endemicidade mais elevada do Estado, baseando-se nos dados de prevalência de puérperas com doença de Chagas obtidos na primeira fase desse trabalho e também nos dados obtidos em estudo piloto realizado no ano de 1997.2 Foram selecionadas as microrregiões com proporção de amostras alteradas pelo ELISA em papel filtro maior ou igual a 2,0%, além dos Municípios de Bambuí, Formiga, Curvelo e Carbonita, pela importância geográfica e histórica relacionada à doença de Chagas.
Para definição de infecção chagásica foi utilizado o critério da OMS que exige a positividade em pelo menos dois testes sorológicos de técnicas diferentes.15
Triagem sorológica dos neonatos para doença de Chagas
Triagem sorológica em amostras de sangue capilar seco em papel filtro
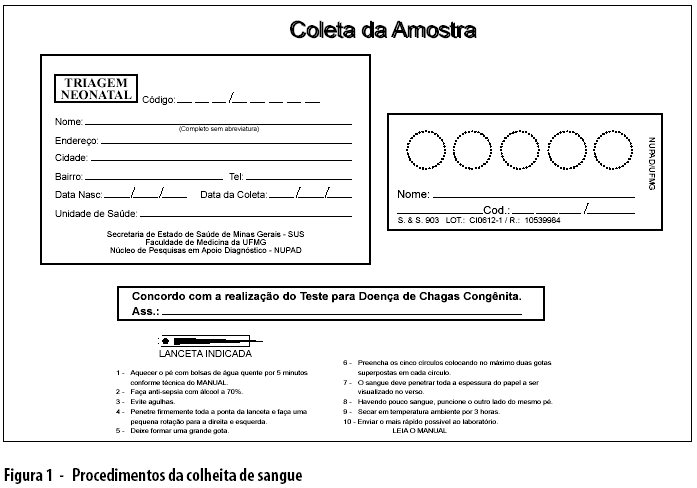
]]> Inicialmente, foram utilizadas amostras de sangue capilar de crianças entre o 5o e o 7o dias de vida. Tais amostras em papel filtro foram enviadas rotineiramente ao laboratório do Nupad, pelo PETN. No momento da coleta, foram anotados o código do centro de saúde, iniciais, registro da mãe e data de coleta. De cada recém-nascido foi colhida amostra de 1ml de sangue, suficiente para preencher cinco círculos de aproximadamente 1,0cm de diâmetro no papel filtro. Após secagem à temperatura ambiente, foram acondicionadas em sacos plásticos bem vedados, contendo sílica, colocadas em geladeira (4oC) e encaminhadas ao laboratório do Nupad. A partir da amostra contida no último círculo do papel foi realizado teste ELISA IgG (CHAGATEK ELISA® - Biomérieux) anti-T. cruzi (Figura 1). As amostras com títulos superiores a 0,6 foram consideradas positivas, e entre 0,4 e 0,6 indeterminadas. Todas as amostras reativas ou indeterminadas, além de 20% das amostras negativas alocadas aleatoriamente, foram submetidas à reação de Imunofluorescência Indireta-IFI (IFI - Doença de Chagas Bio-Manguinhos) como segundo teste no Laboratório de Referência do Estado na Fundação Ezequiel Dias (Funed). Os exames foram executados de modo independente pelos dois laboratórios. No caso de resultados discordantes entre as reações de ELISA e IFI, foi realizada a reação de Hemaglutinação indireta-HAI (HEMACRUZI® - Biomérieux) como terceiro teste.

Confirmação sorológica com testes de sorologia convencional em sangue venoso
Para confirmação dos resultados indeterminados ou positivos das amostras colhidas em papel filtro, uma segunda amostra de sangue venoso foi colhida até três meses após o nascimento. Para cada binômio mãe e filho, foram colhidos cerca de 6ml de sangue no centro de saúde do Município de residência. O soro centrifugado foi devidamente identificado, em tubo soro gel, acondicionado em saco plástico bem vedado e colocado em geladeira (4oC) até seu encaminhamento, em caixa de isopor, bem vedada, contendo gelo, ao laboratório da Funed, no prazo máximo de sete dias. Nesta segunda amostra foram realizados testes titulados de sorologia convencional: ELISA (ELISA - Doença de Chagas Bio-Manguinhos), IFI (IFI - Doença de Chagas Bio-Manguinhos) e HAI (HEMACRUZI® - Biomérieux).
Os testes selecionados mostram boa sensibilidade e especificidade. Estudo anterior estimara a concordância entre os resultados dos testes de ELISA, IFI e HAI em papel filtro e demonstrou acuidade de 98,3% e índice Kappa de 0,77.2 A razão entre as sensibilidades dos testes ELISA e IFI foi de 0,92 - IC95% (0,74; 1.13). Os resultados mostraram que o teste ELISA em sangue seco pode ser utilizado com a mesma segurança do teste IFI.16
Teste imunoenzimático por Western-blot para detecção de anticorpos anti-SAPA
O teste imunoenzimático por Western-blot utilizando TESA (antígenos excretados-secretados de tripomastigotas) de T. cruzi da cepa γ (TESA-blot)17 foi realizado nas primeiras 84 amostras encaminhadas. Reações positivas seriam aquelas com presença de bandas na região de massa molecular de 120-200 kDa, e reações negativas aquelas com ausência de tais bandas. Devido à complexidade do método e a negatividade de todos os testes realizados, optou-se por interromper a realização do exame.
]]> Exames parasitológicosReação em Cadeia da Polimerase (PCR)
Esta técnica foi realizada nas crianças que tiveram resultado positivo ou indeterminado em papel filtro e que colheram amostra para confirmação sorológica. Foram transferidos 2ml de sangue para tubos plásticos de 15ml, estéreis, contendo igual volume de Guanidina- HCl 6M/EDTA 0,2 M pH 8,018 e enviadas ao Laboratório de Biologia do Trypanosoma cruzi e doença de Chagas do Departamento de Parasitologia, ICB/UFMG. A extração do DNA foi realizada conforme descrita,19 em cada amostra de 2ml de sangue preservada em guanidina-EDTA, fervida em banho-maria durante 15 minutos, com o objetivo de promover a linearização dos minicírculos concatenados na rede de kDNA,20 permitindo uma distribuição homogênea das seqüências alvo presentes na amostra. Nas reações da PCR, as seqüências da região constante dos minicírculos da rede de kDNA do T. cruzi constituíram o alvo da reação, amplificando um fragmento de 330pb com os iniciadores 121 e 122.21 O programa de amplificação constou de uma desnaturação inicial a 95oC (5min) e de 35 ciclos com desnaturação a 95oC (1min), anelamento a 65oC (1min) e extensão a 72oC (1min) seguida de extensão final de 10 minutos em um termociclador MJ Research PTC-100.19 Os produtos da reação foram visualizados em géis de poliacrilamida a 6% corados pela prata.22
Hemocultura
Esta técnica foi realizada de acordo com Chiari e colaboradores23 no sangue de mães e filhos que compareceram para exames clínicos e avaliação pré e pós-terapêutica específica a partir de maio de 2006.
Conduta após resultado sorológico
Os resultados sorológicos positivos foram entregues pessoalmente pelo responsável pelo convênio do PETN em cada Município, e os resultados negativos foram encaminhados via correio. As crianças que apresentaram sorologia reativa em pelo menos dois testes diferentes foram examinadas pelo médico de referência do Município, juntamente com suas mães. Aquelas com quadro clínico sugestivo foram encaminhadas para avaliação no Ambulatório de Infectologia do Hospital das Clínicas da UFMG e Secreetaria Municipal de Saúde e Belo Horizonte-MG (Centro de Treinamento e Referência em Doenças Infecciosas e Parasitárias Orestes Diniz). As crianças com um ou dois testes positivos usando tecnologias diferentes que se mostraram assintomáticas e, com exames parasitológicos negativos, foram submetidas à nova colheita de sangue em papel filtro entre seis a oito meses após o nascimento e com sorologia reativa. Para a análise estatística foi utilizado o programa Access para entrada dos dados e, para a análise descritiva, o software EPI-INFO.
Considerações éticas
O projeto foi aprovado pelo Comitê de Ética em Pesquisa (COEP) da UFMG, ETIC 260/03. Foi solicitado o Consentimento Livre e Informado para a participação na pesquisa, conforme Resolução 196/96. Durante a colheita do sangue para o PETN, foi solicitado à mãe ou responsável que assinasse a concordância para realizar o exame para o diagnóstico da infecção chagásica impressa no envelope próprio, onde era armazenada a amostra individual para ser enviada ao laboratório do Nupad. Todas as mães das crianças receberam folha impressa contendo os resultados dos exames realizados, recomendações e atenção médica. Foram afixados cartazes em todos os postos de colheita do "Teste do Pezinho" e distribuídos folhetos informativos sobre a importância da pesquisa e seus objetivos. Todas as instituições participantes assinaram o Termo de Compromisso com a execução da pesquisa.
]]> Resultados
Triagem sorológica dos neonatos
O inquérito compreendeu a análise de 63.673 amostras colhidas durante 15 meses, no período de agosto de 2005 a outubro de 2006 em toda a área de abrangência do PETN-MG.
Etapa 1 – Inquérito epidemiológico para definição da prevalência da infecção chagásica em puérperas do Estado de Minas Gerais
Na primeira fase, realizada durante três meses, de agosto a outubro de 2005, foram triadas 24.969 crianças. Nesta etapa, a sorologia realizada pela técnica de ELISA resultou em 246 resultados positivos (1%), 36 indeterminados (0,1%) e 24.687 negativos (98,9%). Foram encaminhadas para a Funed, 5.260 amostras, que revelaram 126 reações positivas, 13 indeterminadas e 5.121 negativas pelo método de IFI. Destas, 5.236 amostras foram submetidas também à técnica de HAI com 77 permanecendo positivas, uma indeterminada e 5.158 negativas.
Na primeira fase, foram confirmados 113 (0,45%) casos positivos, 204 (0,82%) permaneceram indeterminados, 24.585 (98,7%) mantiveram-se negativos e 67 (0,27%) amostras foram inadequadas para o exame. A prevalência da doença de Chagas em puérperas no estado de Minas Gerais foi então estimada em 0,5% (IC95% 0,37-0,54).
Etapa 2 – Inquérito epidemiológico nos Municípios endêmicos
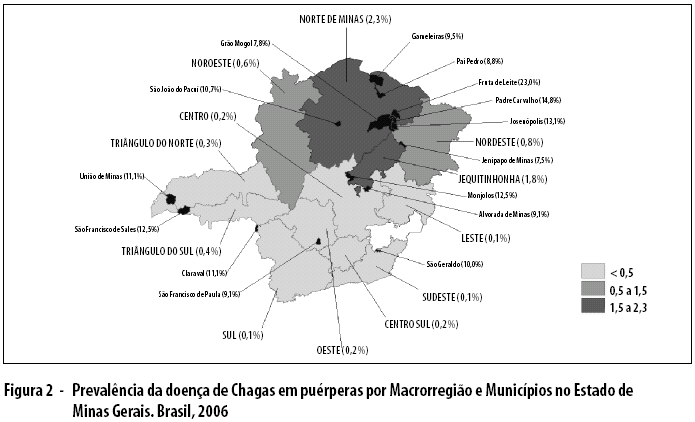
Nas 38.704 amostras provenientes dos Municípios endêmicos, foram encontradas 584 reações de ELISA positivas (1,5%), 29 indeterminadas (0,1%) e 38.091 negativas (98,4%). Para a Funed foram enviadas 8.400 amostras que revelaram, pela técnica de IFI, 365 reações positivas, 14 indeterminadas e 8.021 negativas. Dos exames submetidos à técnica de HAI, no total de 6.969, 314 foram positivos, seis indeterminados e 6.649 negativos. No total de amostras analisadas, 374 foram positivas (0,97%), 269 (0,69%) indeterminadas, 38.006 (98,3%) negativas e 55 amostras (0,14%) foram consideradas inadequadas para exame. A prevalência entre Municípios considerados endêmicos foi estimada em 1,0%, alcançando coeficientes elevados de até 23% em Fruta de Leite, na região norte do Estado, onde foram verificadas as maiores prevalências, de 2,3% (Figura 2).
]]>
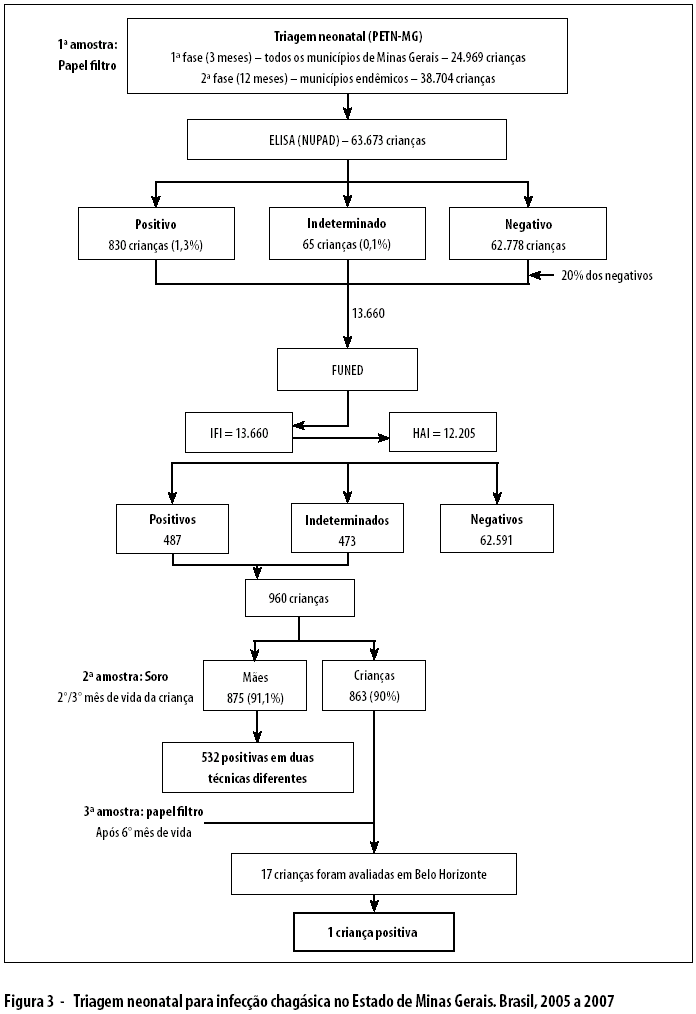
Considerando as duas primeiras fases do projeto (agosto de 2005 a outubro de 2006), identificaram-se 960 crianças com, pelo menos, uma amostra reativa no papel filtro. Dessas, foram obtidas alíquotas de soro em 875 (91,1%) mães e 863 (90%) crianças (Figura 3). Entre as mães, 532 (61 %) amostras foram positivas em duas técnicas diferentes.
Em todos os casos com amostras positivas fez-se o contato telefônico com a Unidade de Saúde, enfatizando o encaminhamento para avaliação clínica. Além disso, era enviado fax da comunicação para o responsável pela Triagem Neonatal daquela Unidade de Saúde, que deveria providenciar o contato com a mãe para informá-la do resultado. Cerca de 70% dos Municípios enviaram os relatórios referentes ao atendimento clínico das crianças/mães com a infecção chagásica. Após a avaliação médica inicial das crianças em seus Municípios, 17 delas foram encaminhadas e atendidas no Hospital das Clínicas, juntamente com suas mães. As crianças apresentaram-se assintomáticas. Apesar da solicitação de sorologia dos irmãos dos casos suspeitos, totalizando 42 pedidos, apenas quatro amostras foram encaminhadas para a Funed, todas com resultados negativos.
Para pesquisa de anticorpos anti-SAPA, foram analisadas 84 amostras com 42 pares mães-RNs que apresentavam sorologia positiva após seis meses de idade. Nessa população, nenhuma criança mostrou perfil de reatividade. Todas as crianças apresentaram perfis semelhantes aos perfis maternos.
No final do inquérito, identificaram-se duas crianças que preenchiam os critérios de caso. Entretanto, o diagnóstico foi confirmado em somente uma. Para a segunda criança, apesar da PCR positiva, os resultados sorológicos foram, repetidamente, negativos. As crianças foram submetidas à avaliação clínica, fundoscopia, radiografias de crânio e tórax, eletrocardiograma e ecocardiograma, que não mostraram alterações.
]]> O risco de transmissão vertical da infecção chagásica foi de 0,2%, representado pelo encontro de uma criança infectada no total de 532 mães positivas, (IC95% 0,00-0,56) e a incidência de infecção chagásica congênita foi de 1,6 em 100 mil nascidos vivos, ou seja uma criança infectada em 63.673 crianças examinadas, com intervalo de confiança a 95% variando de 0,00 a 5,0 (Figura 3). Após o término do tratamento específico, foram programadas reavaliações de seis em seis meses com exame clínico, hemocultura, PCR e sorologia para controle de cura, até os três anos de idade.A PCR foi negativa para a maioria das crianças, todavia 40 amostras de sangue dos recém-nascidos amplificaram o fragmento de 330pb do DNA do cinetoplasto do T. cruzi e estas não puderam ser confirmadas pela hibridização, devido a problemas técnicos para a obtenção da sonda (marcada com fosfatase alcalina) que estava sendo usada e foi descontinuada sua marcação por diferentes laboratórios. Em 17 pares mães/filhos foram colhidas novas amostras de sangue para a realização da técnica de hemocultura, e obteve-se uma positividade de 76,1% para as mães e 6,0% para as crianças. Estas crianças persistiram com IgG materna positiva entre os seis e nove meses de idade, com negativação da sorologia posteriormente.
Avaliação clínica das mães com sorologia positiva
Verificou-se que 18,8% das mães com infecção chagásica eram sintomáticas, e 10% necessitaram de acompanhamento cardiológico. Fato preocupante foi o relato de dois óbitos maternos, que ocorreram nos Municípios de Icaraí de Minas e Chapada do Norte. Uma paciente faleceu aos 43 anos, durante internação devido à taquiarritmia, estando anteriormente já em uso de antiarrítmico (amiodarona). O outro óbito, de uma mulher de 42 anos, foi domiciliar, por provável morte súbita. Possivelmente, os dois casos foram decorrentes da doença de Chagas.
Realização de cursos de Capacitação no Manejo Clínico do Paciente Chagásico
Durante o desenvolvimento do projeto, foram realizados três cursos de Capacitação no Manejo Clínico do Paciente Chagásico para sensibilização de profissionais de saúde para o problema da transmissão vertical. Em junho de 2007, com o término do projeto e análise do mapeamento dos Municípios com casos de infecção chagásica em mulheres adultas, e, constatada a extensão da doença, que ainda acomete a quase totalidade dos Municípios do Estado, optou-se, então, pela realização de um Seminário Eletrônico de Atualização no Manejo Clínico da Doença de Chagas. O Seminário visou à apresentação dos resultados do Inquérito Sorológico e a abordagem dos procedimentos clínicos adequados para o diagnóstico, acompanhamento e tratamento da doença, além de aspectos epidemiológicos e do Programa de Controle da endemia no Estado. Além da forma eletrônica, o evento contou com locais para a participação presencial em Belo Horizonte, Montes Claros e Jaíba. Todos os gestores municipais foram informados. Entre os Municípios com casos positivos, 56% participaram do evento. A principal razão alegada para a não-participação foi falta de infra-estrutura tecnológica de acesso à internet de alta velocidade.
Discussão
O declínio do total de casos em adultos pode ser atribuído ao controle do vetor, que culminou em 2003 com a certificação pela OPAS de eliminação do Triatoma infestans no Estado. As campanhas sistemáticas de controle do vetor, iniciadas no final da década de 1970, empregando modernos piretróides de síntese e atividades de vigilância com a luta química culminaram no controle do principal transmissor do T. cruzi.24 Focos residuais permanecem, especialmente em áreas pobres e mais isoladas, e a possibilidade de domiciliação de outras espécies significa que devem ser mantidos os programas de controle de vetores e a atenção aos pacientes com doença de Chagas. Os atuais desafios do controle da doença continuam em ações de prevenção e assistência para as milhões de pessoas infectadas, implantação de políticas médico-sociais que garantam acesso, cobertura, eqüidade e benefícios da Previdência social para aqueles com incapacidade laboral.
A infecção chagásica congênita pode ser considerada um agravo para o qual não se dispõe de prevenção primária, nem de marcador de transmissão ou de um diagnóstico imediato factível e sensível. O tratamento específico da gestante com doença de Chagas não está indicado pela toxicidade da droga disponível e possível efeito teratogênico sobre o concepto. Apesar do declínio da doença de Chagas em indivíduos mais jovens, em decorrência do bem sucedido Programa Brasileiro de Controle Vetorial, enquanto existirem grávidas com a infecção, haverá o risco de transmissão vertical da doença.
]]> Utilizou-se a identificação de IgG anti-T.cruzi no sangue do recém-nascido como marcador indireto da infecção materna. Essa opção baseou-se nas observações da correspondência entre os títulos de IgG materno e fetal a partir da 33o semana de gestação, embora alguns fatores possam influenciar o transporte placentário de IgG: anormalidades placentárias, concentração de IgG materna e a idade gestacional do feto.13 Considerando que a imensa maioria das crianças nasce a termo e que a fase crônica da infecção chagásica caracteriza-se por títulos elevados de IgG específica, avaliou-se como mínimas as possíveis perdas de mães infectadas e não identificadas por essa metodologia.O mapeamento dos Municípios do Estado demonstrou amplas oscilações nos coeficientes de prevalência da infecção chagásica em mulheres adultas, em idade reprodutiva, variando de 0,0 a 23,5%, com 14 Municípios apresentando prevalências superiores a 7,5%. O encontro de mães positivas reafirma a necessidade de manter a vigilância sobre a via de transmissão vertical, para a detecção precoce de crianças infectadas, quando a eficácia da medicação específica é próxima de 100%. O encaminhamento de crianças soropositivas ao Serviço de Infectologia ressalta a importância de vigilância das gestantes positivas e atenção médica precoce ao neonato exposto. A verificação de dois óbitos maternos, com grande probabilidade de terem sido relacionados à doença de Chagas, remete à necessidade de políticas de saúde pública que garantam a atenção à saúde dos indivíduos com a doença. A prevalência de 0,5%, apesar de ter sofrido redução em relação ao inquérito semelhante conduzido em 1997, ainda mostra a existência de 532 mulheres, em idade fértil, em risco de transmitir o parasito. O encontro de 19% com sintomatologia e sinais sugestivos de cardiopatia indica a necessidade de serviços de saúde preparados para prestar atenção médica adequada. Os dois óbitos maternos, provavelmente relacionados à doença de Chagas reafirmam a necessidade de atendimento pré-natal de qualidade. As mães procedentes de região endêmica ou com história epidemiológica positiva devem ser acompanhadas desde o pré-natal, com acesso aos procedimentos adequados às manifestações clínicas apresentadas. Gestantes portadoras de cardiopatias devem ser inseridas em serviços de pré-natal de alto risco para controle de possíveis complicações cardíacas e a indicação de cesariana, quando pertinente.
As taxas de transmissão congênita, assim como a mortalidade e a morbidade causadas pela infecção no recém-nascido são muito variáveis na literatura.3,4,25 No presente estudo, estimou-se o risco de transmissão vertical da infecção chagásica em 0,2% e a incidência de infecção chagásica congênita foi de 1,6 em 100 mil nascidos vivos. Trabalhos com metodologias diversas em países do Cone Sul relatam valores que oscilam de 2,4% na Argentina26 e de 4,6% na Bolívia, sem diferenças em relação ao nível de endemicidade do local de residência materna.27 A quase totalidade dos neonatos com infecção congênita (90%) nascem a termo, assintomáticos, permanecendo assim nos meses subseqüentes.15,27 A única experiência discordante ocorre na Bolívia, onde 50% das crianças são sintomáticas.6
O diagnóstico da infecção congênita deve ser realizado, preferencialmente, pela pesquisa do parasito, por técnicas de exame direto, como, por exemplo, o microhematócrio, que apresenta facilidade de execução e necessita de pequeno volume de sangue. Entretanto, operacionalmente este procedimento é mais complicado, pois nem todos os laboratórios contam com técnicos experientes na visualização do parasito ao microscópio. Outro fator complicador é a possibilidade de baixa parasitemia. Se o recém-nascido infectar-se durante o parto, o exame parasitológico pode resultar em um falso-negativo24 pela falta de tempo suficiente para a multiplicação do parasito. Exames mais complexos, como a PCR, estão disponíveis apenas em centros de pesquisa.28 Outros métodos, como a investigação de IgM, não se mostram de grande utilidade na infecção congênita,6 pois estudos demonstram sua negatividade na presença de infecção, ou mesmo a ocorrência de resultados falso-negativos. A detecção de anticorpos anti-SAPA,15 além de não estar comercializado, não se mostrou efetivo no presente estudo. Portanto, uma alternativa mais prática em casos de mães com a doença de Chagas é a repetição da sorologia da criança após a eliminação dos anticorpos IgG de origem materna. Neste estudo, a negativação mais tardia da sorologia, aos sete e nove meses, demonstra a necessidade do monitoramento até os nove meses, antes de considerar a criança como infectada, caso a sorologia após os seis meses persista reativa.
Dados na literatura demonstraram não haver diferença na morbidade, nos casos tratados no primeiro ano de vida, e a eficácia permanece alta, em torno de 90%.10 Na Argentina, o acompanhamento durante 30 anos demonstrou que as crianças que receberam tratamento até os três anos de idade negativaram a sorologia, sendo consideradas curadas.26 Trabalho semelhante observou a cura sorológica de 100% das crianças que iniciaram o tratamento com Nifurtimox durante os oito primeiros meses de vida e de 98% daquelas que foram tratadas até os três anos de idade.29 Nesse sentido, vale recomendar a solicitação de testes sorológicos em todos os filhos menores de 15 anos de mãe portadora da doença de Chagas, para os quais, ainda na fase de infecção crônica recente, o tratamento específico pode significar possibilidade de cura em torno de 70%.12,30
A alta possibilidade de cura da transmissão congênita justifica amplamente os esforços necessários para detectar a infecção pelo T. cruzi nas mães e seus recém-nascidos. O mapeamento das áreas endêmicas do estado e a eficácia do tratamento específico em crianças até um ano de idade são duas ferramentas poderosas para a intervenção do Estado no controle da transmissão congênita.
A detecção da transmissão da infecção chagásica em Minas Gerais por meio do PETN mostrou a exeqüibilidade da estratégia, especialmente pela facilidade da colheita do sangue em papel filtro, a elevada sensibilidade do teste ELISA e a existência de toda uma estrutura já regulamentada, que possibilita a entrega do resultado para a família e o agendamento de avaliação clínica em curto período de tempo. O teste para a doença de Chagas deveria ser incluído no Programa em todas as áreas com prevalência elevada, superior a 7%. O diagnóstico de infecção chagásica materna deve ser incluído entre os exames de pré-natal nos Municípios com prevalência superior a 5%.
Para os demais Municípios, todas as gestantes com história epidemiológica sugestiva da infecção chagásica devem ser submetidas à sorologia para detecção de anticorpos anti-T. cruzi. Os recém-nascidos, quando assintomáticos, devem ser submetidos à sorologia após os seis meses, e, caso permaneça positiva, deve ser repetida até os nove meses de nascimento, utilizando as reações convencionais disponíveis nos serviços de atenção primária. Para facilidade operacional, o exame pode ser solicitado quando da ida aos centros de saúde da Rede, para vacinação, entre os sete e 12 meses de idade. As crianças com sorologia reativa devem ser submetidas à avaliação clínica e tratamento específico, em regime ambulatorial, e seguimento oportuno.
Enquanto existir uma coorte de mulheres em idade fértil com infecção chagásica, devem ser mantidas estratégias de detecção precoce para o tratamento imediato das crianças positivas como Política de Saúde Pública. O Sistema de Saúde, especialmente nas áreas que, no passado, tiveram transmissão vetorial ativa, deve estar preparado para atender com qualidade os pacientes com doença de Chagas.
Finalmente, como política de Saúde Pública, a realização de provas sorológicas continua sendo a melhor opção de diagnóstico para a infecção chagásica congênita, por sua elevada sensibilidade, especificidade, facilidade operacional e os baixos custos, especialmente quando a criança estiver assintomática e tenha garantia de acompanhamento médico no primeiro ano de vida.
]]>Agradecimentos
Ao Ministério da Saúde, Programa de Triagem Neonatal do Núcleo de Ações e Pesquisa em Apoio Diagnóstico da Faculdade de Medicina/UFMG, aos laboratórios da Funed, Fiocruz e de Biologia do Trypanosoma cruzi e doença de Chagas do Departamento de Parasitologia do ICB-UFMG.
Referências
1. WHO. Seventeenth Programme Report, Special Programme and Training in Tropical Diseases Research (TDR) Progress 2003-2004. 2005: 30-4.
2. Gontijo ED, Andrade GMQ, Januzzi JH, Moreira E, Januário JN, Mourão O, et al. Doença de Chagas Congênita - Inquérito Sorológico em Minas Gerais - modelo e proposta. Revista da Sociedade Brasileira de Medicina Tropical 1998;31(Supl III):53.
3. Torrico F, Alonso-Vega C, Suarez E, Rodriguez P, Torrico MC, Dramaix M. Maternal Trypanosoma cruzi infection, pregnancy outcome, morbidity, and mortality of congenitally infected and non-infected newborns in Bolivia. American Journal of Tropical Medicine and Hygiene. 2004;70(2):201-9.
4. Gürtler RE, Segura EL, Cohen JE. Congenital transmission of Trypanosoma cruzi infection in Argentina. Emerging Infectious Diseases. 2003;9(1):29-32.
5. Streiger M, Fabbro D, Barco MD, Beltramino R, Bovero N. Chagas congenito en la ciudad de Santa Fe diagnostico y tratamiento. MEDICINA (Buenos Aires). 1995;55:125-33.
6. Carlier Y, Torrico F. Congenital infection with Trypanosoma cruzi: from mechanisms of transmission to strategies for diagnosis and control. Revista da Sociedade Brasileira de Medicina Tropical. 2003;36(6):767-71.
7. Truyens C, Mjihdi K, Lambot MA, Rivera MT, Noël C, Carlier Y. Efectos de la infección aguda y crônica por Trypanosoma cruzi em la gestación de los ratones. Revista da Sociedade Brasileira de Medicina Tropical. 2005;38(Supl 2):68-72.
8. Hermann E, Truyens C, Alonso-Vega C, Rodriguez P, Berthe A, Torrico F, et al. Congenital Transmission of Trypanosoma cruzi is associated with maternal enhanced parasitemia and decreased production of Interferon-γ in response to parasite antigens. The Journal of Infectious Diseases. 2004;189: 1274-81.
9. Rassi A, Neto VA, Rassi GG, Amato VS, Júnior AR, Luquetti AO, et al. Busca retrospectiva da transmissão maternal da infecção chagásica em pacientes na fase crônica. Revista da Sociedade Brasileira de Medicina Tropical. 2004;37(6):485-89.
10. Freilij B, Altcheh J. Congenital Chagas' disease: diagnostic and clinical aspects. Clinical Infectious Diseases. 1995;21:551-5.
11. Organización Panamericana de la Salud. Organización Mundial de la Salud. Tratamiento etiológico de la enfermidad de Chagas: conclusiones de reunion de especialistas. Revista de Patologia Tropical 1999;28(2):247-79.
12. Andrade ASS, Martelli CMT, Oliveira RM, Silva AS, Aires AIS, Soussumi LMT, et al. Short report: benznidazole efficacy among Trypanosoma cruzi-infected adolescents after a six-year follow-up. American Journal of Tropical Medicine and Hygiene. 2004;71(5):594-7.
13. Englund JA. The influence of maternal immunization on infant immune responses. Journal of Comparative Pathology. 2007;137(Supplement 1):S16-9.
14. Consenso Brasileiro em Doença de Chagas. Revista da Sociedade Brasileira de Medicina Tropical Secretaria de vigilância em saúde do Ministério da Saúde. 2005;38(Suppl. III).
15. Lorca MH, Bahamonde MI, García A, Tassara R, Urarte E, Contreras MdC, et al. Infección materna y transmisión transplacentaria del T. cruzi em Chile: diagnóstico, tratamiento y control. Revista da Sociedade Brasileira de Medicina Tropical 2005;38(Supl II):46-8.
16. Andrade AQ, Gontijo ED. Triagem neonatal para infecção chagásica congênita: aplicação de análise de classe latente para avaliação dos testes diagnósticos. Revista da Sociedade Brasileira de Medicina Tropical. 2008;41(6):1-6.
17. Umezawa ES, Shikanai-Yasuda MA, Stolf AM. Changes in isotype composition and antigen recognition of anti-Trypanosoma cruzi antibodies from acute to chronic Chagas disease. Journal of Clinical Laboratory Analysis. 1996;10(6):407-13.
18. Avila H, Siman DS, Cohen LM, Millikan RC, Simpson L. Polymerase chain reaction amplification of Trypanosoma cruzi kinetoplast minicircle DNA isolated from whole blood lysates: Diagnostic of chronic Chagas disease. Molecular and Biochemical Parasitology. 1991;48:211-22.
19. Gomes ML, Macedo AM, Vago AR, Pena SDJ, Galvão LMC, Chiari E. Trypanosoma cruzi: Optimization of polymerase chain reaction for detection in human blood. Experimental Parasitology 1998;88:28-33.
20. Britto C, Cardoso MA, Wincker P, Morel CMM. Simple protocol for cleavage of Trypanosoma cruzi kinetoplast DNA in blood and its use in polymerase chain reaction (PCR) based diagnosis of chronic Chagas' disease. Memórias do Instituto Oswaldo Cruz. 1993;88:171-2.
21. Degrave W, Fragoso SP, Britto C, Hieuverswyn HV, Kideane GZ, Cardoso MAB, et al. Peculiar sequence organization of kinetoplast DNA minicircles from Trypanosoma cruzi. Molecular and Biochemical Parasitology. 1988;27:63-70.
22. Santos FR, Pena SDJ, Epplen JT. Genetic and population study of a Y-linked tetranucleotide repeat DNA polymorphism with a simple non-isotopic technique. Human Genetics. 1993;90:655-6.
23. Chiari E, Dias JCP, Lana M, Chiari CA. Hemocultures for the parasitological diagnostic of human chronic Chagas' disease. Revista da Sociedade Brasileira de Medicina Tropical. 1989;22:19-23.
24. Dias JCP, Carvalho SH. Doença de Chagas. In: Farhat CK, Carvalho LHFR, Succi RCM, editors. Infectologia Pediátrica. São Paulo: Atheneu; 2007. p. 821-49.
25. Luquetti AO, Dias JC, Prata A. Transmísion congénita del T. cruzi em Brasil; Diagnóstico y tratamiento de la infección congénita por T. cruzi em Brasil. Revista da Sociedade Brasileira de Medicina Tropical. 2005;38(Supl II):27-8.
26. Moya P, Basso B, Moretti E. Enfermedad de Chagas Congénita em Córdoba, Argentina: aspectos epidemiológicos, clínicos, diagnósticos y terapêuticos. Experiencia de 30 años de seguimiento. Revista da Sociedade Brasileira de Medicina Tropical. 2005;38(Supl II):33-40.
27. Torrico F, Alonso-Vega C, Suarez E, Rodriguez P, Torrico MC, Dramaix M, et al. Nivel de endemia de la infección por T. cruzi en lugar de residencia de la madre y desarrollo de la enfermedad de Chagas congênita em Bolívia. Revista da Sociedade Brasileira de Medicina Tropical. 2005;38(Supl II):17-20.
28. Russomando G, Tomassone MMC, Guillen I, Acosta N, Vera N, Almiron M, et al. Treatment of congenital Chagas disease diagnosed and followed up by the polymerase chain reaction. American Journal of Tropical Medicine and Hygiene. 1998;59(3):487-91.
29. Altcheh J, Biancardi M, Lapeña A, Ballering G, Freilij H. Enfermedad de Chagas Congênita: experiencia del Hospital de Niños Ricardo Gutiérrez, Buenos Aires. Revista da Sociedade Brasileira de Medicina Tropical. 2005;38(Supl II):41-5.
30. Andrade ALSS, Zicker F, Oliveira RM, Silva SA, Luquetti A, Travassos LR. Randomised trial of efficacy of benznidazol e in treatment of early Trypanosoma cruzi infection. Lancet 1996;348:1407-13.
 Endereço para correspondência:
Endereço para correspondência:
Universidade Federal de Minas Gerais,
Faculdade de Medicina, ]]>
Av. Alfredo Balena, 190,
Santa Efigênia, Belo Horizonte-MG, Brasil.
CEP: 30130-100
E-mail:egontijo@medicina.ufmg.br
Recebido em 03/07/2008
Aprovado em 26/04/2009
*Pesquisa financiada pela Secretaria de Vigilância em Saúde com o apoio da Organização Pan-Americana da Saúde.
]]>