Eventos adversos notificados ao Sistema Nacional de Notificações para a Vigilância Sanitária (NOTIVISA): Brasil, estudo descritivo no período 2006 a 2011*
Adverse events notified on the Brazilian Health Surveillance Notification System (NOTIVISA): Brazil, descriptive study, 2006-2011
Jamile Rocha de Oliveira; Rosa Malena Fagundes Xavier; Aníbal de Freitas Santos Júnior
Departamento de Ciências da Vida, Universidade do Estado da Bahia, Salvador-BA, Brasil
]]>
RESUMO
OBJETIVO: descrever a ocorrência e características dos casos de eventos adversos (EA) notificados ao Sistema Nacional de Notificações para a Vigilância Sanitária (NOTIVISA).
MÉTODOS: estudo descritivo das notificações disponibilizadas pelo NOTIVISA, referentes ao período de 2006 a 2011.
RESULTADOS: verificou-se um aumento do número de notificações de EA a artigos médico-hospitalares, uso de sangue ou componente, cosméticos, saneantes e medicamentos no período estudado; o medicamento foi o produto mais relacionado à notificação de EA, com maior frequência em pacientes na faixa etária de 70 anos ou mais.
CONCLUSÃO: observou-se um crescimento no número total de notificações de EA relacionados a medicamentos, principalmente após a criação da Rede Sentinela, contribuindo para o fortalecimento da informação em vigilância de produtos farmacêuticos com potencial para causar reações adversas.
Palavras-chave: Toxicidade de Drogas; Sistemas de Notificação de Reações Adversas a Medicamentos; Farmacovigilância; Informação de Saúde ao Consumidor.
ABSTRACT
OBJECTIVE: to describe the occurrence and characteristics of adverse event (AE) cases reported on the Brazilian Health Surveillance Notification System (NOTIVISA). ]]>
METHODS: descriptive study of NOTIVISA notifications for the period 2006-2011.
RESULTS: there was an increase in the number of AE notifications relating to medical/hospital supplies, use of blood or blood products, cosmetics, disinfectants and medication during the study period. Medication was the product most related to AE notification, being more frequent in patients aged 70 years or older.
CONCLUSION: there was an increase in the total number of AE notifications relating to medication, especially following the creation of the Sentinel Network, contributing to the strengthening of surveillance information on pharmaceutical products with the potential to cause adverse reactions.
Key words: Drug Toxicity, Adverse Drug Reaction Reporting Systems, Pharmacovigilance, Consumer Health Information.
Introdução
As informações em saúde constituem ferramentas importantes para a implementação de ações e projetos em Saúde Coletiva e individual, uma vez que promovem melhor compreensão das mudanças de padrões epidemiológicos e do processo saúde-doença.1 Conceitualmente, um sistema de informações em saúde pode ser entendido como um instrumento para adquirir, organizar e analisar dados necessários à definição de problemas e riscos para a saúde. Tais dados podem servir de base para avaliar a eficácia e a eficiência dos serviços de saúde para a população, além de contribuir para a produção de conhecimento acerca da saúde,2 como por exemplo, das reações adversas a medicamentos (RAM), que devem ser monitoradas pela Vigilância em Saúde.
Para a Organização Mundial da Saúde (OMS), a expressão evento adverso (EA) é definida como "qualquer efeito inesperado ou indesejável que ocorra com um paciente que tenha recebido um produto farmacêutico e que não necessariamente tenha relação causal estabelecida com este tratamento".3 Assim, de acordo com a Agência Nacional de Vigilância Sanitária (Anvisa), um EA inclui "qualquer sinal desfavorável e não intencional (achados laboratoriais anormais, por exemplo), sintomas, ou doença temporariamente associada com o uso do medicamento".4 A identificação de EA é considerada uma informação valiosa para estimar a segurança da utilização dos produtos sob controle da Vigilância Sanitária, conferindo a qualidade do cuidado prestado ao paciente.5,6
Nas últimas décadas, ocorreu um desenvolvimento notável na descoberta de novos fármacos, os quais exigiram diversos estudos de eficácia e de segurança.7 Por exemplo, podem ocorrer EA mesmo quando os medicamentos são utilizados de forma racional.8 Os EA podem acarretar um aumento do número de óbitos e de hospitalizações em todo o mundo, com consequências epidemiológicas e econômicas graves.9 Em 2009, por exemplo, foram observados índices elevados de visitas médicas e hospitalizações após o uso de antiepilépticos; e em 2011, nos quatro hospitais da Rede Sentinela em Salvador-BA, foi encontrada uma prevalência de admissões hospitalares por reações adversas a medicamento (RAM) de 2,1%.10,11
]]> De acordo com Vasen e Fiorentino, a Farmacovigilância compreende "atividades relativas à identificação, avaliação, compreensão e a prevenção de efeitos adversos ou qualquer outro problema relacionado a medicamentos".12 Considerando-se a incapacidade dos ensaios clínicos preverem e descreverem todo o rol de RAM previamente, antes de seu lançamento no comércio, as EA devem ser investigadas no período pós-comercialização.13 No Brasil, a vigilância pós-comercialização de produtos voltados à saúde é uma área que necessita de maior investigação.14 Na Farmacovigilância, é fundamental o uso de sistemas de informações para obter dados que descrevam o perfil dos pacientes com EA, indicações de fármacos, duração da terapia, doses e eventos clínicos, sendo esses sistemas também muito úteis para o monitoramento de pacientes hospitalizados.15A notificação de EA no Sistema de Saúde brasileiro - SUS - é feita de forma espontânea, pelo profissional de saúde. Nishiyama, Bonetti e Bohm classificam a notificação de reações adversas em dois tipos: espontânea; e por busca ativa de RAM.16 A busca espontânea é considerada "de melhor relação custo-efetividade, na qual os profissionais de saúde preenchem um formulário de notificação fornecido pela Agência Nacional de Vigilância Sanitária (Anvisa), sendo, atualmente, a fonte principal de informação em Farmacovigilância". O método de busca ativa ocorre na forma de revisões dos prontuários e entrevistas com pacientes e/ou prescritores.
No Brasil, o Sistema Nacional de Notificações para a Vigilância Sanitária (NOTIVISA) é um sistema informatizado na plataforma WEB (internet), em âmbito de atuação municipal, estadual, distrital ou federal, previsto pela Portaria do Ministério da Saúde de no 1.660, de 22 de Julho de 2009. Podem utilizar e alimentar o sistema, após cadastro de acordo com a categoria do notificante, os profissionais de serviços de diversos órgãos sanitários e instituições de saúde, tais como: hospitais; clínicas; hemocentros; laboratórios; Centros de Integração e Apoio ao Trabalhador (CIAT), entre outros; Anvisa; Vigilâncias Sanitárias estaduais e municipais; Secretarias de Estado e Municipais de Saúde; e Laboratórios de Saúde Pública (Lacen). Ademais, podem notificar eventos as universidades e centros de pesquisa, haja vista seu papel relevante na divulgação e construção do saber científico. O sistema NOTIVISA também permite sua alimentação com dados fornecidos por profissionais que atuam em drogarias, farmácias, empresas detentoras de registro de produtos sob vigilância sanitária (fabricantes, importadores e distribuidores), além dos profissionais de saúde liberais.
O NOTIVISA recebe as notificações de eventos adversos e as queixas técnicas (QT) mediante registro em formulários específicos, relacionadas às seguintes categorias de produtos sob vigilância sanitária: medicamentos; vacinas e imunoglobulinas; artigos médico-hospitalares; equipamentos médico-hospitalares; produtos para diagnóstico de uso in vitro; uso de sangue ou componentes; cosméticos, produtos de higiene pessoal ou perfume; saneantes; e agrotóxicos'.17 O NOTIVISA tem como propósito fortalecer a vigilância pós-uso/pós-comercialização dos produtos supralistados. A publicação de relatórios anuais de notificações de EA e QT iniciou-se em 2007, ano de lançamento do sistema.
Para que a notificação espontânea de EA atingisse o volume e grau de confiança desejáveis, em 2001, foi criada a rede de Hospitais Sentinela para subsidiar o Sistema Nacional de Vigilância Sanitária, com o objetivo de obter informação qualificada e criar um ambiente hospitalar favorável ao envolvimento de ações de vigilância sanitária. Segundo a Anvisa, atualmente, "a rede conta com 247 instituições que atuam no monitoramento e notificação de EA com a responsabilidade de identificar produtos com problemas que comprometam a qualidade e a segurança do seu uso".18 Ainda segundo a Anvisa, a rede está estruturada com a seguinte distribuição das instituições credenciadas, públicas e privadas, por região: Norte, 26 hospitais; Nordeste, 55 hospitais; Centro-Oeste, 16 hospitais; Sudeste, 107 hospitais; e região Sul, 43 hospitais.
O presente estudo teve como objetivo descrever a ocorrência e as características dos casos de eventos adversos notificados ao Sistema Nacional de Notificações para a Vigilância Sanitária, no período 2006 a 2011.
Métodos
Trata-se de um estudo descritivo, com base nos dados contidos nos Relatórios de Eventos Adversos, publicados e disponibilizados no sítio eletrônico http://www.anvisa.gov.br/hotsite/notivisa/relatorios/index.htm desde a implantação do NOTIVISA. A partir de uma análise documental, diretamente no sítio eletrônico do sistema, foi traçado o perfil das notificações referentes a EA, disponibilizadas pelo NOTIVISA no período de 2006 a 2011, em todos os âmbitos de atuação. Foram coletados os dados a partir de 2008, quando a Anvisa começou a publicar os relatórios do NOTIVISA.
Foram estudadas as seguintes variáveis:
]]> - número total de notificações - todas as notificações de EA realizadas a cada ano;- categorias de produto/motivo notificadas - medicamentos; vacina e imunoglobulina; artigo médico-hospitalar; equipamento médico-hospitalar; produto para diagnóstico de uso in vitro; uso de sangue ou componente; cosméticos; saneantes; e intoxicações;
- tipo detalhado de notificante - identificação da classe profissional responsável pelas notificações;
- faixa etária dos indivíduos que sofreram o EA - <1 ano; 1 a 4; 50 a 59; 60 a 69; e 70 anos ou mais; e
- sexo dos indivíduos que sofreram o EA.
Para a análise e interpretação dos dados, foram utilizadas as tabelas fornecidas pelo sistema NOTIVISA. Os dados foram compilados segundo o ano do relatório analisado (2006 a 2011). Com base nas informações contidas nas notificações, foi elaborado um banco de dados com um subconjunto das cinco variáveis estudadas. A análise estatística foi realizada a partir da distribuição de frequência das demais variáveis segundo o sexo, por meio do teste qui-quadrado. Foi considerado significativo estatisticamente o valor de p<0,05.
Por se tratar de um estudo realizado exclusivamente com dados secundários de domínio público, não foi necessária sua aprovação pelo Comitê de Ética em Pesquisa (CEP), conforme recomendações do Conselho Nacional de Saúde em sua Resolução CNS no 466/2012.
Resultados
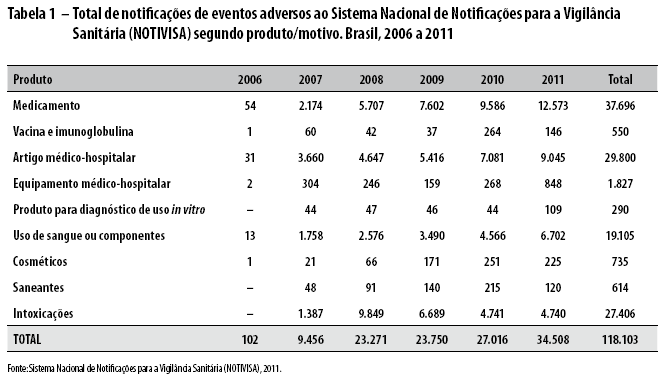
A Tabela 1 apresenta o total de notificações por produto/motivo, no período de 2006 a 2011 (Tabela 1).
]]>

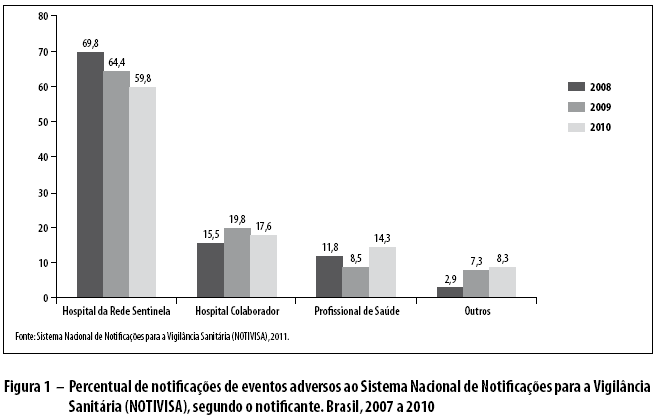
A Figura 1 apresenta os dados referentes ao detalhamento do notificante, conforme os relatórios publicados - por unidade notificante - pelo NOTIVISA a partir de 2008: hospitais da Rede Sentinela, 69,8%; hospitais colaboradores, 15,5%; e profissionais de saúde, 11,8%.
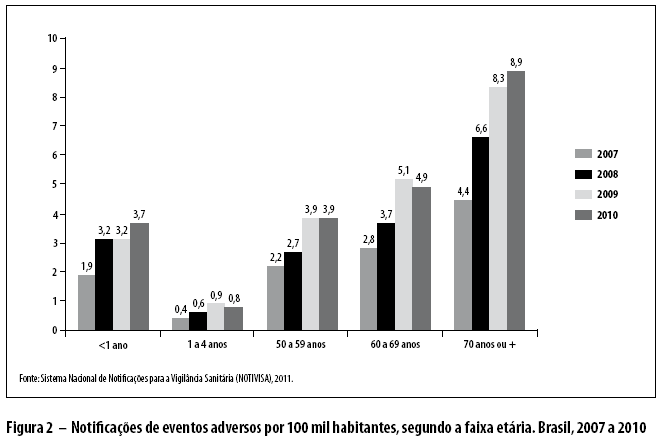
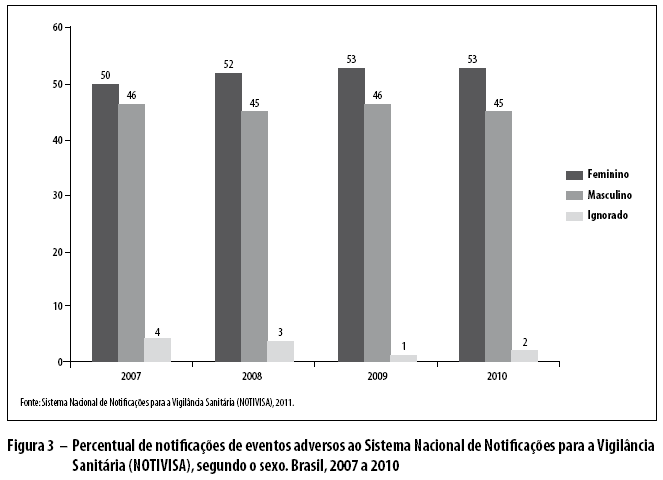
As figuras 2 e 3 apresentam o percentual de notificações por faixa etária do paciente e por sexo, respectivamente, entre os anos de 2007 e 2010. Não houve diferenças entre os sexos quanto à notificação de EA, no período avaliado.
]]>
Discussão
Os dados obtidos mostraram que as notificações de EA por produto/motivo (artigos médico-hospitalares, uso de sangue ou componente, cosméticos, saneantes e medicamentos) aumentaram significativamente no período estudado, principalmente para crianças e idosos, independentemente do sexo. Observou-se aumento do número de notificações de EA por uso de medicamentos, sangue e hemoderivados, a partir de 2007.
]]> A faixa etária constitui uma das variáveis mais importantes para uma maior avaliação de eventos adversos a medicamentos, especialmente em pacientes pediátricos, menores de cinco anos de idade,19 e geriátricos. Os idosos constituem um grupo populacional onde são observadas alterações fisiológicas, que podem afetar, significativamente, os parâmetros farmacocinéticos e farmacodinâmicos de fármacos.20 Além disso, os indivíduos dessa faixa etária utilizam diversos medicamentos para o tratamento de enfermidades e comorbidades associadas ao processo de envelhecimento, necessitam de um acompanhamento especial durante o tratamento farmacoterapêutico e, muitas vezes, carecem inclusive de um ajuste posológico.21De acordo com Fonteles e colaboradores, as mulheres apresentam maior percentual de envolvimento em EA, provavelmente devido a fatores como "diferenças no peso corporal, níveis hormonais ou consumo de medicamentos, maior frequência às consultas médicas e maior cumprimento/adesão às prescrições médicas".22 Apesar do aumento do número de notificações, não houve associação significativa (p>0,05) entre EA e sexo.
O aumento do número de notificações de EA por uso de sangue e hemoderivados a partir de 2007 indica que a implantação do NOTIVISA representou um avanço para a Hemovigilância, pois facilitou as notificações das reações transfusionais, seu monitoramento e a tomada de ações de correção dos problemas identificados, tanto de parte dos órgãos que compõem o Sistema Nacional de Vigilância Sanitária como dos serviços de hemoterapia e serviços de saúde.23
Houve crescimento no número total de notificações de EA a medicamentos, por ano. Alguns fatores podem ter proporcionado o aumento das notificações de EA: (i) aumento da busca pelas instituições de saúde, o que favorece o uso de medicamentos; (ii) descoberta de novos fármacos; (iii) maior acesso a medicamentos por diversos mecanismos, como por exemplo, a difusão dos genéricos e outros programas de saúde do governo; e, entre outros, (iv) o desenvolvimento e difusão da Farmacovigilância, que, por meio de sistemas de informações em saúde, favorece a notificação de EA. Apesar dessas variáveis incentivarem a identificação de eventos adversos, o número real de EA que podem ser detectados ainda é considerado baixo, provavelmente devido à subnotificação.24
Faz-se necessária uma maior participação dos profissionais da saúde na notificação de EA, contribuindo, dessa forma, para a ampliação e divulgação das atividades da Farmacovigilância.25 Entretanto, falta tradição dos profissionais de saúde em notificar; ou sobra o medo de que o reconhecimento de eventos adversos possa refletir negativamente na imagem de competência desses profissionais e os coloque sob risco de processo legal.26 A subnotificação também pode estar relacionada a outros fatores: falhas durante o ensino médico; ação pouco expressiva dos conselhos de classe na vigilância da qualidade da prescrição; e inércia dos pacientes e seus familiares na luta por direitos frente à iatrogenia, ou seja, os efeitos e complicações resultantes de um tratamento médico.27
Em 2010, 59,8% das notificações realizadas no sistema NOTIVISA foram feitas por hospitais da Rede Sentinela, 14,3% por profissionais de saúde e 8,3% por hospitais, não sendo relatado o percentual de hospitais colaboradores como tipo detalhado de notificante. Naquele contexto, os hospitais da Rede Sentinela representaram o principal notificante porque são motivados e qualificados para a notificação de eventos adversos e queixas técnicas de produtos de saúde. No ambiente hospitalar, apesar de serem monitorados por uma equipe multiprofissional capaz de reconhecer e notificar EA, pacientes internados são, normalmente, expostos a diversos fármacos e susceptíveis a EA, que podem conduzir ao óbito.28
Alguns fatores - comuns, quando se utilizam fontes de dados secundários - poderiam constituir limitações para o presente estudo, principalmente no que se refere ao método da notificação espontânea preconizado pelo NOTIVISA. Tal método consiste na quantificação de reações produzidas por diversos produtos, disponíveis no mercado, como causa de determinadas reações adversas; porém, ele não permite a avaliação da segurança e eficácia desses produtos para a Saúde Coletiva e individual. Além desta, outra possível limitação deste estudo reside na possibilidade de subnotificação, que pode camuflar a real ocorrência de agravos à saúde.
O monitoramento de qualquer problema relacionado com um medicamento constitui o atual desafio da Farmacovigilância. Contudo, estudos clínicos são insuficientes para identificar e delimitar a resposta, a segurança e a eficácia de medicamentos usados por extensos e heterogêneos grupos populacionais, como se apresenta a miscigenação da população brasileira.29
As informações em saúde são instrumentos fundamentais para a Farmacovigilância porque permitem o rastreamento de situações de risco e EA potenciais referentes ao uso de medicamentos e outros produtos voltados à saúde. As notificações recebidas pelos sistemas de Farmacovigilância - sobre os padrões de consumo da população, a segurança do produto, o impacto que os eventos adversos promovem na Saúde Pública e nos custos da Saúde - devem servir de informação para definir as políticas públicas de medicamentos.
Também se faz necessária uma integração da Farmacovigilância com o desenvolvimento de atividades de Atenção Farmacêutica e Farmacologia Clínica, no país. Os farmacêuticos podem contribuir para a disseminação de informações, especialmente em ações de promoção do uso racional de medicamentos.
]]> Conclui-se que há necessidade de o sistema NOTIVISA revisar periodicamente seus formulários de notificação, para promover melhorias no serviço e evolução do sistema em si. A divulgação das informações obtidas pelo sistema, não só na forma de dados brutos e gráficos como também na discussão de seus resultados, em alertas e boletins informativos, dão acesso imediato ao conhecimento clínico, compreensão e análise dos eventos adversos pelos profissionais de saúde e a comunidade geral, visando à melhoria da qualidade de vida da população.
Agradecimentos
Ao grupo de pesquisa 'Uso racional de medicamentos como necessidade de saúde', da Universidade do Estado da Bahia - UNEB -, pelo estímulo à discussão e promoção do uso racional de medicamentos.
Contribuição dos autores
Oliveira JR e RMF Xavier participaram da coleta e análise dos dados.
Todos os autores participaram da concepção, delineamento do estudo, elaboração, análise e revisão final do artigo.
Todos os autores aprovaram a versão final do manuscrito, e são responsáveis por todos os aspectos do trabalho, incluindo a garantia de sua precisão e integridade.
]]> Referências
1. Malta DC, Leal MC, Costa MFL, Morais Neto OL. Inquéritos nacionais de saúde: experiência acumulada e proposta para o inquérito de saúde brasileira. Rev Bras Epidemiol. 2008 mai;11 Suppl 1:159-67.
2. Branco MAF. Sistemas de informação em saúde no nível local. Cad Saude Publica. 1996 abr-jun;12(2):267-70.
3. World Health Organization. Department of essential drugs and medicines. The Uppsala Monitoring Centre. The importance of pharmacovigilance: safety monitoring of medicinal products. Genebra: World Health Organization; 2002.
4. Ministério da Saúde (BR). Agência Nacional de Vigilância Sanitária. Sistema Nacional de Notificações para a Vigilância Sanitária: módulo de notificação. [citado 2011 abr 10]. Disponível em: http://www.anvisa.gov.br/hotsite/notivisa/manual/ea_medicamento_profissional.pdf
5. Roque KE, Melo ECP. Adaptação dos critérios de avaliação de eventos adversos a medicamentos para uso em um hospital público no estado do Rio de Janeiro. Rev Bras Epidemiol. 2010 dez;13(4):607-19.
6. Torres AS, Mota ELA. Notificação de eventos adversos em vigilância sanitária: incompletitude das variáveis do Notivisa em 2007 e 2008. Cad Saude Colet. 2010 jan-mar;18(1):133-43.
7. Gomes SMM. Notificação de reacções adversas medicamentosas: sua relevância para a saúde pública. Rev Port Saude Publica. 2001 jul-dez;19(2):5-14.
8. Rigo KGP, Nishiyama P. A evolução da farmacovigilância no Brasil. Acta Sci Health Sci. 2005;27(2):131-5.
9. Arrais PSD, Vidotti CCF, Heleodoro NM, Martins R, Castilho SR. Sistema Nacional de Farmacovigilância: propostas de contribuição do Sistema Brasileiro de Informação sobre Medicamentos. Saude Debate. 2002 mai-ago;26(61):210-8.
10. Guilhoto LMFF, Alexandre V, Martins HH, Santos CM, Lin K, Silva ARCO, et al. Há riscos na utilização de diferentes formulações de drogas antiepilépticas? Relato da ABE através de entrevista de pessoas com epilepsia. J Epilepsy Clin Neurophysiol. 2009 mar;15(1):41-9.
11. Noblat ACB, Noblat LACB, Toledo LAK, Santos PM, Oliveira MGG, Tanajura GM, et al. Prevalência de admissão hospitalar por reação adversa a medicamentos em Salvador, BA. Rev Assoc Med Bras. 2011 jan-fev;57(1):42-5.
12. Vasen W, Fiorentino RML. Farmacovigilancia: una herramienta poco utilizada. Medicina (B. Aires). 2006 may-jun;66(3):257-62.
13. Dias MF. Introdução à Farmacovigilância. In: Storpirtis S, Mori ALPM, Yochiy A, Ribeiro E, Porta V. Farmácia clínica e atenção farmacêutica. Rio de Janeiro: Guanabara Koogan; 2008. p. 46-63.
14. Rabelo RB. Vigilância pós-comercialização de produtos para a saúde: o desafio da rede sentinela [dissertação]. Recife (PE): Fundação Oswaldo Cruz; 2007.
15. Louro E, Romano-Lieber NS, Ribeiro E. Adverse events to antibiotics in inpatients of a university hospital. Rev Saude Publica. 2007 Dec;41(6):1042-8.
16. Nishiyama P, Bonetti MFS, Böhm ACF, Margonato FB. Experiência de farmacovigilância no Hospital Universitário Regional de Maringá, Estado do Paraná. Acta Sci, Health Sci. 2002;24(3):749-55.
17. Ministério da Saúde (BR). Sistema Nacional de Notificações em Vigilância Sanitária. Bem-vindo ao Sistema Nacional de Notificações para a Vigilância Sanitária. [citado 2011 mar]. Disponível em: http://www.anvisa.gov.br/hotsite/notivisa/apresenta.htm
18. Ministério da Saúde (BR). Agência Nacional de Vigilância Sanitária. Rede Sentinela. [citado 2013 jul 30]. Disponível em: http://portal.anvisa.gov.br/wps/content/Anvisa+Portal/Anvisa/Pos+-+Comercializacao+-+Pos+-+Uso/Rede+Sentinela
19. Ramos CLJ, Targa MBM, Stein, AT. Perfil das intoxicações na infância atendidas pelo centro de informação toxicológica do Rio Grande do Sul Brasil. Cad Saude Publica. 2005 jul-ago;21(4):1134-41.
20. Clewell HJ, Teeguarden J, McDonald T, Sarangapani R, Lawrence G, Covington T, et al. Review and evaluation of the potential impact of age-and gender-specific pharmacokinetic differences on tissue dosimetry. Crit Rev Toxicol. 2002 Set;32(5):329-89.
21. Nóbrega OT, Karnikowsk MGO. A terapia medicamentosa no idoso: cuidados na medicação. Cienc Saude Coletiva. 2005;10(2):309-313.
22. Fonteles MMF, Francelino EV, Santos LKX, Silva KM, Siqueira R, Viana GSB, et al. Reações adversas causadas por fármacos que atuam no sistema nervoso: análise de registros de um centro de farmacovigilância do Brasil. Rev Psiquiatr Clin. 2009;36(4):137-44.
23. Proietti ABFC, Cioffi JGM. Hemovigilância: verificação final da qualidade da transfusão? Rev Bras Hematol Hemoter. 2008;30(3):173-6.
24. Romeu GA, Távora MRF, Costa AKM, Souza MOB, Gondim APS. Notificação de reações adversas em um hospital sentinela de Fortaleza (CE). Rev Bras Farm Hosp Serv Saude. 2011 jan-abr;2(1):5-9.
25. Dresch C. A Farmacovigilância e a atenção primária à saúde: diálogo possível e necessário. Rev APS. 2006 jan-jun;9(1):73-82.
26. Organização Mundial da Saúde. Monitorização da segurança de medicamentos: diretrizes para criação e funcionamento de um centro de farmacovigilância. Brasília: Organização Pan-Americana da Saúde; 2005.
27. Fiorati RC, Saeki T. O acompanhamento terapêutico na internação hospitalar: inclusão social, resgate de cidadania e respeito à singularidade. Interface (Botucatu). 2008 out-dez;12(27):763-72.
28. Bortoletto ME, Bochner R. Impacto dos medicamentos nas intoxicações humanas no Brasil. Cad Saude Publica. 1999 out-dez;15(4):859-69.
29. Organização Mundial da Saúde. Departamento de medicamentos essenciais e outros medicamentos. A importância da farmacovigilância: monitorização da segurança dos medicamentos. Brasília: Organização Pan-Americana da Saúde; 2005.
 Endereço para correspondência:
Endereço para correspondência:
Aníbal de Freitas Santos Júnior
- Universidade do Estado da Bahia,
Departamento de Ciências da Vida,
Campus I, Rua Silveira Martins, no 2555,
Cabula, Salvador-BA, Brasil.
CEP: 41150-000
E-mail: afjunior@uneb.br
*Trabalho de Conclusão de Curso, apresentado ao Curso de Graduação em Farmácia da Universidade do Estado da Bahia como requisito para obtenção do grau em Bacharel em Farmácia no ano de 2011.
]]>